1 . 25℃时,某酸H2R溶液中存在的各种含R元素微粒在总浓度中所占分数δ随溶液pH的变化关系如图所示。已知常温下Ksp(MR)=1.0×10-18,M2+不水解。下列叙述正确的是
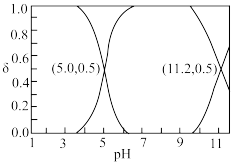
| A.常温下H2R的二级电离常数K的数量级为10-11 |
| B.NaHR溶液中,c(H2R)<c(R2-) |
C.反应H2R(aq)+M2+(aq) MR(s)+2H+(aq)的平衡常数K=101.8 MR(s)+2H+(aq)的平衡常数K=101.8 |
| D.向MR的饱和溶液中加酸调节至中性,则一定存在:2c(M2+)=2c(R2-)+c(HR-) |
您最近一年使用:0次
2 . 甘氨酸(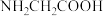 )是人体必需氨基酸之一,25℃时,甘氨酸溶液中
)是人体必需氨基酸之一,25℃时,甘氨酸溶液中 、
、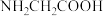 、
、 的分布分数与溶液
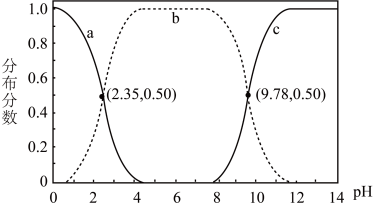
的分布分数与溶液 关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
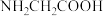 )是人体必需氨基酸之一,25℃时,甘氨酸溶液中
)是人体必需氨基酸之一,25℃时,甘氨酸溶液中 、
、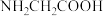 、
、 的分布分数与溶液
的分布分数与溶液 关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
| A.甘氨酸具有两性 |
B.曲线c代表 |
C. 的平衡常数 的平衡常数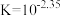 |
D.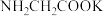 溶液中 溶液中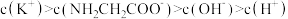 |
您最近一年使用:0次
3 . 某实验小组根据以下装置制备84消毒液,并探究84消毒液的性质。 ,若温度超过
,若温度超过 ,会生成
,会生成 杂质。
杂质。
回答下列问题:
I.84消毒液的制备
(1)仪器a的名称为___________ 。
(2)装置A中反应的离子方程式为___________ 。
(3)装置B的作用是___________ (任写一个即可)。
(4)制备 溶液时,为减少
溶液时,为减少 杂质的产生,应采取的措施是
杂质的产生,应采取的措施是___________ (写两条)。
(5)为探究 性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
Ⅱ.探究84消毒液的性质
84消毒液和医用酒精均为重要的消毒剂且二者不能混用,某小组对84消毒液与医用酒精的反应产物进行了探究。
【提出假设】医用酒精中的 被氧化为
被氧化为
【实验方案】实验方案及现象如下:
【实验结论1】
(6)产物中有乙醛,且乙醛会被转化为其它物质。补充①的实验现象:___________ 。
【查阅资料】混合体系中可能发生以下反应:

 (卤化反应)
(卤化反应)
【实验设计】取2份 84消毒液,缓慢滴加医用酒精或蒸馏水各
84消毒液,缓慢滴加医用酒精或蒸馏水各 ,通过测定过程中
,通过测定过程中 变化判断是否发生卤化反应(忽略过程中的热效应对
变化判断是否发生卤化反应(忽略过程中的热效应对 的影响)。实验结果如图。
的影响)。实验结果如图。 增大,说明乙醛发生了卤化反应。
增大,说明乙醛发生了卤化反应。
【查阅资料】某同学查阅资料后认为结论2不严谨,原因是工业上为了稳定 ,在84消毒液中添加了少量
,在84消毒液中添加了少量 ,且由于乙醇的“锁水”效应也会使
,且由于乙醇的“锁水”效应也会使 增大(提示:乙醇与
增大(提示:乙醇与 不反应)。
不反应)。
【数据分析】②已知上述实验:84消毒液中 。
。
(7)通过计算证明84消毒液中添加了少量 ,写出计算过程
,写出计算过程___________ 。
【优化实验】③该同学增加了对照实验,证明反应生成了 。
。
(8)请简述方案和结果:___________ 。
实验总结:医用酒精中的乙醇能被84消毒液氧化为乙醛,乙醛能进一步发生卤化反应。

 ,若温度超过
,若温度超过 ,会生成
,会生成 杂质。
杂质。回答下列问题:
I.84消毒液的制备
(1)仪器a的名称为
(2)装置A中反应的离子方程式为
(3)装置B的作用是
(4)制备
 溶液时,为减少
溶液时,为减少 杂质的产生,应采取的措施是
杂质的产生,应采取的措施是(5)为探究
 性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
A.饱和 溶液 溶液 | B. 溶液 溶液 | C. | D.浓硫酸 |
Ⅱ.探究84消毒液的性质
84消毒液和医用酒精均为重要的消毒剂且二者不能混用,某小组对84消毒液与医用酒精的反应产物进行了探究。
【提出假设】医用酒精中的
 被氧化为
被氧化为
【实验方案】实验方案及现象如下:
| 实验操作 | 取样检测时间点 | 实验现象 |
常温下将 医用酒精和 医用酒精和 84消毒液混合,在不同反应时间点,分别取 84消毒液混合,在不同反应时间点,分别取 反应后的溶液滴加到新制氢氧化铜悬浊液中加热 反应后的溶液滴加到新制氢氧化铜悬浊液中加热 |  | ① |
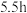 | 橙黄色沉淀 | |
 | 黑色沉淀 |
(6)产物中有乙醛,且乙醛会被转化为其它物质。补充①的实验现象:
【查阅资料】混合体系中可能发生以下反应:

 (卤化反应)
(卤化反应)【实验设计】取2份
 84消毒液,缓慢滴加医用酒精或蒸馏水各
84消毒液,缓慢滴加医用酒精或蒸馏水各 ,通过测定过程中
,通过测定过程中 变化判断是否发生卤化反应(忽略过程中的热效应对
变化判断是否发生卤化反应(忽略过程中的热效应对 的影响)。实验结果如图。
的影响)。实验结果如图。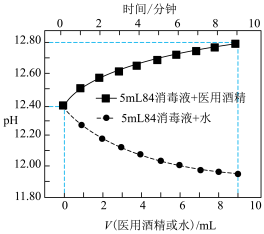
 增大,说明乙醛发生了卤化反应。
增大,说明乙醛发生了卤化反应。【查阅资料】某同学查阅资料后认为结论2不严谨,原因是工业上为了稳定
 ,在84消毒液中添加了少量
,在84消毒液中添加了少量 ,且由于乙醇的“锁水”效应也会使
,且由于乙醇的“锁水”效应也会使 增大(提示:乙醇与
增大(提示:乙醇与 不反应)。
不反应)。【数据分析】②已知上述实验:84消毒液中
 。
。(7)通过计算证明84消毒液中添加了少量
 ,写出计算过程
,写出计算过程【优化实验】③该同学增加了对照实验,证明反应生成了
 。
。(8)请简述方案和结果:
实验总结:医用酒精中的乙醇能被84消毒液氧化为乙醛,乙醛能进一步发生卤化反应。
您最近一年使用:0次
4 . 常温下,用 的
的 溶液滴定
溶液滴定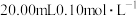 的HX溶液,所得滴定曲线如图所示,下列说法不正确的是
的HX溶液,所得滴定曲线如图所示,下列说法不正确的是

 的
的 溶液滴定
溶液滴定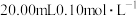 的HX溶液,所得滴定曲线如图所示,下列说法不正确的是
的HX溶液,所得滴定曲线如图所示,下列说法不正确的是
| A.HX为强酸 |
B.对应溶液中水的电离程度: |
C.c点所示的溶液中: |
D.相同条件下, 的水解能力弱于 的水解能力弱于 的电离能力 的电离能力 |
您最近一年使用:0次
解题方法
5 . 常温下,用NaOH溶液滴定NaH2PO4溶液,溶液pH与 的关系如图所示。下列关系正确的是
的关系如图所示。下列关系正确的是
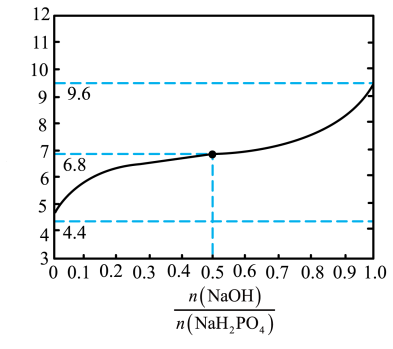
 的关系如图所示。下列关系正确的是
的关系如图所示。下列关系正确的是
A.常温下, |
B.当 =0.5时,水的电离程度最大 =0.5时,水的电离程度最大 |
C.向0.1mol/L的NaH2PO4溶液中滴加NaOH溶液至中性: |
D.0.1mol/LNaH2PO4溶液与0.1mol/LNa3PO4溶液等体积混合:  |
您最近一年使用:0次
名校
解题方法
6 . 298K时,在20mL0.1mol•L-1H2R稀溶液中滴入相同浓度的NaOH溶液,用pH传感器测得混合溶液的pH变化曲线如图所示(已知的H2R的Ka2为1.0×10-10),下列有关叙述正确的是


| A.H2R的Ka1约为1.0×10-3 |
| B.a点存在:c(HR-)>c(R2-) |
| C.b点时:c(Na+)>c(HR-)>c(R2-)>c(H2R) |
| D.c点时:2c(H+)+3c(H2R)+c(HR-)=2c(OH-)+c(R2-) |
您最近一年使用:0次
名校
7 . 下列有关电解质溶液的说法正确的是
A.向盐酸中加入氨水至中性,溶液中 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
| C.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大 |
D.0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中 |
您最近一年使用:0次
解题方法
8 . 25℃时,将0.01mol•L-1的盐酸逐滴加到10mL0.01mol•L-1NaA溶液中,A-、HA物质的量所占分数(δ)、pH变化曲线如甲、乙图所示。下列溶液中微粒的物质的量浓度关系正确的是


| A.溶液显中性时:c(Cl-)=c(HA) |
| B.图甲中a点对应的溶液:c(A-)<c(Cl-) |
| C.图乙中b点对应的溶液:c(Cl-)>c(HA) >c(A-)>c(OH-)>c(H+) |
| D.a点对应的pH=9.5,则常温下,HA的电离平衡常数:Ka(HA)=10-4.5 |
您最近一年使用:0次
9 . 腺嘌呤(A)是一种有机弱碱,用 的盐酸溶液滴定
的盐酸溶液滴定 的A溶液可生成AHCl溶液,溶液pH变化曲线如图所示,下列说法正确的是
的A溶液可生成AHCl溶液,溶液pH变化曲线如图所示,下列说法正确的是

 的盐酸溶液滴定
的盐酸溶液滴定 的A溶液可生成AHCl溶液,溶液pH变化曲线如图所示,下列说法正确的是
的A溶液可生成AHCl溶液,溶液pH变化曲线如图所示,下列说法正确的是
A.腺嘌呤的 值数量级为 值数量级为 |
B. |
C.a~b过程中, 的值逐渐减小 的值逐渐减小 |
D.滴入盐酸过程中,溶液中一直存在 |
您最近一年使用:0次
名校
10 . 已知: 。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随
。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
变化关系如图所示。下列说法错误的是
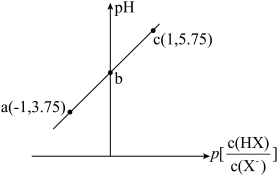
 。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随
。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
变化关系如图所示。下列说法错误的是
| A.溶液中水的电离程度:a<b<c |
B.b点溶液中: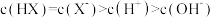 |
C.c点溶液中: |
D.室温下NaX的水解平衡常数为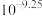 |
您最近一年使用:0次



