1 . 甘氨酸(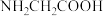 )是人体必需氨基酸之一,25℃时,甘氨酸溶液中
)是人体必需氨基酸之一,25℃时,甘氨酸溶液中 、
、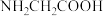 、
、 的分布分数与溶液
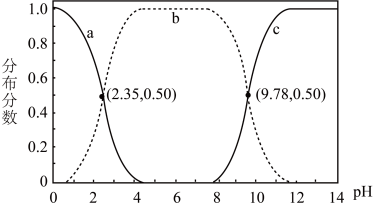
的分布分数与溶液 关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
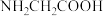 )是人体必需氨基酸之一,25℃时,甘氨酸溶液中
)是人体必需氨基酸之一,25℃时,甘氨酸溶液中 、
、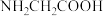 、
、 的分布分数与溶液
的分布分数与溶液 关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
关系如图(分布分数即各组分的平衡浓度占总浓度的分数)。下列说法不正确的是
| A.甘氨酸具有两性 |
B.曲线c代表 |
C. 的平衡常数 的平衡常数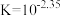 |
D.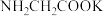 溶液中 溶液中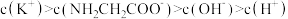 |
您最近半年使用:0次
23-24高二上·广东深圳·期末
名校
解题方法
2 . 回答下列问题
(1)某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
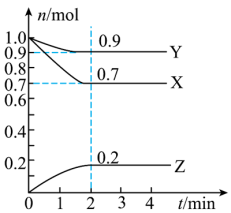
①反应从开始至2min,用Z的浓度变化表示的平均反应速率为v(Z)=___________ 。
②由图中所给数据进行分析,该反应的化学方程式为___________ 。
③下列措施能加快反应速率的有___________ 。
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.升高温度
(2)已知25℃时H3PO4的各级电离平衡常数如表所示:
①NaH2PO4水解反应的离子方程式为___________ ;其水解常数Kh=___________ (保留3位有效数字),NaH2PO4溶液呈___________ 性。(填“酸”、“碱”或“中”)
②计算H2PO +PO
+PO
 2HPO
2HPO 的平衡常数K=
的平衡常数K=___________ (保留2位有效数字)。
(1)某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。

①反应从开始至2min,用Z的浓度变化表示的平均反应速率为v(Z)=
②由图中所给数据进行分析,该反应的化学方程式为
③下列措施能加快反应速率的有
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.升高温度
(2)已知25℃时H3PO4的各级电离平衡常数如表所示:
| 平衡常数 | H3PO4 |
| Ka1 | 8×10-3 |
| Ka2 | 6×10-8 |
| Ka3 | 4×10-13 |
②计算H2PO
 +PO
+PO
 2HPO
2HPO 的平衡常数K=
的平衡常数K=
您最近半年使用:0次
3 . 下列有关电解质溶液的说法正确的是
A.室温下, 的 的 溶液与 溶液与 的 的 溶液等体积混合,溶液 溶液等体积混合,溶液 |
B.将 溶液从 溶液从 升温至 升温至 ,溶液中 ,溶液中 增大 增大 |
C.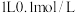 的 的 溶液和 溶液和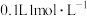 的 的 溶液中 溶液中 物质的量相同 物质的量相同 |
D.常温下 浓度相同的:① 浓度相同的:① 溶液② 溶液② 溶液③ 溶液③ 溶液,溶质物质的量浓度大小排序为:③>①>② 溶液,溶质物质的量浓度大小排序为:③>①>② |
您最近半年使用:0次
4 . 硫及其化合物在生产生活中具有广泛的应用,根据所学知识,回答下列问题:
(1) 溶液显
溶液显_______________ 性,判断的理由是_______________ (用离子方程式表示),若将该溶液蒸干,最终所得固体为_______________ (填化学式)。
(2) 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为_______________ 。
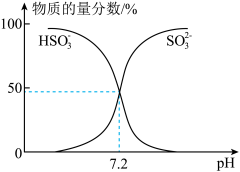
(3)常温下,在某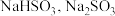 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数
_______________ 。
(4)常温下,某浓度的 溶液中:
溶液中:
① 为
为_______________ (填“强”或“弱”)电解质。
②往 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______________ ,此时所得溶液的
_______________ (填“变大”、“变小”或“不变”)。
(5)在 的
的 溶液中加入等体积
溶液中加入等体积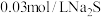 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中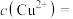
_______________ [已知: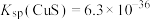 ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
(1)
 溶液显
溶液显(2)
 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为(3)常温下,在某
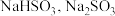 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数

(4)常温下,某浓度的
 溶液中:
溶液中:①
 为
为②往
 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
(5)在
 的
的 溶液中加入等体积
溶液中加入等体积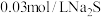 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中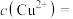
 ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
您最近半年使用:0次
名校
解题方法
5 . 苯甲酸钠(NaA)是一种常见的食品防离剂。已知苯甲酸(HA)的 Ka=10-4.2,常温时,下列关于 0.1 ml·L-1某甲酸钠水溶液的说法不正确的是
| A.NaA 溶液呈碱性 | B.溶液中存在;c(HA)+c(H+)=c(OH-) |
| C.微粒浓度大小:c(Na+)>c(A-)>c(OH-)>c(HA) | D.加水稀释时,溶液中 不变 不变 |
您最近半年使用:0次
6 . 根据表中数据判断,下列选项结论正确的是
| 酸 | H2C2O4 | HCN | H2CO3 |
| 电离常数(25℃) | K1=5.6×10-2 K1=1.5×10-4 | K=6.2×10-10 | K1=4.5×10-7 K2=4.4×10-11 |
| A.NaCN+H2O+CO2(少量)=HCN+Na2CO3 |
| B.0.1mol/L的Na2CO3溶液逐渐滴加到同浓度的HCN溶液中,无明显现象,说明无反应 |
C.浓度均为 的Na2CO3、NaHCO3、NaCN、 的Na2CO3、NaHCO3、NaCN、 溶液,pH最大的是Na2CO3 溶液,pH最大的是Na2CO3 |
D. 溶液呈酸性,溶液中离子浓度由大到小的顺序是 溶液呈酸性,溶液中离子浓度由大到小的顺序是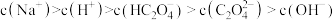 |
您最近半年使用:0次
名校
7 . 已知25℃时部分弱酸的电离平衡常数如下表所示:
(1) 溶液呈碱性的原因是
溶液呈碱性的原因是_____ (用离子方程式表示)。向NaCN溶液中通入少量的 时发生反应的离子方程式为
时发生反应的离子方程式为_____ 。
(2)等物质的量浓度的下列溶液: 由大到小排列顺序是
由大到小排列顺序是_____ (填选项)。
A. B.NaCN C.
B.NaCN C. D.
D.
(3)25℃时,pH=4的HCOOH溶液与pH=4的 溶液中由水电离出的
溶液中由水电离出的 之比为
之比为_____ 。
(4)25℃时,等物质的量浓度的HCN和NaCN的混合溶液,溶液中① 、②
、② 、③
、③ 、④
、④ 的物质的量浓度由大到小的顺序依次为
的物质的量浓度由大到小的顺序依次为_____ (填序号)。
(5)常温下,稀 溶液加水稀释过程中,下列数据变大的是_____。
溶液加水稀释过程中,下列数据变大的是_____。
(6)工业上常用, 溶液吸收
溶液吸收 ,当溶液的
,当溶液的 时,此时
时,此时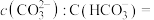
_____ 。
| 弱酸 |  |  |  |
 |  | 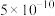 | 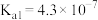 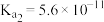 |
(1)
 溶液呈碱性的原因是
溶液呈碱性的原因是 时发生反应的离子方程式为
时发生反应的离子方程式为(2)等物质的量浓度的下列溶液:
 由大到小排列顺序是
由大到小排列顺序是A.
 B.NaCN C.
B.NaCN C. D.
D.
(3)25℃时,pH=4的HCOOH溶液与pH=4的
 溶液中由水电离出的
溶液中由水电离出的 之比为
之比为(4)25℃时,等物质的量浓度的HCN和NaCN的混合溶液,溶液中①
 、②
、② 、③
、③ 、④
、④ 的物质的量浓度由大到小的顺序依次为
的物质的量浓度由大到小的顺序依次为(5)常温下,稀
 溶液加水稀释过程中,下列数据变大的是_____。
溶液加水稀释过程中,下列数据变大的是_____。A. | B.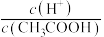 | C.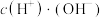 | D. |
(6)工业上常用,
 溶液吸收
溶液吸收 ,当溶液的
,当溶液的 时,此时
时,此时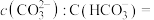
您最近半年使用:0次
名校
8 . 常温下,向0.1mol·L1H3PO4溶液中加入NaOH的过程中各微粒的物质的量分数(δ),随pH的变化关系如图所示(H3PO4的三级电离常数依次为Ka1、Ka2、Ka3)。下列叙述错误的是


A.Ka2=10-7.2,HPO 的水解平衡常数为10-6.8 的水解平衡常数为10-6.8 |
| B.为获得尽可能纯的NaH2PO4,pH应控制在4~5 |
C.反应H2PO +H2O +H2O H3PO4+OH- 的K=10-11.9 H3PO4+OH- 的K=10-11.9 |
D.Na2HPO4溶液中存在c(OH-)+c(PO )=c(H+)+c(H2PO )=c(H+)+c(H2PO )+c(H3PO4) )+c(H3PO4) |
您最近半年使用:0次
名校
9 . 盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多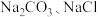 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为___________ (用离子方程式说明);已知 时,
时, 的
的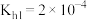 ,则当
,则当 溶液中
溶液中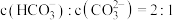 时,溶液的
时,溶液的
___________ 。
(2) 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液___________ (填“喷在叶片上”或“随水灌入土壤中”),主要理由是___________ 。
(3)已知:常温下,碳酸的电离平衡常数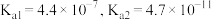 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加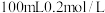 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
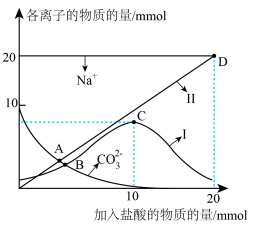
①曲线Ⅰ代表的离子是_______ 。
②A、B两点水的电离程度大小为A_______ B。
③根据上图,下列有关说法不正确的是_______ 。
a.滴加至 点时,
点时,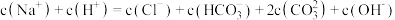
b.滴加至 点时,
点时,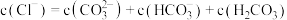
c.滴加至 点时,溶液
点时,溶液
④已知 电离平衡常数约为
电离平衡常数约为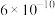 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱_______ 。
⑤证明 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是_______ 。
(1)盐碱地(含较多
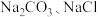 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为 时,
时, 的
的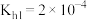 ,则当
,则当 溶液中
溶液中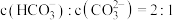 时,溶液的
时,溶液的
(2)
 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液(3)已知:常温下,碳酸的电离平衡常数
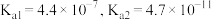 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加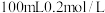 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至
 点时,
点时,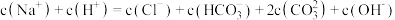
b.滴加至
 点时,
点时,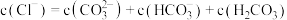
c.滴加至
 点时,溶液
点时,溶液
④已知
 电离平衡常数约为
电离平衡常数约为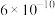 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱⑤证明
 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是
您最近半年使用:0次
2023-12-13更新
|
64次组卷
|
2卷引用:广东省佛山市H7教育共同体2023-2024学年高二上学期联考化学试题
10 . 25℃时,部分物质的电离平衡常数如下表所示:
(1)25℃时,物质的量浓度为 的氨水中,
的氨水中,
___________  (列出算式即可)。
(列出算式即可)。
(2)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法不正确 的是___________ (填字母序号)
a.开始反应时的速率:A<B b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A>B
(3)常温下, 溶液中离子浓度由大到小的顺序是
溶液中离子浓度由大到小的顺序是___________ 。
(4)25℃时,物质的量浓度相等的 溶液和NaClO溶液pH大小关系是:
溶液和NaClO溶液pH大小关系是:
___________ NaClO(填“>”“<”或“=”),请结合题目有关信息说明原因___________ 。
(5)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是___________ 。
(6)用蒸馏水稀释 的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。
的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。
| 化学式 |  |  | HClO |  |
| 电离平衡常数 |  |  , , |  |  |
 的氨水中,
的氨水中,
 (列出算式即可)。
(列出算式即可)。(2)25℃时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法
a.开始反应时的速率:A<B b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A>B
(3)常温下,
 溶液中离子浓度由大到小的顺序是
溶液中离子浓度由大到小的顺序是(4)25℃时,物质的量浓度相等的
 溶液和NaClO溶液pH大小关系是:
溶液和NaClO溶液pH大小关系是:
(5)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
(6)用蒸馏水稀释
 的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。
的醋酸,则下列各式表示的数值随水量的增加而增大的是_______。A.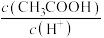 | B. | C.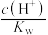 | D. |
您最近半年使用:0次



