23-24高二上·广东深圳·期末
名校
解题方法
1 . 回答下列问题
(1)某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
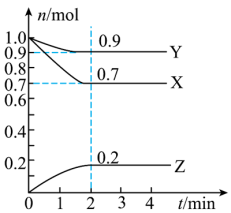
①反应从开始至2min,用Z的浓度变化表示的平均反应速率为v(Z)=___________ 。
②由图中所给数据进行分析,该反应的化学方程式为___________ 。
③下列措施能加快反应速率的有___________ 。
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.升高温度
(2)已知25℃时H3PO4的各级电离平衡常数如表所示:
①NaH2PO4水解反应的离子方程式为___________ ;其水解常数Kh=___________ (保留3位有效数字),NaH2PO4溶液呈___________ 性。(填“酸”、“碱”或“中”)
②计算H2PO +PO
+PO
 2HPO
2HPO 的平衡常数K=
的平衡常数K=___________ (保留2位有效数字)。
(1)某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。

①反应从开始至2min,用Z的浓度变化表示的平均反应速率为v(Z)=
②由图中所给数据进行分析,该反应的化学方程式为
③下列措施能加快反应速率的有
A.恒压时充入He B.恒容时充入He C.恒容时充入X D.升高温度
(2)已知25℃时H3PO4的各级电离平衡常数如表所示:
| 平衡常数 | H3PO4 |
| Ka1 | 8×10-3 |
| Ka2 | 6×10-8 |
| Ka3 | 4×10-13 |
②计算H2PO
 +PO
+PO
 2HPO
2HPO 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
2 . 根据表中数据判断,下列选项结论正确的是
| 酸 | H2C2O4 | HCN | H2CO3 |
| 电离常数(25℃) | K1=5.6×10-2 K1=1.5×10-4 | K=6.2×10-10 | K1=4.5×10-7 K2=4.4×10-11 |
| A.NaCN+H2O+CO2(少量)=HCN+Na2CO3 |
| B.0.1mol/L的Na2CO3溶液逐渐滴加到同浓度的HCN溶液中,无明显现象,说明无反应 |
C.浓度均为 的Na2CO3、NaHCO3、NaCN、 的Na2CO3、NaHCO3、NaCN、 溶液,pH最大的是Na2CO3 溶液,pH最大的是Na2CO3 |
D. 溶液呈酸性,溶液中离子浓度由大到小的顺序是 溶液呈酸性,溶液中离子浓度由大到小的顺序是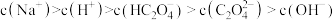 |
您最近一年使用:0次
3 . 某实验小组根据以下装置制备84消毒液,并探究84消毒液的性质。 ,若温度超过
,若温度超过 ,会生成
,会生成 杂质。
杂质。
回答下列问题:
I.84消毒液的制备
(1)仪器a的名称为___________ 。
(2)装置A中反应的离子方程式为___________ 。
(3)装置B的作用是___________ (任写一个即可)。
(4)制备 溶液时,为减少
溶液时,为减少 杂质的产生,应采取的措施是
杂质的产生,应采取的措施是___________ (写两条)。
(5)为探究 性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
Ⅱ.探究84消毒液的性质
84消毒液和医用酒精均为重要的消毒剂且二者不能混用,某小组对84消毒液与医用酒精的反应产物进行了探究。
【提出假设】医用酒精中的 被氧化为
被氧化为
【实验方案】实验方案及现象如下:
【实验结论1】
(6)产物中有乙醛,且乙醛会被转化为其它物质。补充①的实验现象:___________ 。
【查阅资料】混合体系中可能发生以下反应:

 (卤化反应)
(卤化反应)
【实验设计】取2份 84消毒液,缓慢滴加医用酒精或蒸馏水各
84消毒液,缓慢滴加医用酒精或蒸馏水各 ,通过测定过程中
,通过测定过程中 变化判断是否发生卤化反应(忽略过程中的热效应对
变化判断是否发生卤化反应(忽略过程中的热效应对 的影响)。实验结果如图。
的影响)。实验结果如图。 增大,说明乙醛发生了卤化反应。
增大,说明乙醛发生了卤化反应。
【查阅资料】某同学查阅资料后认为结论2不严谨,原因是工业上为了稳定 ,在84消毒液中添加了少量
,在84消毒液中添加了少量 ,且由于乙醇的“锁水”效应也会使
,且由于乙醇的“锁水”效应也会使 增大(提示:乙醇与
增大(提示:乙醇与 不反应)。
不反应)。
【数据分析】②已知上述实验:84消毒液中 。
。
(7)通过计算证明84消毒液中添加了少量 ,写出计算过程
,写出计算过程___________ 。
【优化实验】③该同学增加了对照实验,证明反应生成了 。
。
(8)请简述方案和结果:___________ 。
实验总结:医用酒精中的乙醇能被84消毒液氧化为乙醛,乙醛能进一步发生卤化反应。

 ,若温度超过
,若温度超过 ,会生成
,会生成 杂质。
杂质。回答下列问题:
I.84消毒液的制备
(1)仪器a的名称为
(2)装置A中反应的离子方程式为
(3)装置B的作用是
(4)制备
 溶液时,为减少
溶液时,为减少 杂质的产生,应采取的措施是
杂质的产生,应采取的措施是(5)为探究
 性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
性质,设计如图所示装置,在A处通入未经干燥的氯气。当关闭K处弹簧夹时,C处红布条看不到明显现象;当打开K处的弹簧夹后,C处红布条逐渐褪色。则B瓶内液体可能是___________。
A.饱和 溶液 溶液 | B. 溶液 溶液 | C. | D.浓硫酸 |
Ⅱ.探究84消毒液的性质
84消毒液和医用酒精均为重要的消毒剂且二者不能混用,某小组对84消毒液与医用酒精的反应产物进行了探究。
【提出假设】医用酒精中的
 被氧化为
被氧化为
【实验方案】实验方案及现象如下:
| 实验操作 | 取样检测时间点 | 实验现象 |
常温下将 医用酒精和 医用酒精和 84消毒液混合,在不同反应时间点,分别取 84消毒液混合,在不同反应时间点,分别取 反应后的溶液滴加到新制氢氧化铜悬浊液中加热 反应后的溶液滴加到新制氢氧化铜悬浊液中加热 |  | ① |
 | 橙黄色沉淀 | |
 | 黑色沉淀 |
(6)产物中有乙醛,且乙醛会被转化为其它物质。补充①的实验现象:
【查阅资料】混合体系中可能发生以下反应:

 (卤化反应)
(卤化反应)【实验设计】取2份
 84消毒液,缓慢滴加医用酒精或蒸馏水各
84消毒液,缓慢滴加医用酒精或蒸馏水各 ,通过测定过程中
,通过测定过程中 变化判断是否发生卤化反应(忽略过程中的热效应对
变化判断是否发生卤化反应(忽略过程中的热效应对 的影响)。实验结果如图。
的影响)。实验结果如图。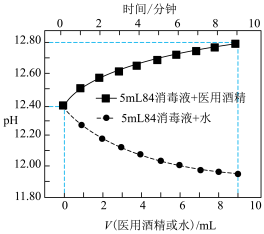
 增大,说明乙醛发生了卤化反应。
增大,说明乙醛发生了卤化反应。【查阅资料】某同学查阅资料后认为结论2不严谨,原因是工业上为了稳定
 ,在84消毒液中添加了少量
,在84消毒液中添加了少量 ,且由于乙醇的“锁水”效应也会使
,且由于乙醇的“锁水”效应也会使 增大(提示:乙醇与
增大(提示:乙醇与 不反应)。
不反应)。【数据分析】②已知上述实验:84消毒液中
 。
。(7)通过计算证明84消毒液中添加了少量
 ,写出计算过程
,写出计算过程【优化实验】③该同学增加了对照实验,证明反应生成了
 。
。(8)请简述方案和结果:
实验总结:医用酒精中的乙醇能被84消毒液氧化为乙醛,乙醛能进一步发生卤化反应。
您最近一年使用:0次
解题方法
4 . 常温下,用NaOH溶液滴定NaH2PO4溶液,溶液pH与 的关系如图所示。下列关系正确的是
的关系如图所示。下列关系正确的是
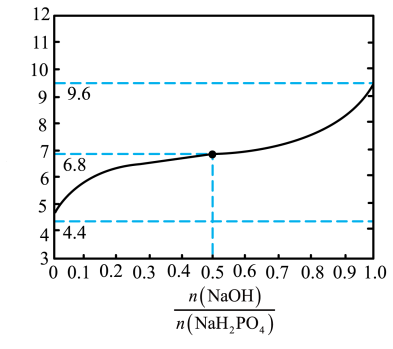
 的关系如图所示。下列关系正确的是
的关系如图所示。下列关系正确的是
A.常温下, |
B.当 =0.5时,水的电离程度最大 =0.5时,水的电离程度最大 |
C.向0.1mol/L的NaH2PO4溶液中滴加NaOH溶液至中性: |
D.0.1mol/LNaH2PO4溶液与0.1mol/LNa3PO4溶液等体积混合:  |
您最近一年使用:0次
解题方法
5 . 25℃时,将0.01mol•L-1的盐酸逐滴加到10mL0.01mol•L-1NaA溶液中,A-、HA物质的量所占分数(δ)、pH变化曲线如甲、乙图所示。下列溶液中微粒的物质的量浓度关系正确的是


| A.溶液显中性时:c(Cl-)=c(HA) |
| B.图甲中a点对应的溶液:c(A-)<c(Cl-) |
| C.图乙中b点对应的溶液:c(Cl-)>c(HA) >c(A-)>c(OH-)>c(H+) |
| D.a点对应的pH=9.5,则常温下,HA的电离平衡常数:Ka(HA)=10-4.5 |
您最近一年使用:0次
名校
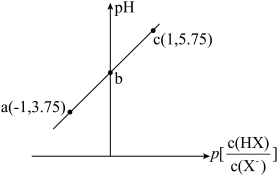
6 . 已知: 。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随
。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
变化关系如图所示。下列说法错误的是
 。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随
。室温下,向0.10mol/LHX溶液中滴加0.10mol/LNaOH溶液,溶液pH随 变化关系如图所示。下列说法错误的是
变化关系如图所示。下列说法错误的是
| A.溶液中水的电离程度:a<b<c |
B.b点溶液中: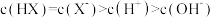 |
C.c点溶液中: |
D.室温下NaX的水解平衡常数为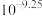 |
您最近一年使用:0次
解题方法
7 . 25℃时,向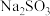 溶液中滴入盐酸,混合溶液的
溶液中滴入盐酸,混合溶液的 与离子浓度变化的关系如图所示。下列叙述错误的是
与离子浓度变化的关系如图所示。下列叙述错误的是
已知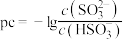 或
或 。
。
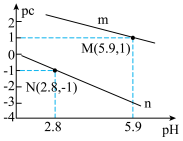
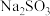 溶液中滴入盐酸,混合溶液的
溶液中滴入盐酸,混合溶液的 与离子浓度变化的关系如图所示。下列叙述错误的是
与离子浓度变化的关系如图所示。下列叙述错误的是已知
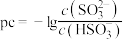 或
或 。
。
A.曲线 表示 表示 与 与 的变化关系 的变化关系 |
B.当溶液呈中性时, |
C.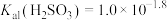 |
D.25℃时, 的平衡常数为 的平衡常数为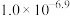 |
您最近一年使用:0次
解题方法
8 . 某化学研究学习小组对高二所学部分内容作了归纳总结(均指常温下),现摘录6条,其中错误的有
①物质的量的浓度相同的2种盐,若pH:NaX>NaY,则HX>HY
②已知CH3COOH电离平衡常数为Ka,CH3COO-水解常数为Kh,水的离子积为KW,则三者关系为:Ka·Kh = KW
③pH=7的NH3·H2O与NH4Cl的混合溶液中:c(Cl-) = c( )
)
④0.1 mol·L-1的硫酸铵溶液中:c( )>c(
)>c( )>c(H+)
)>c(H+)
⑤冰晶胞中水分子的空间排列方式与干冰晶胞类似
⑥1mol [Cu(NH3)4]2+中含有σ键的数目为12NA
①物质的量的浓度相同的2种盐,若pH:NaX>NaY,则HX>HY
②已知CH3COOH电离平衡常数为Ka,CH3COO-水解常数为Kh,水的离子积为KW,则三者关系为:Ka·Kh = KW
③pH=7的NH3·H2O与NH4Cl的混合溶液中:c(Cl-) = c(
 )
)④0.1 mol·L-1的硫酸铵溶液中:c(
 )>c(
)>c( )>c(H+)
)>c(H+)⑤冰晶胞中水分子的空间排列方式与干冰晶胞类似
⑥1mol [Cu(NH3)4]2+中含有σ键的数目为12NA
| A.①⑤⑥ | B.①③⑤ | C.②④⑥ | D.③④⑥ |
您最近一年使用:0次
名校
9 . 常温下,体积和浓度一定的 溶液中各微粒浓度的负对数(
溶液中各微粒浓度的负对数(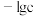 )随溶液pH的变化关系如图所示。下列叙述正确的是
)随溶液pH的变化关系如图所示。下列叙述正确的是
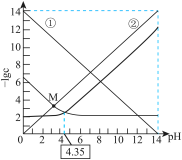
A.曲线②表示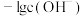 随溶液pH的变化情况 随溶液pH的变化情况 |
B.等物质的量浓度 和 和 混合溶液: 混合溶液: |
C. 的 的 的数量级为 的数量级为 |
D.常温下,将M点对应溶液加水稀释,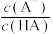 不变 不变 |
您最近一年使用:0次
2023-04-01更新
|
775次组卷
|
6卷引用:广东省六校2024届高三第一次联考化学试题
解题方法
10 . 以酚酞为指示剂,用 溶液滴定
溶液滴定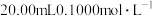 一元酸
一元酸 的溶液。溶液中,
的溶液。溶液中, 、分布系数(
、分布系数( ,比如
,比如 的分布系数:
的分布系数: )随
)随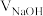 的变化关系如图所示,下列叙述不正确的是
的变化关系如图所示,下列叙述不正确的是
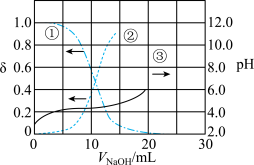
 溶液滴定
溶液滴定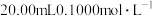 一元酸
一元酸 的溶液。溶液中,
的溶液。溶液中, 、分布系数(
、分布系数( ,比如
,比如 的分布系数:
的分布系数: )随
)随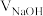 的变化关系如图所示,下列叙述不正确的是
的变化关系如图所示,下列叙述不正确的是
A.曲线①代表 ,曲线②代表 ,曲线②代表 |
B. 的数量级为 的数量级为 |
C.滴定过程中,溶液中 不断减小 不断减小 |
D.滴定终点时,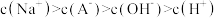 |
您最近一年使用:0次
2023-03-16更新
|
2058次组卷
|
4卷引用:广东省广州市2023届高三一模考试化学试题
广东省广州市2023届高三一模考试化学试题(已下线)专题16 水溶液中的离子平衡(已下线)广东省广州市天河区2023届高三二模化学试题变式题(选择题11-16)广东省广州市2022-2023学年高三普通高中毕业班综合测试(一)化学试题



