名校
1 . 已知:常温下, 溶液的电离平衡常数
溶液的电离平衡常数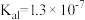 ,
,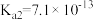 ,
, 、
、 的
的 分别为
分别为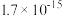 、
、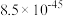 ,
,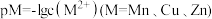 ,
, ,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线
,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线 表示
表示 。下列说法错误的是
。下列说法错误的是
 溶液的电离平衡常数
溶液的电离平衡常数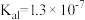 ,
,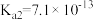 ,
, 、
、 的
的 分别为
分别为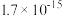 、
、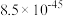 ,
,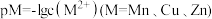 ,
, ,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线
,三种硫化物的沉淀溶解平衡曲线如图所示,其中曲线 表示
表示 。下列说法错误的是
。下列说法错误的是
A.曲线 表示 表示 |
B.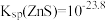 |
C.将浓度均为 的 的 溶液和 溶液和 溶液等体积混合,有沉淀产生 溶液等体积混合,有沉淀产生 |
D.含 和 和 的悬浊液中: 的悬浊液中: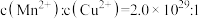 |
您最近一年使用:0次
2020-12-18更新
|
1603次组卷
|
4卷引用:湖南省长沙市长郡中学2021届高三上学期第5次月考化学试题
湖南省长沙市长郡中学2021届高三上学期第5次月考化学试题(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)难点6 水溶液中的四大平衡常数-2021年高考化学专练【热点·重点·难点】福建省莆田市2021届高三毕业班第一次教学质量检测化学试卷
2020高三·全国·专题练习
解题方法
2 . 按要求完成下列填空。
(1)(溶解度与Ksp的换算)已知某温度时Ksp(CaCO3)=1×10-10,则该温度下,CaCO3的溶解度约为________ 。
(2)(平衡常数与Ksp的关系)在1.0 L Na2CO3溶液中溶解0.01 mol BaSO4,计算Na2CO3溶液的最初浓度不得低于________ mol·L-1(忽略溶液体积变化)[已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaCO3)=5.1×10-9]。
(3)(Ksp与Ka的计算关系)汽车尾气中的SO2可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液的pH为9,忽略SO 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=________ (保留3位有效数字)[已知:Ka1(H2SO3)=1.54×10-2,Ka2(H2SO3)=1.02×10-7]。
(1)(溶解度与Ksp的换算)已知某温度时Ksp(CaCO3)=1×10-10,则该温度下,CaCO3的溶解度约为
(2)(平衡常数与Ksp的关系)在1.0 L Na2CO3溶液中溶解0.01 mol BaSO4,计算Na2CO3溶液的最初浓度不得低于
(3)(Ksp与Ka的计算关系)汽车尾气中的SO2可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液的pH为9,忽略SO
 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=
您最近一年使用:0次
名校
3 . 25℃时,AgCl的Ksp=1.8×10-10,Ag2CO3在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是


| A.Ag2CO3的Ksp为8.1×10-12 |
B.Ag2CO3(s)+2Cl-(aq) 2AgCl(s)+ 2AgCl(s)+ (aq)的平衡常数K=2.5×108 (aq)的平衡常数K=2.5×108 |
| C.加入适量K2CO3(s),可使溶液由Y点变到Z点 |
D.向同浓度的KCl和K2CO3的混合溶液中滴入0.001mol·L-1AgNO3溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
2020-11-10更新
|
567次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2021-2022学年高二上学期第三次月考化学试题
名校
解题方法
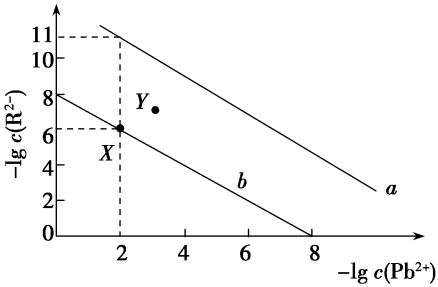
4 . 25 ℃时,PbR(R2-为SO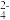 或CO
或CO )的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法不正确的是( )
)的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法不正确的是( )
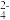 或CO
或CO )的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法不正确的是( )
)的沉淀溶解平衡关系图如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法不正确的是( )
| A.线a表示PbCO3 |
| B.Y点溶液是PbCO3 的过饱和溶液 |
C.当PbSO4和PbCO3沉淀共存时,溶液中c(SO )和c(CO )和c(CO )的比是1×105 )的比是1×105 |
| D.向X点对应的饱和溶液中加入少量Pb(NO3)2,可转化为Y点对应的溶液 |
您最近一年使用:0次
2020-10-21更新
|
1000次组卷
|
10卷引用:选择性必修1(SJ)专题3第四单元 沉淀溶解平衡
选择性必修1(SJ)专题3第四单元 沉淀溶解平衡课选择性必修1 专题3 第四单元 课时2 Ksp相关计算及其图像分析辽宁省沈阳市重点高中联合体2021-2022学年高二12月考试化学试题内蒙古赤峰二中2021届高三上学期第二次月考化学试题黑龙江省肇东市第四中学校2020-2021学年高二上学期期中考试化学试题(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析3.4.2沉淀溶解平衡原理的应用 课后3.4.1沉淀溶解平衡原理 课后(已下线)第5讲 难溶电解质的溶解平衡
解题方法
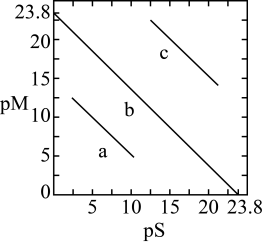
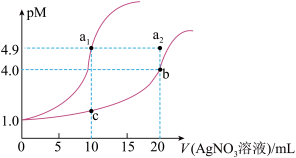
5 . 某温度下,向10 mL 0.1 mol·L-1 NaCl溶液和10 mL 0.1 mol·L-1 K2CrO4溶液中分别滴加0.1 mol·L-1 AgNO3溶液。滴加过程中pM[pM=-lgM,M为c(Cl-)或c(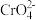 )]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为深红色沉淀,100.1≈1.259,
)]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为深红色沉淀,100.1≈1.259,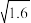 ≈1.265。下列说法错误的是( )
≈1.265。下列说法错误的是( )
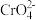 )]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为深红色沉淀,100.1≈1.259,
)]与所加AgNO3溶液体积之间的关系如图所示。已知Ag2CrO4为深红色沉淀,100.1≈1.259,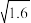 ≈1.265。下列说法错误的是( )
≈1.265。下列说法错误的是( )
| A.a1、b、c三点所示溶液中c(Ag+):b>c>a1 |
| B.若将上述NaCl溶液的浓度改为0.2 mol·L-1,则a1点会平移至a2点 |
| C.若将a1与b点溶液混合,则有AgCl与Ag2CrO4固体析出 |
| D.用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂 |
您最近一年使用:0次
名校
解题方法
6 . 已知:25℃时,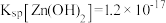 ,
, 。该温度下,下列说法错误的是
。该温度下,下列说法错误的是
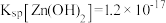 ,
, 。该温度下,下列说法错误的是
。该温度下,下列说法错误的是A. 的水解常数为 的水解常数为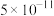 |
B. 溶于水形成的饱和溶液中, 溶于水形成的饱和溶液中,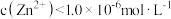 |
C.向 悬浊液中加入 悬浊液中加入 ,溶液中 ,溶液中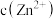 增大 增大 |
D.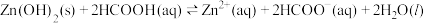 的平衡常数 的平衡常数 |
您最近一年使用:0次
2020-10-13更新
|
736次组卷
|
4卷引用:选择性必修1(SJ)专题3专题综合检测
7 . 常温时,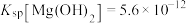 ,
, ,
, ,
,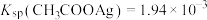 ,下列叙述不正确的是
,下列叙述不正确的是
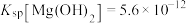 ,
, ,
, ,
,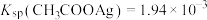 ,下列叙述不正确的是
,下列叙述不正确的是A.浓度均为 的 的 溶液和 溶液和 溶液等体积混合一定产生 溶液等体积混合一定产生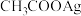 沉淀 沉淀 |
B.将 的 的 溶液滴入浓度均为 溶液滴入浓度均为 的 的 和 和 的混合溶液中,先产生 的混合溶液中,先产生 沉淀 沉淀 |
C.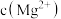 为 为 的溶液要产生 的溶液要产生 沉淀,溶液的pH应控制在8.5以上 沉淀,溶液的pH应控制在8.5以上 |
D.在其他条件不变的情况下,向饱和 溶液中加入 溶液中加入 溶液, 溶液,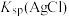 不变 不变 |
您最近一年使用:0次
2020-10-13更新
|
311次组卷
|
2卷引用:选择性必修1(SJ)专题3易错疑难集训(二)
名校
解题方法
8 . 氢氧化铈是黄色难溶于水、可溶于酸的常用化学试剂。以氟碳铈矿(主要成分为CeFCO3)为原料提取氢氧化铈的工艺流程如图所示:
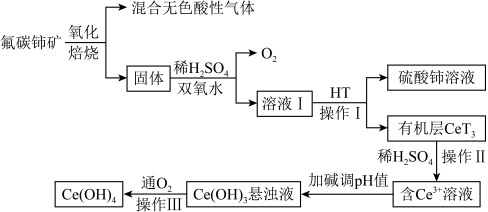
请回答下列问题:
(1)CeFCO3中Ce的化合价为____ 。“酸浸”时,为提高矿石的浸出率,下列措施可采取的是___ (填标号)。
A.提高浸出温度 B.延长浸出时间 C.用98%的硫酸
(2)氧化焙烧发生的反应方程式为__________ 。
(3)H2O2的作用是__________ 。
(4)HT是一种难溶于水的有机溶剂,它能将Ce3+从水溶液中萃取出来,该过程可表示为Ce3+(水层)+3HT(有机层) CeT3(有机层)+3H+(水层)。操作I的名称是
CeT3(有机层)+3H+(水层)。操作I的名称是________ ,操作III的步骤是_______ 。
(5)从平衡的角度解释加碱调pH值生成Ce(OH)3悬浊液的原因________ 。

请回答下列问题:
(1)CeFCO3中Ce的化合价为
A.提高浸出温度 B.延长浸出时间 C.用98%的硫酸
(2)氧化焙烧发生的反应方程式为
(3)H2O2的作用是
(4)HT是一种难溶于水的有机溶剂,它能将Ce3+从水溶液中萃取出来,该过程可表示为Ce3+(水层)+3HT(有机层)
 CeT3(有机层)+3H+(水层)。操作I的名称是
CeT3(有机层)+3H+(水层)。操作I的名称是(5)从平衡的角度解释加碱调pH值生成Ce(OH)3悬浊液的原因
您最近一年使用:0次
2020-09-25更新
|
247次组卷
|
3卷引用:山东省济南市历城第二中学2022届高三上学期开学考试化学试卷(A)
山东省济南市历城第二中学2022届高三上学期开学考试化学试卷(A)北京市清华大学附属中学中学生标准学术能力基础性测试2021届高三9月测试化学试题(已下线)北京市清华大学附属中学2021届高三上学期9月月考化学试题
9 . 已知: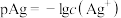 ,
,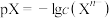 。
。 时,几种物质的
时,几种物质的 的值如下表:
的值如下表:
 、
、 、
、 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
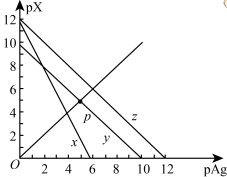
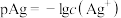 ,
,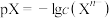 。
。 时,几种物质的
时,几种物质的 的值如下表:
的值如下表:| 化学式 |  |  |  |
| 颜色 | 白 | 浅黄 | 红 |
 |  |  |  |
 、
、 、
、 的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
的饱和溶液中,阳离子和阴离子的浓度关系如图所示。下列说法正确的是
A.图中x代表 曲线,z代表 曲线,z代表 曲线 曲线 |
B.298K时,在 和 和 的物质的量浓度均为 的物质的量浓度均为 的溶液中,滴入少量 的溶液中,滴入少量 的 的 溶液,首先产生的是红色沉淀 溶液,首先产生的是红色沉淀 |
| C.298K时,若增大p点的阴离子浓度,则y上的点沿曲线向上移动 |
D.298K时, 的平衡常数 的平衡常数 |
您最近一年使用:0次
2020-09-13更新
|
1245次组卷
|
20卷引用:选择性必修1 专题3 第四单元综合训练
选择性必修1 专题3 第四单元综合训练(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)重庆市第一中学2020届高三10月月考理综化学试题贵州省铜仁市第一中学2020届高三上学期第三次月考化学试题黑龙江省哈尔滨市第六中学2020届高三上学期第三次调研考试化学试题2019年秋高三化学复习强化练习—— 难溶电解质的沉淀溶解平衡2020届高三《新题速递·化学》12月第01期(考点07-11)2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编内蒙古赤峰市赤峰二中2019-2020学年高二下学期第一次月考化学试题陕西省西安中学2020届高三第六次模拟考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节综合训练高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节综合训练(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)陕西省汉中市部分高中2020-2021学年高二上学期12月月考化学试题福建省莆田二中2020-2021学年高三上学期期中检测化学试题陕西省西安市长安区第一中学2021-2022学年高二下学期期中考试化学试题陕西省西安中学2022届高三下学期五月全仿真模拟考试(一)理综化学试题吉林省通化市辉南县第六中学2022-2023学年高二上学期第一次月考化学试题广西 南宁市第三中学2021-2022学年高二下学期期中考试化学试题
10 . 常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L 悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌。加入Na2CO3固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是


| A.常温下,Ksp(BaSO4)=2.5×10-9 |
| B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
| C.若要使BaSO4全部转化为BaCO3至少要加入0.65mol Na2CO3 |
D.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小关系为:c( )>c( )>c( )>c(Ba2+)>c(OH-) )>c(Ba2+)>c(OH-) |
您最近一年使用:0次
2020-06-23更新
|
1077次组卷
|
3卷引用:专题八 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)
(已下线)专题八 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)内蒙古包头市2020届高三普通高等学校招生全国统一考试(第二次模拟考试)理科综合化学试题内蒙古赤峰二中2020-2021学年高二上学期第二次月考化学试题



