名校
解题方法
1 . I.根据下列图象,进行分析:
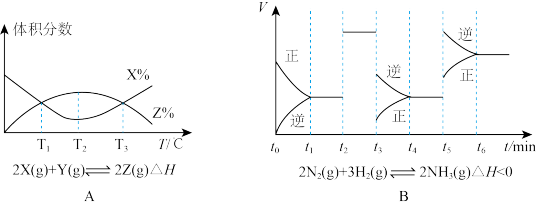
(1)由图A知,该反应的K值随温度的升高而_____ (填“增大”、“减小”或“不变”)。
(2)由图B知,t3时采取的措施为_____ ,t1~t6中,氨气的含量最低的是_____ 。
II.已知H2A在水中电离:H2A=HA-+H+,HA- A2-+H+。
A2-+H+。
(1)常温下NaHA溶液的pH__ (填序号)。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/LKOH溶液至溶液呈中性(稀溶液体积可以加和),此时该混合溶液中的下列关系一定正确的是______ 。
A.c(H+)·c(OH-)=1×10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq)∆H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq)∆H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有______ 。
A.升高温度 B.加入Na2A固体 C.加入NH4Cl晶体

(1)由图A知,该反应的K值随温度的升高而
(2)由图B知,t3时采取的措施为
II.已知H2A在水中电离:H2A=HA-+H+,HA-
 A2-+H+。
A2-+H+。(1)常温下NaHA溶液的pH
A.大于7 B.小于7 C.等于7 D.无法确定
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/LKOH溶液至溶液呈中性(稀溶液体积可以加和),此时该混合溶液中的下列关系一定正确的是
A.c(H+)·c(OH-)=1×10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)
 Ca2+(aq)+A2-(aq)∆H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq)∆H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有A.升高温度 B.加入Na2A固体 C.加入NH4Cl晶体
您最近一年使用:0次
名校
解题方法
2 . 国家规定,排放的废水中氟的含量不得超过10.0mg/L,砷的含量不得超过0.5mg/L。硫酸工厂废水中除含有稀硫酸外,还含有H3AsO3、H2SiF6等物质。工业上常通过化学沉淀和氧化、吸附沉降处理废水,实现水体达标排放。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO4)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:___________ 。
②充分沉淀后测得废水中F的含量为9.5mg/L,此时 的浓度为
的浓度为___________ 。[已知:Ksp(CaSO4)=5.0×10-5、Ksp(CaF2)=5.0×10-9]
(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(II)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电你越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。
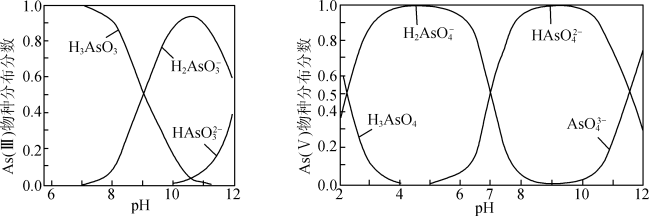
①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:___________ 。
②其它条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO4溶液。
方式I:先加NaClO溶液,再加FeSO4溶液;
方式II:先加FeSO4溶液,再加NaClO溶液。
反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是___________ 。
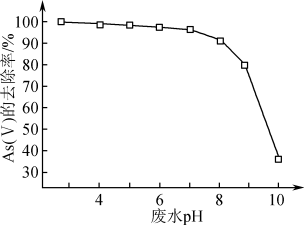
③废水的pH对As(V)的去除率的影响如图所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是___________ 。
(1)化学沉淀:向废水中加入石灰乳[以Ca(OH)2为主过滤。滤渣中主要含有CaSO4、CaF2、SiO2和少量Ca3(AsO4)2。
①写出该过程中H2SiF6和石灰乳反应生成CaF2、SiO2的化学方程式:
②充分沉淀后测得废水中F的含量为9.5mg/L,此时
 的浓度为
的浓度为(2)氧化、吸附沉降:利用NaClO和FeSO4进一步处理废水中残余的As(III)。
已知:i.NaClO能将As(II)氧化为As(V)、Fe(II)氧化为Fe(III)。形成的Fe(OH)3胶体吸附废水中的As(V)物种而沉降。
ii.溶液的pH对Fe(OH)3胶体表面所带电荷有影响。pH>7时,Fe(OH)3胶体表面带负电荷,pH越高,表面所带负电你越多。
iii.As(III)和As(V)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①向化学沉淀后的废水(pH≈8)中加入NaClO溶液,写出As(III)发生主要反应的离子方程式:
②其它条件相同的情况下,用以下两种方式向废水样中添加NaClO和FeSO4溶液。
方式I:先加NaClO溶液,再加FeSO4溶液;
方式II:先加FeSO4溶液,再加NaClO溶液。
反应相同时间,测得As(III)的氧化效果方式II不如方式I,原因是
③废水的pH对As(V)的去除率的影响如图所示。pH>8时,随着废水的pH增大,As(V)的去除率发生如图所示变化的原因是

您最近一年使用:0次
2021-05-29更新
|
451次组卷
|
2卷引用:江苏省苏州市姑苏区苏州中学2020-2021学年高二下学期期中考试化学试题
解题方法
3 . 大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO 浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO
浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO (aq)+H2O(aq)
(aq)+H2O(aq)  2HCO
2HCO (aq),下列说法不正确的是
(aq),下列说法不正确的是
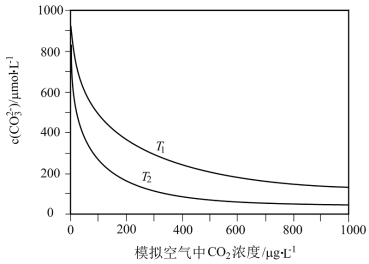
 浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO
浓度与模拟空气中CO2浓度的关系曲线。已知:海水中存在以下平衡:CO2(aq)+CO (aq)+H2O(aq)
(aq)+H2O(aq)  2HCO
2HCO (aq),下列说法不正确的是
(aq),下列说法不正确的是
| A.T1>T2 |
B.海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,CO 浓度降低 浓度降低 |
C.当大气中CO2浓度确定时,海水温度越高,CO 浓度越低 浓度越低 |
| D.大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
您最近一年使用:0次
2021-03-13更新
|
409次组卷
|
6卷引用:解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练
(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)浙江省绍兴市柯桥区2020届高三上学期1月模拟普通高校招生考试化学试题浙江省绍兴市柯桥区2021-2022 学年高三下学期选考科目6月适应性考试化学试题安徽省蚌埠四校2021-2022学年高三下学期三模化学试题(已下线)第5讲 难溶电解质的溶解平衡
解题方法
4 . 海洋是一个十分巨大的资源宝库,海水中含量最多的是H、O两种元素,还含有Na、Cl、Mg、Br、Ca、S等元素。海水资源的利用主要包括海水淡化、海水晒盐,从海水中制取镁、钾、溴等化工产品。从海水中提取镁的步骤是将石灰乳加入海水沉淀池中,得到氢氧化镁沉淀,再将氢氧化镁与盐酸反应,得到的溶液蒸发结晶,获得六水合氯化镁晶体(MgCl2•6H2O)进一步操作得到无水氯化镁,电解熔融氯化镁可获得单质镁。海水淡化是解决淡水资源短缺的有效途径之一,其方法主要有蒸馏法、电渗析法和离子交换法等。下列有关海水提镁的说法正确的是
| A.得到Mg(OH)2沉淀的化学反应方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl |
B.加入盐酸,Mg(OH)2(s) Mg2+(aq)+2OH-(aq)平衡正向移动 Mg2+(aq)+2OH-(aq)平衡正向移动 |
| C.在空气中加热灼烧MgCl2•6H2O可得到无水氯化镁 |
| D.电解熔融氯化镁时金属镁在阳极析出 |
您最近一年使用:0次
2021-02-24更新
|
413次组卷
|
2卷引用:江苏省六市(南通、淮安、泰州、徐州、镇江、宿迁)2021届高三一模化学试卷
解题方法
5 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的沉淀溶解平衡均属于化学平衡。
I.已知 在水中存在以下平衡:
在水中存在以下平衡: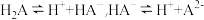 。
。
(1)常温下, 溶液的
溶液的
______ (填字母序号),原因是______ (填离子方程式)。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向 的
的 溶液中逐滴滴加
溶液中逐滴滴加
 溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是______ (填字母序号)。
A.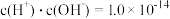 B.
B.
C.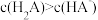 D.
D.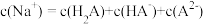
(3)常温下, 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: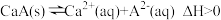 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有______ (填字母序号)。
A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入 固体
固体
Ⅱ.化学沉淀法是除去酸性废水中 的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液
的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液 变化的关系如图所示。向含
变化的关系如图所示。向含 的溶液中逐滴滴加
的溶液中逐滴滴加 溶液,溶液变浑浊,继续滴加
溶液,溶液变浑浊,继续滴加 溶液又变澄清。
溶液又变澄清。
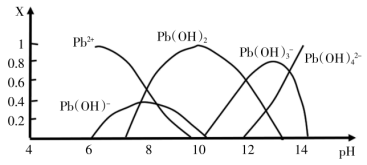
(4)若采用氢氧化物沉淀法除溶液中的 ,应将溶液的
,应将溶液的 调至约为
调至约为______ ; 时,溶液中发生的主要离子方程式为
时,溶液中发生的主要离子方程式为______ 。
(5)向酸性含铅废水中加 可将
可将 转化为
转化为 沉淀除去。若某工厂处理过的废水中
沉淀除去。若某工厂处理过的废水中 浓度为
浓度为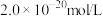 ,则
,则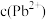 为
为______ 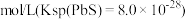 。
。
I.已知
 在水中存在以下平衡:
在水中存在以下平衡: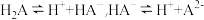 。
。(1)常温下,
 溶液的
溶液的
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向
 的
的 溶液中逐滴滴加
溶液中逐滴滴加
 溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是A.
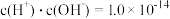 B.
B.
C.
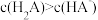 D.
D.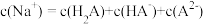
(3)常温下,
 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: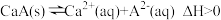 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入
 固体
固体Ⅱ.化学沉淀法是除去酸性废水中
 的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液
的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液 变化的关系如图所示。向含
变化的关系如图所示。向含 的溶液中逐滴滴加
的溶液中逐滴滴加 溶液,溶液变浑浊,继续滴加
溶液,溶液变浑浊,继续滴加 溶液又变澄清。
溶液又变澄清。
(4)若采用氢氧化物沉淀法除溶液中的
 ,应将溶液的
,应将溶液的 调至约为
调至约为 时,溶液中发生的主要离子方程式为
时,溶液中发生的主要离子方程式为(5)向酸性含铅废水中加
 可将
可将 转化为
转化为 沉淀除去。若某工厂处理过的废水中
沉淀除去。若某工厂处理过的废水中 浓度为
浓度为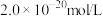 ,则
,则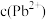 为
为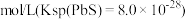 。
。
您最近一年使用:0次
2021-01-30更新
|
398次组卷
|
2卷引用:湖南省怀化市2020-2021学年高二上学期期末考试化学试题
名校
解题方法
6 . I 、H2A在水中存在以下平衡:H2A  H+ +HA- ,HA-
H+ +HA- ,HA- H+ +A2-
H+ +A2-
(1)NaHA溶液显酸性,则溶液中离子浓度的大小顺序为__________ 。
(2)常温时,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性。此时该混合溶液的下列关系中,一定正确的是__________ 。
A.c(Na+ )>c(K+ ) B. c(H +)•c(OH )=1×10-14
C. c(Na+ )=c(K+ ) D. c(Na+ )+c(K+ )=c(HA- )+c(A2-)
Ⅱ、含有Cr2O 的废水毒性较大,某工厂废水中含4.00×10-3 mol/L Cr2O
的废水毒性较大,某工厂废水中含4.00×10-3 mol/L Cr2O 。为使废水能达标排放,作如下处理:
。为使废水能达标排放,作如下处理:
Cr2O
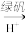 Cr3+、Fe3+
Cr3+、Fe3+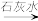 Cr(O3)、Fe(OH)3
Cr(O3)、Fe(OH)3
(3)该废水中加入FeSO4•7H2O和稀硫酸,发生反应的离子方程式为:________________ 。
(4)欲使25 L该废水中 转化为Cr3+,理论上需要加入
转化为Cr3+,理论上需要加入_________ g FeSO4•7H2O。
(5)若处理后的废水中残留的 c(Fe3+)=1×10-13mol/L ,则残留的 Cr3+ 的浓度为_________ mol/L ,Cr3+________ (填是或否)沉淀完全。(已知:Ksp[Fe(OH)3]≈1.0×10-38mol/L ,Ksp[Cr(OH)3]≈1.0×10-31 mol/L )
III. 已知:I2+2S2O32-==2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
(6)步骤c中判断恰好反应完全的现象为_______________
(7)根据以上实验和包装袋说明,所测精制盐的碘含量是_____ g/kg。(以含w的代数式表示)
 H+ +HA- ,HA-
H+ +HA- ,HA- H+ +A2-
H+ +A2-(1)NaHA溶液显酸性,则溶液中离子浓度的大小顺序为
(2)常温时,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性。此时该混合溶液的下列关系中,一定正确的是
A.c(Na+ )>c(K+ ) B. c(H +)•c(OH )=1×10-14
C. c(Na+ )=c(K+ ) D. c(Na+ )+c(K+ )=c(HA- )+c(A2-)
Ⅱ、含有Cr2O
 的废水毒性较大,某工厂废水中含4.00×10-3 mol/L Cr2O
的废水毒性较大,某工厂废水中含4.00×10-3 mol/L Cr2O 。为使废水能达标排放,作如下处理:
。为使废水能达标排放,作如下处理:Cr2O

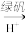 Cr3+、Fe3+
Cr3+、Fe3+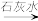 Cr(O3)、Fe(OH)3
Cr(O3)、Fe(OH)3(3)该废水中加入FeSO4•7H2O和稀硫酸,发生反应的离子方程式为:
(4)欲使25 L该废水中
 转化为Cr3+,理论上需要加入
转化为Cr3+,理论上需要加入(5)若处理后的废水中残留的 c(Fe3+)=1×10-13mol/L ,则残留的 Cr3+ 的浓度为
III. 已知:I2+2S2O32-==2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
(6)步骤c中判断恰好反应完全的现象为
(7)根据以上实验和包装袋说明,所测精制盐的碘含量是
您最近一年使用:0次



