名校
解题方法
1 . 已知AgCl的溶解平衡:AgCl(s) Ag+(aq)+Cl-(aq),下列说法不正确的是
Ag+(aq)+Cl-(aq),下列说法不正确的是
 Ag+(aq)+Cl-(aq),下列说法不正确的是
Ag+(aq)+Cl-(aq),下列说法不正确的是| A.除去溶液中Ag+,加盐酸盐比硫酸盐好 |
| B.加入H2O,溶解平衡不移动 |
| C.用NaCl溶液代替蒸馏水洗涤AgCl,可以减少沉淀损失 |
| D.反应2AgCl+Na2S=Ag2S+2NaCl,说明溶解度:AgCl>Ag2S |
您最近一年使用:0次
2021-09-03更新
|
409次组卷
|
12卷引用:四川省遂宁市射洪中学2020-2021学年高二下学期第一次月考化学试题
四川省遂宁市射洪中学2020-2021学年高二下学期第一次月考化学试题河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题(已下线)第三章第四节 难溶电解的溶解平衡(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)(已下线)3.4.2 沉淀溶解平衡原理的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)2018版化学(苏教版)高考总复习专题八课时跟踪训练--难溶电解质的沉淀溶解平衡四川省成都市七中实验学校2018-2019学年高二5月月考化学试题(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》云南省曲靖市沾益县第二中学2019-2020学年高二上学期期末考试化学试题云南省景东彝族自治县第一中学2021-2022学年高二下学期开学考试化学试题作业(二十二) 沉淀的溶解与生成、转化及应用作业(二十一) 沉淀溶解平衡与溶度积云南省昆明师范专科学校附属中学2022-2023学年高二上学期期末考试化学试题
2021高三·全国·专题练习
名校
2 . 某兴趣小组进行下列实验:
①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是
①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是
| A.将①中所得浊液过滤,所得滤液中含少量Mg2+ |
| B.①中浊液中存在沉淀溶解平衡: Mg(OH)2(s)⇌ Mg2+(aq)+2OH-(aq) |
| C.实验②和③均能说明Fe(OH)3比Mg(OH)2难溶 |
D.NH4Cl溶液中的NH 可能是④中沉淀溶解的原因 可能是④中沉淀溶解的原因 |
您最近一年使用:0次
2021-08-10更新
|
982次组卷
|
11卷引用:考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)3.4.1 沉淀溶解平衡原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)江苏省扬州中学2021-2022学年上学期高二12月月考化学试题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)河北省石家庄市正中实验中学东校区2022-2023学年高二上学期10月月考化学试题黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡作业(二十一) 沉淀溶解平衡的应用
3 . 已知p(Ba2+)=-lgc(Ba2+)、p(X2-)= -lgc(X2-),常温下BaSO4、BaCO3的沉淀溶解平衡曲线如图所示,下列叙述中正确的是
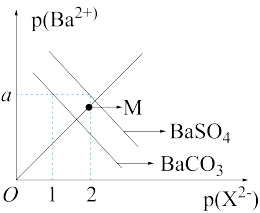

A.BaCO3与BaSO4的饱和溶液中,p(Ba2+)=a时,c(SO ) = 2c(CO ) = 2c(CO ) ) |
| B.向纯水中加入适量BaCO3固体可配制M点对应的溶液 |
C.向c(SO )=c(CO )=c(CO )的溶液中加入BaCl2固体,先生成BaCO3沉淀 )的溶液中加入BaCl2固体,先生成BaCO3沉淀 |
| D.Ksp(BaSO4)<Ksp(BaCO3),BaSO4不能转化为BaCO3 |
您最近一年使用:0次
2021-08-04更新
|
425次组卷
|
4卷引用:重庆南开中学2020-2021学年高二下学期期中考试化学试题
重庆南开中学2020-2021学年高二下学期期中考试化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)辽宁省辽河油田第一高级中学2021-2022学年高二上学期期中考试化学试题
解题方法
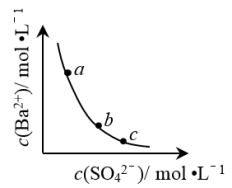
4 . 一定温度下,BaSO4(s)⇌Ba2+(aq)+ (aq)平衡体系中,c(Ba2+)和c(
(aq)平衡体系中,c(Ba2+)和c( )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是
 (aq)平衡体系中,c(Ba2+)和c(
(aq)平衡体系中,c(Ba2+)和c( )的关系如图所示。下列说法正确的是
)的关系如图所示。下列说法正确的是
| A.a、b、c三点对应的KW不相等 |
B.a、b、c三点对应c(Ba2+)•c( )的数值,a点最大 )的数值,a点最大 |
C.BaSO4在水中形成的饱和溶液,c(Ba2+)=c( ) ) |
| D.a点对应的溶液中加入BaSO4固体,c(Ba2+)沿曲线向b、c点方向变化 |
您最近一年使用:0次
名校
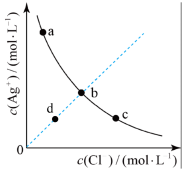
5 . 一定温度下,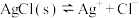 体系中,
体系中, 和
和 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 体系中,
体系中, 和
和 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.a、b、c三点对应的 相等 相等 |
| B.d点的溶液为AgCl的不饱和溶液 |
| C.向该平衡体系中加入NaCl固体,不会有AgCl沉淀析出 |
D.AgCl溶于水形成的饱和溶液中,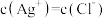 |
您最近一年使用:0次
2021-08-01更新
|
911次组卷
|
5卷引用:选择性必修1(SJ)专题3第四单元 沉淀溶解平衡
选择性必修1(SJ)专题3第四单元 沉淀溶解平衡(已下线)第3章 水溶液中的离子平衡(提分小卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)3.4.1 难溶电解质的沉淀溶解平衡(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)3.4.1沉淀溶解平衡原理 课后云南省楚雄第一中学2022-2023学年高二下学期期末考试化学试题
6 . 常温下几种阳离子浓度与溶液pH的关系如图所示。据图判断下列说法正确的是
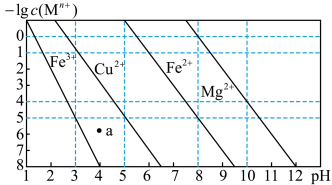

| A.Ksp[Fe(OH)2]=1.0×10-21 |
| B.Mg(OH)2饱和溶液中c(Mg2+)=1.0×10-4mol/L |
| C.a点可表示Fe(OH)3的不饱和溶液,Cu(OH)2的饱和溶液 |
| D.Fe3+浓度为0.01mol/L溶液中,调节pH=3.2,可认为Fe3+沉淀完全 |
您最近一年使用:0次
7 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
I.已知 在水中存在以下平衡:
在水中存在以下平衡: ,
, 。
。
(1)常温下NaHA溶液的pH_______ (填序号),原因_______ ;
A.大于7 B.小于7 C.等于7 D.无法确定
(2)某温度下,若向 的NaHA溶液中逐滴滴加
的NaHA溶液中逐滴滴加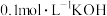 溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是_______ ;
A.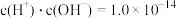 B.
B.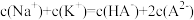
C.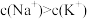 D.
D.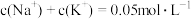
(3)已知常温下 的钙盐(CaA)的饱和溶液中存在以下平衡:
的钙盐(CaA)的饱和溶液中存在以下平衡: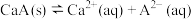
 。若要使该溶液中
。若要使该溶液中 浓度变小,可采取的措施有
浓度变小,可采取的措施有_______ ;
A.升高温度 B.降低温度 C.加入 晶体
晶体
II.含有 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含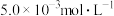 的
的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理: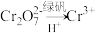 、
、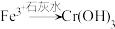 、
、
(1)若处理后的废水中残留的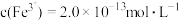 ,则残留的
,则残留的 的浓度为
的浓度为_______ ;(已知: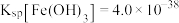 ,
,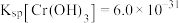 )
)
(2)已知室温时,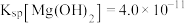 。在0.1mo/L的
。在0.1mo/L的 溶液中,逐滴加入NaOH溶液,当
溶液中,逐滴加入NaOH溶液,当 完全沉淀时,溶液的pH是
完全沉淀时,溶液的pH是_______ ;(已知 )
)
I.已知
 在水中存在以下平衡:
在水中存在以下平衡: ,
, 。
。(1)常温下NaHA溶液的pH
A.大于7 B.小于7 C.等于7 D.无法确定
(2)某温度下,若向
 的NaHA溶液中逐滴滴加
的NaHA溶液中逐滴滴加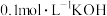 溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性(忽略混合后溶液的体积变化)。此时该混合溶液中的下列关系一定正确的是A.
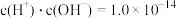 B.
B.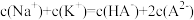
C.
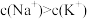 D.
D.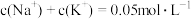
(3)已知常温下
 的钙盐(CaA)的饱和溶液中存在以下平衡:
的钙盐(CaA)的饱和溶液中存在以下平衡: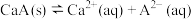
 。若要使该溶液中
。若要使该溶液中 浓度变小,可采取的措施有
浓度变小,可采取的措施有A.升高温度 B.降低温度 C.加入
 晶体
晶体II.含有
 的废水毒性较大,某工厂废水中含
的废水毒性较大,某工厂废水中含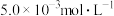 的
的 。为了使废水的排放达标,进行如下处理:
。为了使废水的排放达标,进行如下处理: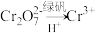 、
、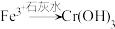 、
、
(1)若处理后的废水中残留的
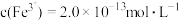 ,则残留的
,则残留的 的浓度为
的浓度为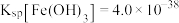 ,
,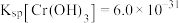 )
)(2)已知室温时,
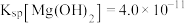 。在0.1mo/L的
。在0.1mo/L的 溶液中,逐滴加入NaOH溶液,当
溶液中,逐滴加入NaOH溶液,当 完全沉淀时,溶液的pH是
完全沉淀时,溶液的pH是 )
)
您最近一年使用:0次
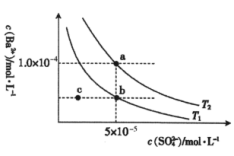
8 .  、
、 不同温度下
不同温度下 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
 、
、 不同温度下
不同温度下 在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A. |
| B.升温可使分散系由c点变为b点 |
C. 时 时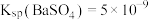 |
D.在 曲线下方区域(不含曲线)任意一点时,均有 曲线下方区域(不含曲线)任意一点时,均有 沉淀生成 沉淀生成 |
您最近一年使用:0次
名校
9 . 通过表中的相关数据,计算、分析、判断给出结论,题目所给数据和条件均为常温下:
(1)NH4F溶液显_______ 性。
(2)NH4HCO3 溶液与少量NaOH溶液反应时,_______ (填离子符号)先与 NaOH溶液中的OH-反应。
(3)①反应 CuS(s) + H2SO4(aq)⇌H2S(aq) + CuSO4(aq)的 K=_______ ;反应 FeS(s) + H2SO4(aq)⇌H2S(aq)+FeSO4 (aq)的 K= 3.9×103;
②反应 CuS(s)+Fe2+(aq)⇌FeS(s)+Cu2+(aq)的 K=_______ (以上计算结果均保留两位有效数字)。
③由计算结果可以知道实验室制备H2S气体应选用_______ ,检验H2S气体应选用_______ (均用上述反应中的盐类物质作答)
(4)除去废水中的Cu2+使用过量的FeS固体的优点有:
①可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;
②_______ 。
| NH3•H2O | Kb=1.8×10-5 |
| H2CO3 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| HF | Ka=6.8×10-4 |
| H2S | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| H2O | Kw=10-14 |
| Cu(OH)2 | Ksp=2.2×10-20 |
| Fe(OH)3 | Ksp=4.0×10-38 |
| CuS | Ksp=6.3×10-36 |
| FeS | Ksp=3.6×10-18 |
| 常用对数 | lg2=0.3 lg2.2=0.34 lg3=0.48 |
(1)NH4F溶液显
(2)NH4HCO3 溶液与少量NaOH溶液反应时,
(3)①反应 CuS(s) + H2SO4(aq)⇌H2S(aq) + CuSO4(aq)的 K=
②反应 CuS(s)+Fe2+(aq)⇌FeS(s)+Cu2+(aq)的 K=
③由计算结果可以知道实验室制备H2S气体应选用
(4)除去废水中的Cu2+使用过量的FeS固体的优点有:
①可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;
②
您最近一年使用:0次
解题方法
10 . 下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 取两支试管,各加入4mL0.01mol·L-1KMnO4酸性溶液,然后向一支试管中加入2mL0.1mol·L-1H2C2O4溶液;向另一支试管中加入2mL0.2mol·L-1H2C2O4溶液。第二支试管中溶液褪色更快些 | 其他条件相同时,H2C2O4的浓度越大,反应速率越快 |
| B | 用pH试纸测得CH3COONa溶液的pH约为8,NaClO溶液的pH约为10 | CH3COOH电离出H+的能力比HClO的强 |
| C | 检验FeCl2溶液中是否含有Fe2+时,取少量该溶液,滴入酸性KMnO4溶液,溶液紫红色褪去 | 证明溶液中含有Fe2+ |
| D | 向浓度均为0.05mol·L-1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



