湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
湖北
高二
开学考试
2021-07-23
277次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、化学与STSE、化学实验基础、常见无机物及其应用
湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
湖北
高二
开学考试
2021-07-23
277次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、化学与STSE、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 化学知识在新冠肺炎的疫情防控中发挥着重要作用,下列说法正确的是
| A.冠状病毒粒子直径约60~220nm,故介于溶质和胶体粒子之间 |
| B.针对新冠肺炎疫情,可用高锰酸钾溶液、无水酒精、双氧水等对场所进行杀菌消毒 |
| C.过氧乙酸和ClO2泡腾片均可杀灭病毒,二者消毒原理均是利用了其强氧化性 |
| D.用热的“84”消毒液可以提升杀菌消毒效果 |
您最近一年使用:0次
单选题
|
适中(0.65)
2. 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,22.4LCl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为2NA |
| B.密闭容器中2molNO与1molO2充分反应,产物分子的数目为2NA |
| C.钢铁发生电化学腐蚀生成0.1molFe2O3·nH2O(铁锈),则负极上铁单质失去的电子数为0.4NA |
| D.1L0.1mol·L-1葡萄糖溶液中分子总数为0.1NA |
【知识点】 阿伏加德罗常数的求算解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、 、 、 |
B. =1×10-12的溶液中:K+、Na+、 =1×10-12的溶液中:K+、Na+、 、 、 |
C.c(Fe3+)=1mol/L的溶液中:Na+、SCN-、ClO-、 |
D.能使甲基橙变红的溶液中:Cu2+、Fe2+、 、 、 |
【知识点】 限定条件下的离子共存解读 水的电离
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
4. 下列离子方程式书写正确的是
A.侯式联合制碱法:Na++H2O+NH3+CO2=NaHCO3↓+ |
B.电解氯化镁溶液:2Cl—+2H2O 2OH—+H2↑+Cl2↑ 2OH—+H2↑+Cl2↑ |
C.草酸使酸性KMnO4溶液褪色:2 +5 +5 +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
D.铅蓄电池放电时负极反应:PbO2+2e—+4H++ =PbSO4+2H2O =PbSO4+2H2O |
【知识点】 离子方程式的正误判断解读 铅蓄电池解读 电解原理的应用
您最近一年使用:0次
单选题
|
适中(0.65)
名校
5. 下列说法正确的是
| A.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| B.用H2S作沉淀剂,可除去废水中的Fe2+和Cu2+ |
| C.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| D.将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,AgCl沉淀少于AgBr |
您最近一年使用:0次
2021-07-16更新
|
195次组卷
|
4卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题安徽省合肥市第八中学2021-2022学年高二下学期实验班开学考化学试题(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)
单选题
|
较易(0.85)
6. 无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为:2Al2O3(s)+6Cl2(g)⇌4AlCl3(g)+3O2(g) ΔH>0。下列分析正确的是
| A.增大Al2O3用量,化学平衡向正反应方向移动 |
| B.电解熔融的Al2O3和AlCl3均能得到单质铝 |
| C.加入碳粉,平衡正向移动是因为碳与O2反应,降低了生成物的浓度且放出热量 |
| D.其他条件不变时,升高温度,正反应速率加快,逆反应速率减慢 |
您最近一年使用:0次
2021-07-16更新
|
174次组卷
|
2卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
单选题
|
适中(0.65)
解题方法
7. 叠氮酸(HN3)是无色有刺激性气味极易爆炸的液体,酸性类似于醋酸。下列说法错误的是
| A.0.01mol·L-1HN3溶液的pH>2 |
B.NaN3的电离方程式:NaN3=Na++ |
| C.HN3溶液的pH随温度升高而减小 |
D.0.01mol·L-1NaN3溶液中:c(Na+)+c(H+)=c( )+c(HN3) )+c(HN3) |
您最近一年使用:0次
单选题
|
适中(0.65)
8. 某化工厂制备净水剂硫酸铁铵晶体[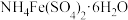 ]的一种方案如下:
]的一种方案如下:
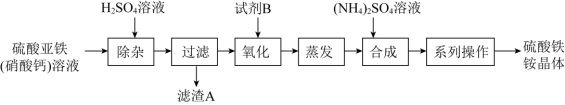
下列说法不正确的是
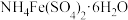 ]的一种方案如下:
]的一种方案如下:
下列说法不正确的是

| A.滤渣A的主要成分是CaSO4 |
| B.硫酸铁铵水解形成的胶体具有吸附作用 |
| C.“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等 |
D.相同条件下,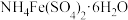 净水能力比FeCl3强 净水能力比FeCl3强 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
9. 下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 取两支试管,各加入4mL0.01mol·L-1KMnO4酸性溶液,然后向一支试管中加入2mL0.1mol·L-1H2C2O4溶液;向另一支试管中加入2mL0.2mol·L-1H2C2O4溶液。第二支试管中溶液褪色更快些 | 其他条件相同时,H2C2O4的浓度越大,反应速率越快 |
| B | 用pH试纸测得CH3COONa溶液的pH约为8,NaClO溶液的pH约为10 | CH3COOH电离出H+的能力比HClO的强 |
| C | 检验FeCl2溶液中是否含有Fe2+时,取少量该溶液,滴入酸性KMnO4溶液,溶液紫红色褪去 | 证明溶液中含有Fe2+ |
| D | 向浓度均为0.05mol·L-1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)>Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
10. 接触法制硫酸的工艺流程中的关键步骤是SO2的催化氧化:2SO2+O2 2SO3ΔH<0,在催化剂表面的反应历程如下:
2SO3ΔH<0,在催化剂表面的反应历程如下:
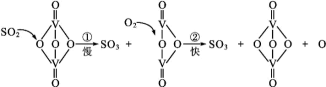
下列说法正确的是
 2SO3ΔH<0,在催化剂表面的反应历程如下:
2SO3ΔH<0,在催化剂表面的反应历程如下:
下列说法正确的是
| A.过程中既有V—O键的断裂,又有V—O键的形成 |
| B.该反应的中间产物是V2O5 |
| C.反应①的活化能比反应②小 |
| D.反应放热,为提高SO2转化率,应尽可能在较低温度下反应 |
您最近一年使用:0次
2021-07-16更新
|
244次组卷
|
3卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题重庆市实验中学2021-2022学年上学期高二10月月考化学试题(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)
单选题
|
适中(0.65)
名校
11. 我国科学家采用碳基电极材料成功实现了电解气态HCl制备Cl2,其工作原理如图所示。下列说法正确的是


| A.电路中转移2mol电子,需要消耗11.2LO2 |
| B.阳极的电极反应为2Cl--2e-=Cl2↑ |
| C.通电后H+从左室迁移至右室 |
| D.左室中发生反应4Fe2++O2+4H+=4Fe3++2H2O,实现了Fe3+的再生 |
【知识点】 电解原理的应用
您最近一年使用:0次
2021-07-16更新
|
176次组卷
|
4卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 用CuCl2·2H2O晶体制取无水CuCl2的实验装置如图所示,下列说法错误的是
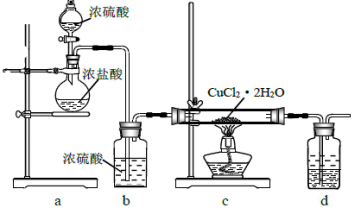

| A.先滴入浓硫酸,再点燃c处酒精灯 |
| B.通入HCl可以抑制CuCl2的水解 |
| C.装置d中上层为苯,下层为NaOH溶液 |
| D.硬质玻璃管内部右侧会出现白雾 |
您最近一年使用:0次
2021-07-16更新
|
153次组卷
|
2卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
单选题
|
适中(0.65)
名校
13. 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,发生如下反应:PCl5(g)⇌PCl3(g)+Cl2(g) ΔH=akJ·mol-1(a>0),0~10min保持容器温度不变,10min时改变一种条件,整个过程中PCl5、PCl3、Cl2的物质的量随时间的变化如图所示:
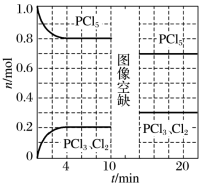
下列说法正确的是

下列说法正确的是
| A.0~4min的平均速率v(PCl3)=0.05mol·L-1·min-1 |
| B.4min反应达平衡时,吸收的热量为0.2akJ |
| C.10min时改变的条件是增加了一定量的PCl5 |
| D.增大压强,活化分子百分数增大,反应速率加快 |
您最近一年使用:0次
2021-07-16更新
|
152次组卷
|
2卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
单选题
|
适中(0.65)
14. 近日,中国科学院深圳先进技术研究院研发出一种高性能的钙离子电池:以溶有六氟磷酸钙Ca(PF6)2的碳酸酯类溶剂为电解液,放电时合金Ca7Sn6发生去合金化反应,阴离子(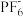 )从石墨烯中脱嵌,进入电解质溶液。放电时其工作原理如下图所示。下列说法正确的是
)从石墨烯中脱嵌,进入电解质溶液。放电时其工作原理如下图所示。下列说法正确的是
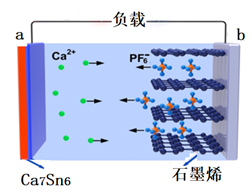
(已知:比能量为单位质量的电极放出电能的大小)
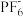 )从石墨烯中脱嵌,进入电解质溶液。放电时其工作原理如下图所示。下列说法正确的是
)从石墨烯中脱嵌,进入电解质溶液。放电时其工作原理如下图所示。下列说法正确的是
(已知:比能量为单位质量的电极放出电能的大小)
| A.此高性能的钙离子电池放电时,化学能可以全部转化为电能 |
| B.放电时,a电极的电极反应式为:Ca7Sn6-14e-=7Ca2++6Sn |
| C.充电时,b电极接电源的负极 |
| D.与锂离子电池相比较钙离子电池具有材料储量丰富、比能量高的优点 |
您最近一年使用:0次
单选题
|
适中(0.65)
15. 常温下,向1L0.5mol·L-1二元弱酸H2A溶液中滴加0.5mol·L-1NaOH溶液,溶液中含A粒子的物质的量分数(δ)与溶液pH的关系如下图所示。下列说法正确的是
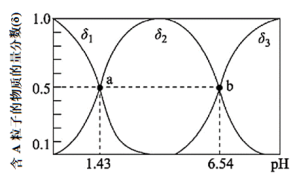

| A.向pH=6.54的溶液中持续滴加NaOH溶液,水的电离程度持续变大 |
| B.b点对应溶液中存在:c(HA-)=c(A2-)=c(H+) |
| C.当滴加1LNaOH溶液时,溶液中存在:c(Na+)>c(HA-)>c(H2A)>c(A2-) |
| D.反应H2A+A2-=2HA-的平衡常数K=105.11 |
您最近一年使用:0次
2021-07-16更新
|
254次组卷
|
3卷引用:湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题
湖北省新高考联考协作体2020-2021学年高二下学期收心考试化学试题(已下线)3.2.1 溶液的酸碱性-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)湖南省衡阳师范学院祁东附属中学2021-2022学年高三上学期12月月考化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
16. 利用尿素[CO(NH2)2]制备N2H4·H2O(水合肼)的实验流程如下图所示:
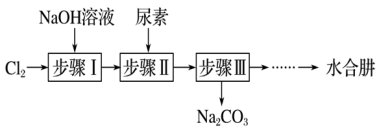
已知:①氯气与烧碱溶液的反应是放热反应;
②N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤I制备NaClO溶液。该反应的离子方程式为_______ 。实验中,为使步骤I中反应温度不高于40℃,除可采用冷水浴之外,还可采取的措施是_______ 。
(2)N2H4与硫酸形成的酸式盐的化学式为_______ 。
(3)步骤II合成N2H4·H2O。生成水合肼反应的化学方程式为_______ 。
(4)蒸馏得到水合肼粗产品,称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,在一定条件下,用0.15mol·L-1的碘的标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①滴定时,选用的指示剂为_______ 。
②达到滴定终点时消耗碘的标准溶液20.00mL,馏分中N2H4·H2O的质量分数为_______ 。
③下列操作中可能使馏分中水合肼的含量测定结果偏高的是_______ (填编号)。
A.锥形瓶清洗干净后未干燥
B.滴定前,滴定管内无气泡,滴定后有气泡
C.读数时,滴定前平视,滴定后俯视
D.盛标准液的滴定管水洗后,直接装标准液

已知:①氯气与烧碱溶液的反应是放热反应;
②N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。
(1)步骤I制备NaClO溶液。该反应的离子方程式为
(2)N2H4与硫酸形成的酸式盐的化学式为
(3)步骤II合成N2H4·H2O。生成水合肼反应的化学方程式为
(4)蒸馏得到水合肼粗产品,称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,在一定条件下,用0.15mol·L-1的碘的标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①滴定时,选用的指示剂为
②达到滴定终点时消耗碘的标准溶液20.00mL,馏分中N2H4·H2O的质量分数为
③下列操作中可能使馏分中水合肼的含量测定结果偏高的是
A.锥形瓶清洗干净后未干燥
B.滴定前,滴定管内无气泡,滴定后有气泡
C.读数时,滴定前平视,滴定后俯视
D.盛标准液的滴定管水洗后,直接装标准液
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
17. 我国科学家最近发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
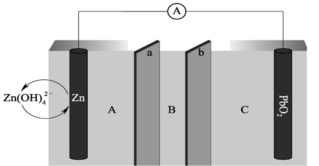
回答下列问题:
(1)电池中PbO2为_______ 极,C区域的电解质为_______ (填“K2SO4”“H2SO4”或“KOH”)。
(2)电池反应的离子方程式为_______ 。
(3)图中a膜为_______ 离子交换膜(填“阳”或“阴”)。
(4)已知E为电池电动势(即电池的理论电压,是两个电极电位之差,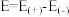 ),则该电池与传统铅酸蓄电池相比较
),则该电池与传统铅酸蓄电池相比较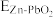
_______ 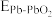 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)Zn是一种重要的金属材料,工业上一般先将ZnS氧化,再采用热还原或者电解法制备。利用H2还原ZnS生成Zn的反应方程式为:ZnS(s)+H2(g)⇌Zn(s)+H2S(g)。727℃时,该反应的平衡常数KP=2×10-6.此温度下,在盛有ZnS的刚性容器内通入压强为100kPa的H2,达平衡时H2S的分压为_______ Pa。

回答下列问题:
(1)电池中PbO2为
(2)电池反应的离子方程式为
(3)图中a膜为
(4)已知E为电池电动势(即电池的理论电压,是两个电极电位之差,
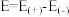 ),则该电池与传统铅酸蓄电池相比较
),则该电池与传统铅酸蓄电池相比较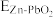
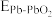 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)Zn是一种重要的金属材料,工业上一般先将ZnS氧化,再采用热还原或者电解法制备。利用H2还原ZnS生成Zn的反应方程式为:ZnS(s)+H2(g)⇌Zn(s)+H2S(g)。727℃时,该反应的平衡常数KP=2×10-6.此温度下,在盛有ZnS的刚性容器内通入压强为100kPa的H2,达平衡时H2S的分压为
【知识点】 化学反应原理综合考查解读 化学平衡的有关计算 原电池 原电池原理
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
解题方法
18. 2019年诺贝尔化学奖授予了三位对锂离子电池研究有突出贡献的著名科学家。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一、采用湿法治金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如下图:

已知:Ksp(Li2CO3)=1.6×10—3。部分物质的溶解度(S)如下表所示:
(1)写出碱溶时Al箔溶解的离子方程式_______ 。
(2)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放时正极的电极反应式为____ 。
(3)酸浸时产生标准状况下6.72LNO时,溶解LiFePO4_______ mol(其他杂质不与HNO3反应),若用H2O2代替HNO3,发生反应的离子方程式为_______ 。
(4)流程中用“热水洗涤”的原因是_______ 。
(5)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3后,Li+的沉降率到90%,计算滤液③中c( )=
)=_______ mol/L。
(6)“沉淀”时不能用Na2SO4溶液代替饱和Na2CO3溶液,原因是_______ 。

已知:Ksp(Li2CO3)=1.6×10—3。部分物质的溶解度(S)如下表所示:
| T/℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
| 20 | 1.33 | 34.2 | 0.039 |
| 80 | 0.85 | 30.5 | —— |
| 100 | 0.72 | —— | —— |
(1)写出碱溶时Al箔溶解的离子方程式
(2)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放时正极的电极反应式为
(3)酸浸时产生标准状况下6.72LNO时,溶解LiFePO4
(4)流程中用“热水洗涤”的原因是
(5)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3后,Li+的沉降率到90%,计算滤液③中c(
 )=
)=(6)“沉淀”时不能用Na2SO4溶液代替饱和Na2CO3溶液,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
19. 液氨是一种潜在的清洁汽车燃料,它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。请回答下列问题:
I.已知反应N2(g)+3H2(g)⇌2NH3(g)的活化能Ea1=akJ/mol,相关化学键键能数据如下表:
(1)反应2NH3(g)⇌N2(g)+3H2(g)的活化能Ea2=_______ kJ/mol(用含a的代数式表示)。
II.在2L恒容密闭容器中通入3molH2和1molN2,测得不同温度下,NH3的产率随时间变化如图所示:
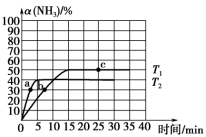
(2)下列有关说法正确的是_______ 。
A.由b点到c点混合气体密度逐渐减小
B.达到平衡时,3v正(H2)=2v逆(NH3)
C.平衡常数Ka<Kb=Kc
D.达到平衡时,向容器中通入氩气,平衡正向移动
(3)T1温度时,0~15min内v(H2)=_______ mol·L-1·min-1。
(4)已知:瞬时速率表达式v正=k正c3(H2)·c(N2),v逆=k逆c2(NH3)(k为速率常数,只与温度有关)。温度由T1调到T2,活化分子百分数___ (填“增大”“减小”或“不变”)。T1℃时, =
=____ (结果保留二位小数)。
III.向M、N两个装置中分别充入相同投料比的N2、H2,进行合成氨反应,各反应1小时,测定不同温度下N2的转化率,得到下图。
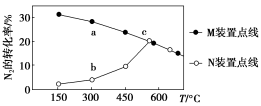
(5)N2、H2在M、N两装置中反应时,不同的条件可能是_______ 。
(6)在300℃时,a、b两点转化率存在差异的原因是______ 。
I.已知反应N2(g)+3H2(g)⇌2NH3(g)的活化能Ea1=akJ/mol,相关化学键键能数据如下表:
| 化学键 | H-H | N≡N | N-H |
| 键能/kJ·mol-1 | 436 | 946 | 391 |
(1)反应2NH3(g)⇌N2(g)+3H2(g)的活化能Ea2=
II.在2L恒容密闭容器中通入3molH2和1molN2,测得不同温度下,NH3的产率随时间变化如图所示:

(2)下列有关说法正确的是
A.由b点到c点混合气体密度逐渐减小
B.达到平衡时,3v正(H2)=2v逆(NH3)
C.平衡常数Ka<Kb=Kc
D.达到平衡时,向容器中通入氩气,平衡正向移动
(3)T1温度时,0~15min内v(H2)=
(4)已知:瞬时速率表达式v正=k正c3(H2)·c(N2),v逆=k逆c2(NH3)(k为速率常数,只与温度有关)。温度由T1调到T2,活化分子百分数
 =
=III.向M、N两个装置中分别充入相同投料比的N2、H2,进行合成氨反应,各反应1小时,测定不同温度下N2的转化率,得到下图。

(5)N2、H2在M、N两装置中反应时,不同的条件可能是
(6)在300℃时,a、b两点转化率存在差异的原因是
【知识点】 温度对化学反应速率的影响解读 化学平衡的有关计算
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、化学反应原理、有机化学基础、化学与STSE、化学实验基础、常见无机物及其应用
试卷题型(共 19题)
题型
数量
单选题
15
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 分散系概念及其分类 盐类水解在生活、生产中的应用 蛋白质的变性 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 阿伏加德罗常数的求算 | |
| 3 | 0.65 | 限定条件下的离子共存 水的电离 | |
| 4 | 0.65 | 离子方程式的正误判断 铅蓄电池 电解原理的应用 | |
| 5 | 0.65 | 溶度积规则及其应用 铜的电解精炼 金属的防护 | |
| 6 | 0.85 | 影响化学反应速率的因素 温度对化学反应速率的影响 浓度对化学平衡移动的影响 温度对化学平衡移动的影响 | |
| 7 | 0.65 | 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 8 | 0.65 | 盐类水解的应用 探究影响盐类水解平衡的因素 盐类水解在解题方面的应用 蒸发与结晶 | |
| 9 | 0.65 | Fe2+的鉴别及其应用 影响化学反应速率的因素 影响盐类水解程度的主要因素 难溶电解质的溶解平衡 | |
| 10 | 0.65 | 二氧化硫的化学性质 催化剂对化学反应速率的影响 化学反应条件的控制及其应用 | |
| 11 | 0.65 | 电解原理的应用 | |
| 12 | 0.65 | 盐类水解的应用 综合实验设计与评价 | |
| 13 | 0.65 | 化学反应速率计算 活化能及其对反应速率的影响 温度对化学反应速率的影响 化学平衡题中基于图表数据的相关计算 | |
| 14 | 0.65 | 原电池原理的应用 原电池电极反应式书写 新型电池 原电池、电解池综合考查 | |
| 15 | 0.65 | 酸碱混合时的定性判断及计算 弱电解质在水溶液中的电离平衡 | |
| 二、解答题 | |||
| 16 | 0.65 | 酸碱中和滴定实验基本操作及步骤 酸碱中和滴定的误差分析 物质含量的测定 | 工业流程题 |
| 17 | 0.65 | 化学反应原理综合考查 化学平衡的有关计算 原电池 原电池原理 | 原理综合题 |
| 18 | 0.4 | 氧化还原反应方程式的配平 溶度积常数相关计算 原电池电极反应式书写 常见无机物的制备 | 工业流程题 |
| 19 | 0.65 | 温度对化学反应速率的影响 化学平衡的有关计算 | 原理综合题 |



