名校
解题方法
1 . 下列表达式不正确的是
A. 制备 制备 : : |
B.AgCl的沉淀溶解平衡: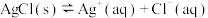 |
C.AgI的悬浊液中滴加 溶液: 溶液: |
D. 在溶液中的电离方程式为: 在溶液中的电离方程式为: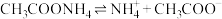 |
您最近一年使用:0次
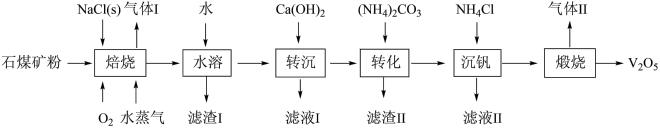
2 . 五氧化二钒(V2O5)可用于冶炼钒铁、用作合金添加剂、化工催化剂等。工业上利用石煤矿粉(主要含V2O3及少量Al2O3、SiO2)为原料生产V2O5的工艺流程如下:
①“水溶”、“转沉”、“转化”后,所得含钒物质分别为NaVO3、Ca3(VO4)2、(NH4)3VO4。
②不同pH下,正五价钒在溶液中主要存在形式见下表:
③25℃时,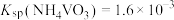 。
。
回答下列问题:
(1)“焙烧”时,V2O3发生反应的化学方程式为_____ 。
(2)“滤渣Ⅰ”的成分为_____ (填化学式,下同),“滤液Ⅰ”中溶质的成分为_____ 。
(3)先“转沉”后“转化”的目的是_____ 。
(4)“滤渣Ⅱ”经高温煅烧后水浸,所得物质可导入到_____ 操作中循环使用。
(5)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是_____ (写出两条)。
(6)25℃时,测得“转化”后所得滤液中 ,为使“沉钒”时,钒元素的沉淀率达到98%,应调节溶液中
,为使“沉钒”时,钒元素的沉淀率达到98%,应调节溶液中 至少为
至少为_____  。
。
(7)“煅烧”NH4VO3,制得产品V2O5,但反应体系中,若不及时分离出气体Ⅱ,部分V2O5。会转化成V2O4。已知V2O5转化成V2O4过程中,消耗的氧化剂与还原剂的物质的量之比为3∶2,则V2O5转化成V2O4的化学方程式为_____ 。
①“水溶”、“转沉”、“转化”后,所得含钒物质分别为NaVO3、Ca3(VO4)2、(NH4)3VO4。
②不同pH下,正五价钒在溶液中主要存在形式见下表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
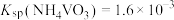 。
。回答下列问题:
(1)“焙烧”时,V2O3发生反应的化学方程式为
(2)“滤渣Ⅰ”的成分为
(3)先“转沉”后“转化”的目的是
(4)“滤渣Ⅱ”经高温煅烧后水浸,所得物质可导入到
(5)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是
(6)25℃时,测得“转化”后所得滤液中
 ,为使“沉钒”时,钒元素的沉淀率达到98%,应调节溶液中
,为使“沉钒”时,钒元素的沉淀率达到98%,应调节溶液中 至少为
至少为 。
。(7)“煅烧”NH4VO3,制得产品V2O5,但反应体系中,若不及时分离出气体Ⅱ,部分V2O5。会转化成V2O4。已知V2O5转化成V2O4过程中,消耗的氧化剂与还原剂的物质的量之比为3∶2,则V2O5转化成V2O4的化学方程式为
您最近一年使用:0次
2023-08-30更新
|
201次组卷
|
2卷引用:山西省朔州市怀仁市怀仁一中三校区2023-2024学年高三上学期第一次月考理综化学试题
3 . 秦俑彩绘中含有难溶的铅白( )和黄色的
)和黄色的 。常温下,
。常温下, 和
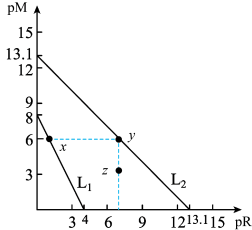
和 在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法错误的是
在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法错误的是
 )和黄色的
)和黄色的 。常温下,
。常温下, 和
和 在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法错误的是
在不同的溶液中分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法错误的是
A.完全沉淀废液中的 , , 的效果不如 的效果不如 |
B.z点,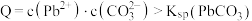 |
C.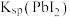 的数量级为 的数量级为 |
D. (s)转化为 (s)转化为 (s)的反应趋势很大 (s)的反应趋势很大 |
您最近一年使用:0次
2023-08-30更新
|
598次组卷
|
2卷引用:山西省朔州市怀仁市怀仁一中三校区2023-2024学年高三上学期第一次月考理综化学试题
名校
4 . 某温度下,Ksp(MnS)=2×10-13,Ksp(PbS)=2×10-28,生产中用MnS作为沉淀剂除去工业废水中Pb2+,其反应原理为Pb2+(aq)+MnS(s) PbS(s)+Mn2+(aq)。下列说法正确的是
PbS(s)+Mn2+(aq)。下列说法正确的是
 PbS(s)+Mn2+(aq)。下列说法正确的是
PbS(s)+Mn2+(aq)。下列说法正确的是| A.该反应的平衡常数K=1015 |
| B.PbS悬浊液中:c(Pb2+)=1×10-14mol•L-1 |
| C.该反应达平衡时c(Mn2+)=c(Pb2+) |
| D.其他条件不变,使平衡体系中c(Mn2+)增大,则c(Pb2+)减小 |
您最近一年使用:0次
2023-05-11更新
|
327次组卷
|
5卷引用:山西省朔州市怀仁一中2023-2024学年高二上学期12月期中考试化学试题
名校
解题方法
5 . 298K时,BaSO4与BaCO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是

已知101.4=25

已知101.4=25
| A.298K时,BaSO4的溶解度小于BaCO3的溶解度 |
| B.U点坐标为(4,4.8) |
| C.作为分散质BaSO4,W点v(沉淀)<v(溶解) |
D.对于沉淀溶解平衡BaSO4(s)+CO (aq) (aq) BaCO3(s)+SO BaCO3(s)+SO (aq),其平衡常数K=0.04 (aq),其平衡常数K=0.04 |
您最近一年使用:0次
2023-03-15更新
|
1089次组卷
|
6卷引用:2023届山西省太原市第五中学高三下学期5月二模理综试题
名校
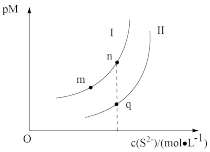
6 . 硫化锌(ZnS)和硫化铅(PbS)常用于光导体、半导体工业,它们在水中的沉淀溶解平衡曲线如图所示。已知: ,M为Zn或Pb,pM表示
,M为Zn或Pb,pM表示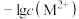 。下列说法正确的是
。下列说法正确的是
 ,M为Zn或Pb,pM表示
,M为Zn或Pb,pM表示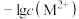 。下列说法正确的是
。下列说法正确的是
| A.曲线Ⅱ代表PbS的沉淀溶解平衡曲线 |
B.n、q两点溶液中的 :n<q :n<q |
C.图中m点和n点对应的 关系为 关系为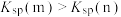 |
D.向m点对应的悬浊液中加入少量 固体,溶液组成由m沿mn曲线向n方向移动 固体,溶液组成由m沿mn曲线向n方向移动 |
您最近一年使用:0次
2023-02-15更新
|
333次组卷
|
2卷引用:山西省名校2022-2023学年高二下学期联合考试化学试题
名校
7 . 常温下, 在水中的沉淀溶解平衡曲线如图所示。下列判断正确的是
在水中的沉淀溶解平衡曲线如图所示。下列判断正确的是
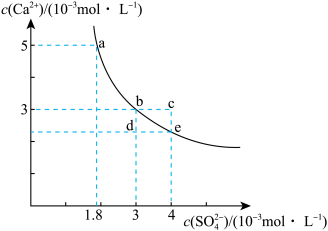
 在水中的沉淀溶解平衡曲线如图所示。下列判断正确的是
在水中的沉淀溶解平衡曲线如图所示。下列判断正确的是
A.溶液从a点变化到b点, 保持不变 保持不变 |
B.在 饱和溶液中加入 饱和溶液中加入 固体,可使溶液由b点变化到d点 固体,可使溶液由b点变化到d点 |
| C.常温下,e点的溶液蒸发溶剂后可变化到c点 |
D.常温下, |
您最近一年使用:0次
2023-02-11更新
|
118次组卷
|
2卷引用:山西省临汾市2022-2023学年高二下学期开学考试化学试题
名校
8 . 下列离子方程式书写正确的是
A. 溶液显碱性的原因: 溶液显碱性的原因: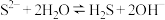 |
B. 的电离方程式: 的电离方程式: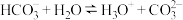 |
C.泡沫灭火器的原理: |
D. 的沉淀溶解平衡: 的沉淀溶解平衡: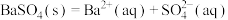 |
您最近一年使用:0次
名校
9 . 在T°C时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示。已知该温度下AgCl的Ksp=1.8×10-10。下列说法正确的是
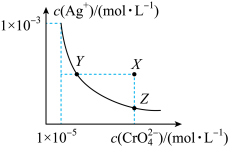

| A.T°C时,Ag2CrO4的Ksp为1.0×10-8 |
| B.T°C时,Y点和Z点时Ag2CrO4的Ksp不相等 |
| C.向Ag2CrO4饱和溶液中加入K2CrO4,可使溶液由Y点最终变为X点 |
| D.T°C时,将0.01mol·L-1AgNO3,溶液滴入20mL0.01mol·L-1KCl和0.01mol·L-1K2CrO4的混合溶液中,Cl-先沉淀 |
您最近一年使用:0次
2022-09-27更新
|
1040次组卷
|
5卷引用:山西省应县第一中学校2022-2023学年高二下学期7月期末考试化学试题
名校
解题方法
10 . 一定温度下,两种碳酸盐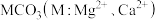 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
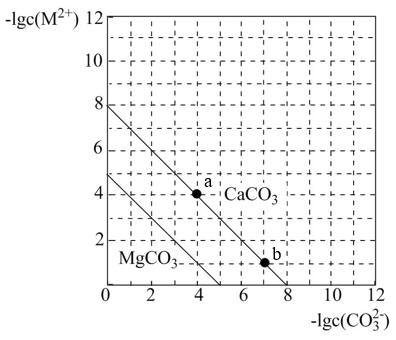
注: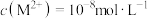 时,
时,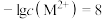 ;
;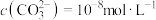 时。
时。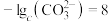
下列说法不正确 的是
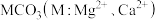 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
注:
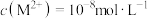 时,
时,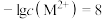 ;
;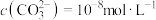 时。
时。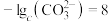
下列说法
A.该温度下, 的 的 |
B.该温度下,溶解度: |
C.欲使a点移动到b点,可向 浊液中加入适量 浊液中加入适量 固体 固体 |
D.反应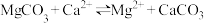 ,正向转化比逆向转化更难实现 ,正向转化比逆向转化更难实现 |
您最近一年使用:0次
2022-01-21更新
|
354次组卷
|
4卷引用:山西省大同市第一中学校2023-2024学年高二上学期12月月考化学试题



