1 . NiSO4•6H2O是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素的化合物杂质)为原料获得。操作步骤如图:

已知:各离子开始沉淀及完全沉淀时的pH如表所示:
(1)向滤液Ⅰ中加入FeS固体是为了生成更难溶于水的硫化物沉淀而除去Cu2+、Zn2+等杂质,则除去Cu2+的离子方程式为___________ ,当c(Cu2+)≤1.0×10-5mol•L-1时,可认为Cu2+已沉淀完全,此时溶液中S2-的浓度不小于___________ 。(已知:Ksp(CuS)=6.3×10-36)
(2)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加H2O2的目的是___________ 。
②调节滤液Ⅱ的pH,pH应控制在范围___________ 。
③检验滤液Ⅲ中杂质金属离子是否除尽的试剂是___________ 。
(3)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是___________ 。

已知:各离子开始沉淀及完全沉淀时的pH如表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 2.2 | 3.2 |
| Ni2+ | 6.4 | 8.4 |
(2)根据对滤液Ⅱ的操作作答:
①向滤液Ⅱ中加H2O2的目的是
②调节滤液Ⅱ的pH,pH应控制在范围
③检验滤液Ⅲ中杂质金属离子是否除尽的试剂是
(3)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是
您最近一年使用:0次
2022-09-26更新
|
251次组卷
|
2卷引用:江西省丰城市第九中学2021-2022学年高二上学期期末考试化学试题
2 . 回答下列问题:
(1)氯化铁水溶液呈酸性,原因是(用离子方程式表示 ) ___________ 。
(2)电离平衡常数可用来衡量弱电解质的电离程度。已知如下表数据( )
)
①25℃时,等物质的量浓度的3种溶液:a.NaCN溶液b.Na2CO3溶液c.CH3COONa溶液,其pH由大到小的顺序为___________ (填序号 ) 。
②25℃时,向 溶液中通入少量的
溶液中通入少量的 ,发生反应的
,发生反应的离子方程式为 ___________ 。
(3)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
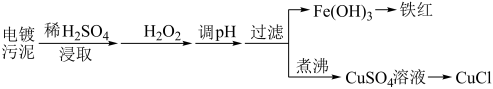
①酸浸后加入 的目的是
的目的是___________ ,调 的最适宜范围为
的最适宜范围为___________ 。
②调pH过程中加入的试剂最好是___________ 。
A.NaOH B.CuO C.NH3⋅H2O D.Cu2(OH)2CO3
③向 溶液中加入一定量的
溶液中加入一定量的 、
、 ,可以生成白色的
,可以生成白色的 沉淀,反应的化学方程式
沉淀,反应的化学方程式___ 。
(1)氯化铁水溶液呈酸性,原因是(
(2)电离平衡常数可用来衡量弱电解质的电离程度。已知如下表数据(
 )
)| 化学式 |  |  |  |
| 电离平衡常数 | 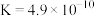 |  | 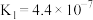  |
②25℃时,向
 溶液中通入少量的
溶液中通入少量的 ,发生反应的
,发生反应的(3)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
 的目的是
的目的是 的最适宜范围为
的最适宜范围为②调pH过程中加入的试剂最好是
A.NaOH B.CuO C.NH3⋅H2O D.Cu2(OH)2CO3
③向
 溶液中加入一定量的
溶液中加入一定量的 、
、 ,可以生成白色的
,可以生成白色的 沉淀,反应的化学方程式
沉淀,反应的化学方程式
您最近一年使用:0次
名校
解题方法
3 . I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过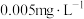 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。
(1)写出磷酸镉[ ]沉淀溶解平衡常数的表达式:
]沉淀溶解平衡常数的表达式: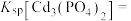
_______ 。
(2)一定温度下, 的
的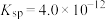 ,
, 的
的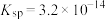 ,该温度下
,该温度下_______ [填“ ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。
(3)向某含镉废水中加入 ,当
,当 浓度达到
浓度达到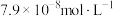 时,废水中
时,废水中 的浓度为
的浓度为____  [已知:
[已知: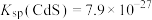 ],此时
],此时____ (填“符合”或“不符合”)《生活饮用水卫生标准》。
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,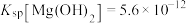 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:
25℃时,向 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为_______ 。
(5)常温下,向50mL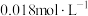 的
的 溶液中加入50mL
溶液中加入50mL 的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。
①反应后,溶液中
_______  。
。
②反应后,溶液的
_______ 。
③如果向反应后的溶液中继续加入50mL 的盐酸,
的盐酸,____ (填“有”或“无”)白色沉淀生成。
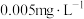 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。(1)写出磷酸镉[
 ]沉淀溶解平衡常数的表达式:
]沉淀溶解平衡常数的表达式: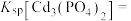
(2)一定温度下,
 的
的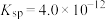 ,
, 的
的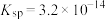 ,该温度下
,该温度下 ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。(3)向某含镉废水中加入
 ,当
,当 浓度达到
浓度达到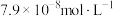 时,废水中
时,废水中 的浓度为
的浓度为 [已知:
[已知: ],此时
],此时II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,
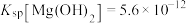 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:| pH |  | 8.0~9.6 | 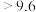 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为(5)常温下,向50mL
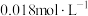 的
的 溶液中加入50mL
溶液中加入50mL 的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。①反应后,溶液中

 。
。②反应后,溶液的

③如果向反应后的溶液中继续加入50mL
 的盐酸,
的盐酸,
您最近一年使用:0次
2022-09-04更新
|
1648次组卷
|
5卷引用:江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题
江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题第三章水溶液中的离子反应与平衡黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期期中考试化学试题广东省揭阳市惠来县第一中学2022-2023学年高二上学期12月月考化学试题(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)
名校
解题方法
4 . 下列实验能达到预期目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 向溶液X中滴加浓盐酸,将产生气体通入品红溶液,溶液褪色 | 证明溶液X中含有 或 或 |
| B | 室温下,向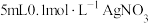 溶液中加入几滴 溶液中加入几滴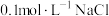 溶液出现白色沉淀,再滴加几滴 溶液出现白色沉淀,再滴加几滴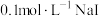 溶液,出现黄色沉淀 溶液,出现黄色沉淀 | 证明相同温度下: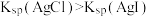 |
| C | 常温下,测得相同浓度溶液的 : : | 证明常温下的水解程度: |
| D | 将 溶液滴入酸性 溶液滴入酸性 溶液中,紫红色褪去 溶液中,紫红色褪去 | 证明 有还原性 有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-02更新
|
1369次组卷
|
4卷引用:江西省新余市2022-2023学年高二上学期期末质量检测化学试题
5 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
 | 向苯酚浊液中加入 溶液,溶液变澄清 溶液,溶液变澄清 | 酸性:苯酚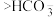 |
 | 无水乙醇与浓硫酸共热至 ,将产生的气体通入溴水中,溴水褪色 ,将产生的气体通入溴水中,溴水褪色 | 乙烯和溴水发生加成反应 |
 | 氯乙烷与 溶液共热后,滴加 溶液共热后,滴加 溶液,生成白色沉淀 溶液,生成白色沉淀 | 氯乙烷已发生水解 |
 | 在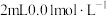 的 的 溶液中先滴入几滴 溶液中先滴入几滴  溶液有白色沉淀生成,再滴入 溶液有白色沉淀生成,再滴入  溶液,又出现黑色沉淀 溶液,又出现黑色沉淀 | 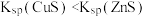 |
A. | B. | C. | D. |
您最近一年使用:0次
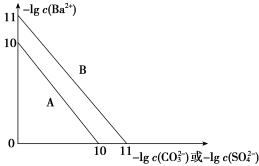
6 . 硫酸钡是一种比碳酸钡更难溶的物质。常温下-lg c(Ba2+)随-lg c(CO )或-lg c(SO
)或-lg c(SO )的变化趋势如图,下列说法正确的是
)的变化趋势如图,下列说法正确的是
 )或-lg c(SO
)或-lg c(SO )的变化趋势如图,下列说法正确的是
)的变化趋势如图,下列说法正确的是
| A.趋势线A表示硫酸钡 |
B.向100 mL含有CO 、SO 、SO 混合溶液中逐滴加入BaCl2溶液,SO 混合溶液中逐滴加入BaCl2溶液,SO 一定先沉淀 一定先沉淀 |
C.将碳酸钡和硫酸钡固体置于水中,此时溶液中的 =10 =10 |
| D.向碳酸钡悬浊液中加入饱和硫酸钠溶液,若碳酸钡转化成了硫酸钡,则可证明硫酸钡Ksp更小 |
您最近一年使用:0次
2022-08-16更新
|
598次组卷
|
7卷引用:江西省上饶市第一中学2022-2023学年高二上学期11月期中考试化学试题
江西省上饶市第一中学2022-2023学年高二上学期11月期中考试化学试题重庆市第七中学校2021-2022学年高二上学期第二次月考化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)【定心卷】3.4.2 沉淀溶解平衡的应用随堂练习-人教版2023-2024学年选择性必修1湖南省衡阳市衡阳县第二中学2023-2024学年高二上学期期中考试化学试题黑龙江省牡丹江市第一高级中学2023-2024学年高二下学期开学初测试 化学试题 (已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)
7 . 工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)制备PbSO4晶体的工艺流程如图:

已知:PbCl2难溶于冷水,易溶于热水;PbCl2(s)+2Cl-(aq) PbCl
PbCl (aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是
(aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是

已知:PbCl2难溶于冷水,易溶于热水;PbCl2(s)+2Cl-(aq)
 PbCl
PbCl (aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是
(aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是| A.“浸取”时的主要离子反应为MnO2+PbS+4H++2Cl-=PbCl2 +S+Mn2++2H2O |
| B.“滤渣2”的主要成分是Fe(OH)3 |
C.“沉降”时加入冰水,PbCl2(s)+2Cl-(aq) PbCl PbCl (aq)平衡左移,有利于PbCl2沉淀更完全 (aq)平衡左移,有利于PbCl2沉淀更完全 |
D.“沉淀转化”过程达平衡时,溶液中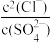 =1.6×103 =1.6×103 |
您最近一年使用:0次
2022-07-19更新
|
729次组卷
|
4卷引用:江西省九校2022-2023学年高二下学期开学联考化学试题
江西省九校2022-2023学年高二下学期开学联考化学试题河北省石家庄市第二中学教育集团2021-2022学年高二下学期期末考试化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)湖南省长沙麓山国际实验学校2023-2024学年高二下学期第一次学情检测化学试卷
8 . 下列事实不能用勒夏特列原理解释的是
A.石蕊(HZ)可发生电离:HZ(红色)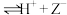 (蓝色),可用作酸碱指示剂 (蓝色),可用作酸碱指示剂 |
B.由 、 、 、HI(g)组成的平衡体系,加压后颜色变深 、HI(g)组成的平衡体系,加压后颜色变深 |
| C.黄绿色的氯水光照后颜色变浅 |
D.用 溶液将锅炉水垢中的 溶液将锅炉水垢中的 转化为 转化为 |
您最近一年使用:0次
解题方法
9 . 下列有关实验操作和现象与结论对应关系正确的是
| 选项 | 操作和现象 | 结论 |
| A | 向 溶液中加入足量硝酸,将产生的气体通入 溶液中加入足量硝酸,将产生的气体通入 溶液中,产生白色沉淀 溶液中,产生白色沉淀 | 非金属性:N>C>Si |
| B | 向酸性 溶液中滴加丙烯醇( 溶液中滴加丙烯醇(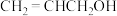 )并振荡,溶液褪色。 )并振荡,溶液褪色。 | 丙烯醇中含有醇羟基 |
| C | 向某待测液中滴加少量 ,再加入几滴KSCN溶液,溶液变为血红色 ,再加入几滴KSCN溶液,溶液变为血红色 | 待测液中一定含Fe3+ |
| D | 向10滴  溶液中,先滴入 溶液中,先滴入 的NaCl溶液,至不再有白色沉淀生成。再滴入 的NaCl溶液,至不再有白色沉淀生成。再滴入 的NaI溶液,白色沉淀转化为黄色沉淀。 的NaI溶液,白色沉淀转化为黄色沉淀。 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 按要求完成下列各空:
(1)25℃时,pH=2的盐酸 L与pH=10的NaOH溶液
L与pH=10的NaOH溶液 L混合,所得溶液pH=4,则
L混合,所得溶液pH=4,则
_______ 。
(2)25℃时,在等体积的①pH=1的 溶液、②
溶液、② 的
的 溶液、③pH=10的
溶液、③pH=10的 溶液、④pH=5的
溶液、④pH=5的 溶液中,发生电离的水的物质的量之比是
溶液中,发生电离的水的物质的量之比是_______ 。
(3) 相等的①
相等的① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液、④
溶液、④ 溶液,其物质的量浓度由大到小的顺序为
溶液,其物质的量浓度由大到小的顺序为_______ 。(填写序号)
(4)向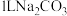 溶液中加入足量
溶液中加入足量 固体,当溶液中
固体,当溶液中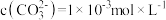 时,此时溶液中
时,此时溶液中
_______  。[已知
。[已知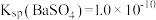 ,
,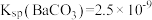 ]
]
(1)25℃时,pH=2的盐酸
 L与pH=10的NaOH溶液
L与pH=10的NaOH溶液 L混合,所得溶液pH=4,则
L混合,所得溶液pH=4,则
(2)25℃时,在等体积的①pH=1的
 溶液、②
溶液、② 的
的 溶液、③pH=10的
溶液、③pH=10的 溶液、④pH=5的
溶液、④pH=5的 溶液中,发生电离的水的物质的量之比是
溶液中,发生电离的水的物质的量之比是(3)
 相等的①
相等的① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液、④
溶液、④ 溶液,其物质的量浓度由大到小的顺序为
溶液,其物质的量浓度由大到小的顺序为(4)向
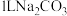 溶液中加入足量
溶液中加入足量 固体,当溶液中
固体,当溶液中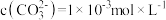 时,此时溶液中
时,此时溶液中
 。[已知
。[已知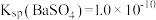 ,
,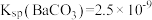 ]
]
您最近一年使用:0次



