名校
1 . 利用含钴废料(主要成分是Co3O4,还含有Fe、Al、Cu等杂质)为原料回收复合氧化钴的流程如图所示:

(1)“碱溶”所得的溶液中含有的阴离子为___________ 。
(2)“氧化”:加热搅拌条件下加入NaClO3的作用是___________ 。
(3)“除铁”:加入适量的Na2CO3调节酸度,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式___________ 。
(4)溶液e中加入(NH4)2C2O4使Co2+沉淀完全[c(Co2+)<10−5 mol∙L−1],控制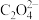 的浓度不小于
的浓度不小于___________ 。(已知:Ksp(CoC2O4)=6.3×10−8)
(5)称取2.940g CoC2O4,在空气中灼烧得1.740g复合氧化钴,则复合氧化钴的化学式为___________ 。

(1)“碱溶”所得的溶液中含有的阴离子为
(2)“氧化”:加热搅拌条件下加入NaClO3的作用是
(3)“除铁”:加入适量的Na2CO3调节酸度,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式
(4)溶液e中加入(NH4)2C2O4使Co2+沉淀完全[c(Co2+)<10−5 mol∙L−1],控制
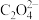 的浓度不小于
的浓度不小于(5)称取2.940g CoC2O4,在空气中灼烧得1.740g复合氧化钴,则复合氧化钴的化学式为
您最近一年使用:0次
2 . 化学与人类生产、生活、可持续发展密切相关。下列说法不正确的是
| A.乙烯的产量是衡量国家石油化工发展水平的重要标志 |
| B.用明矾代替二氧化氯处理生活污水,可提高杀菌消毒效果 |
| C.牙膏中添加氟化物用于预防龋齿 |
| D.锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
您最近一年使用:0次
2022-06-01更新
|
100次组卷
|
2卷引用:江西省丰城市第九中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
3 . 下列离子方程式正确 的是
A.往 溶液中滴加 溶液中滴加 溶液: 溶液: |
B.氢氧化铁溶于氢碘酸中: |
C.向 溶液中加入足量 溶液中加入足量 溶液:Mg(HCO3)2+2OH-=MgCO3↓+CO 溶液:Mg(HCO3)2+2OH-=MgCO3↓+CO +2H2O +2H2O |
D.往 中加入饱和 中加入饱和 溶液:CO 溶液:CO +BaSO4=BaCO3+SO +BaSO4=BaCO3+SO |
您最近一年使用:0次
2022-05-18更新
|
51次组卷
|
4卷引用:江西省赣州市赣县第三中学2021-2022学年高二上学期12月月考化学试卷
名校
4 . 某温度下,向体积均为20.00mL、浓度均为0.1mol•L-1的NaCl溶液、Na2CrO4溶液中分别滴加0.1mol•L-1的AgNO3溶液,滴定过程中的pX(PX=-lgX,X=Cl-、CrO )与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是
)与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是

 )与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是
)与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是
| A.曲线II表示AgNO3溶液滴定NaCl溶液的过程 |
| B.Ksp(Ag2CrO4)=10-2b |
| C.其他条件不变,如果NaCl溶液浓度改为0.05mol•L-1,则滴定终点向上移动 |
| D.若a=5 b=4,则用AgNO3标准液滴定NaCl时可用K2CrO4溶液做指示剂 |
您最近一年使用:0次
2022-05-09更新
|
620次组卷
|
5卷引用:江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
5 . 一种从废旧锂电池(主要含 ,及少量Al、Cu中制备钴酸钾(
,及少量Al、Cu中制备钴酸钾( )的工艺流程如下;
)的工艺流程如下;
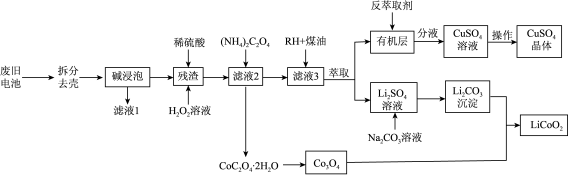
查阅资料: 具有很强的氧化性
具有很强的氧化性
(1)“碱浸泡”用来除去废旧电池中的Al,为提高该物质的去除率可采取的措施有___________ (任写一条)。
(2)向“残渣"中加入稀硫酸和 ,写出
,写出 参与反应的化学方程式
参与反应的化学方程式___________ 。
(3)向“滤液2”中加入沉淀剂时,若不采用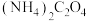 而采用
而采用 ,产物中会混有
,产物中会混有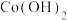 ,试分析原因
,试分析原因___________ 。
(4)RH蒸取 的原理可表示为:
的原理可表示为: 。实验室进行萃取实验用到的玻璃仪器是
。实验室进行萃取实验用到的玻璃仪器是___________ ;向有机层中加入反萃取剂___________ (填化学式)可将 反萃取至水层。
反萃取至水层。
(5)某 样品中可能含有的杂质为
样品中可能含有的杂质为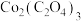 、
、 ,采用
,采用 滴定法测定该样品的组成,实验步骤如下:
滴定法测定该样品的组成,实验步骤如下:
Ⅰ.取m g样品于锥形瓶中,加入稀 溶解,水浴加热至75℃,用c
溶解,水浴加热至75℃,用c  的
的 溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗
溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗 溶液
溶液 mL。
mL。
Ⅱ.向上述溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 后,在75℃继续用c
后,在75℃继续用c 
 溶液滴定至溶液出现粉红色且30s内不褪色,又消耗
溶液滴定至溶液出现粉红色且30s内不褪色,又消耗 溶液
溶液 mL。
mL。
样品中所含 (
( )的质量分数表达式为
)的质量分数表达式为___________ 。若盛装 溶液的滴定管没有润洗,则测得样品中Co元素含量
溶液的滴定管没有润洗,则测得样品中Co元素含量___________ 。(填“偏高”、“偏低”、“无影响”)
 ,及少量Al、Cu中制备钴酸钾(
,及少量Al、Cu中制备钴酸钾( )的工艺流程如下;
)的工艺流程如下;
查阅资料:
 具有很强的氧化性
具有很强的氧化性(1)“碱浸泡”用来除去废旧电池中的Al,为提高该物质的去除率可采取的措施有
(2)向“残渣"中加入稀硫酸和
 ,写出
,写出 参与反应的化学方程式
参与反应的化学方程式(3)向“滤液2”中加入沉淀剂时,若不采用
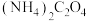 而采用
而采用 ,产物中会混有
,产物中会混有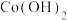 ,试分析原因
,试分析原因(4)RH蒸取
 的原理可表示为:
的原理可表示为: 。实验室进行萃取实验用到的玻璃仪器是
。实验室进行萃取实验用到的玻璃仪器是 反萃取至水层。
反萃取至水层。(5)某
 样品中可能含有的杂质为
样品中可能含有的杂质为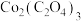 、
、 ,采用
,采用 滴定法测定该样品的组成,实验步骤如下:
滴定法测定该样品的组成,实验步骤如下:Ⅰ.取m g样品于锥形瓶中,加入稀
 溶解,水浴加热至75℃,用c
溶解,水浴加热至75℃,用c  的
的 溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗
溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗 溶液
溶液 mL。
mL。Ⅱ.向上述溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 后,在75℃继续用c
后,在75℃继续用c 
 溶液滴定至溶液出现粉红色且30s内不褪色,又消耗
溶液滴定至溶液出现粉红色且30s内不褪色,又消耗 溶液
溶液 mL。
mL。样品中所含
 (
( )的质量分数表达式为
)的质量分数表达式为 溶液的滴定管没有润洗,则测得样品中Co元素含量
溶液的滴定管没有润洗,则测得样品中Co元素含量
您最近一年使用:0次
6 . 下列有关说法正确的是
| A.使用广泛pH试纸测量“84”消毒液的pH |
B.反应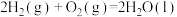 在一定条件能自发进行的原因是 在一定条件能自发进行的原因是 |
C.常温下,将稀 溶液加水稀释后,恢复至原温度,pH减小、 溶液加水稀释后,恢复至原温度,pH减小、 不变 不变 |
D.常温下,向 悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小 悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小 |
您最近一年使用:0次
名校
7 . 下列有关实验操作的解释或结论正确的是
| 实验操作 | 解释或结论 | |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2 固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| B | 加热石蜡油,将产生的气体通入酸性高锰酸钾,溶液褪色 | 证明反应一定生成了乙烯 |
| C | 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 用氢氧化钾与浓硫酸测定中和反应的反应热 | 测得的结果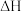 偏大 偏大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 常温下,几种难溶物的溶度积常数如下表所示。下列说法错误的是
| 化合物 |  |  |  |  |  |  |
 | 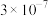 | 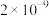 |  | 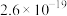 | 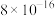 | 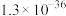 |
A.常温下,溶解度: |
B.向含同浓度的 和 和 混合溶液中滴加稀 混合溶液中滴加稀 溶液, 溶液, 先沉淀 先沉淀 |
C.向 悬浊液中加入 悬浊液中加入 溶液,无明显现象 溶液,无明显现象 |
D.反应 的平衡常数很小,反应几乎不进行 的平衡常数很小,反应几乎不进行 |
您最近一年使用:0次
名校
解题方法
9 . 氧化钴(Co2O3)在工业、电子、电讯等领域都有着广阔的应用前景。以铜钴矿石[主要成分为CoO(OH),CoCO3、Cu2(OH)2CO3和 SiO2,还有少量Fe、Mg、Ca的氧化物]为原料制备氧化钴(Co2O3)的工艺流程如图所示:

已知:常温下:Ksp(FeS)=6.3×10-18 Ksp(CuS)=6.3×10-36 Ksp(CaF2)=4.0×10-11 Ksp(MgF2)=9.0×10-11。
回答下列问题:
(1)写出“浸泡”过程中CoO(OH)与Na2SO3反应的离子方程式_______ 。
(2)“除铜”过程中,加入FeS固体得到更难溶的CuS,写出“除铜”过程的离子方程式_______ 。
(3)检验过程Ⅰ所得滤液中铁元素的离子已被完全沉淀的实验操作及现象:取少量待测液于试管中,_______ 。
(4)常温下,在过程Ⅱ中加入足量的NaF溶液可除去Ca2+、Mg2+,当两者沉淀完全时F-的浓度至少为_______ mol·L-1(溶液中离子浓度小于1×10-5 mol·L-1视为该离子沉淀完全)。
(5)过程Ⅲ中加入Na2CO3得到滤渣后又加入盐酸溶解,其目的是_______ 。

已知:常温下:Ksp(FeS)=6.3×10-18 Ksp(CuS)=6.3×10-36 Ksp(CaF2)=4.0×10-11 Ksp(MgF2)=9.0×10-11。
回答下列问题:
(1)写出“浸泡”过程中CoO(OH)与Na2SO3反应的离子方程式
(2)“除铜”过程中,加入FeS固体得到更难溶的CuS,写出“除铜”过程的离子方程式
(3)检验过程Ⅰ所得滤液中铁元素的离子已被完全沉淀的实验操作及现象:取少量待测液于试管中,
(4)常温下,在过程Ⅱ中加入足量的NaF溶液可除去Ca2+、Mg2+,当两者沉淀完全时F-的浓度至少为
(5)过程Ⅲ中加入Na2CO3得到滤渣后又加入盐酸溶解,其目的是
您最近一年使用:0次
名校
解题方法
10 . 下列实验操作和现象正确,且能得到对应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向 0.01mol/LKMnO4酸性溶液中滴加0.1mol/LH2C2O4溶液,充分振荡 | 溶液褪色 | H2C2O4体现氧化性 |
| B | 向滴有酚酞的Na2CO3溶液中加入BaCl2固体 | 溶液颜色逐渐褪去 | Na2CO3溶液中的水解平衡发生了移动 |
| C | 镀锡铁出现刮痕后浸入饱和食盐水中,一段时间后滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀 | 铁作原电池正极 |
| D | 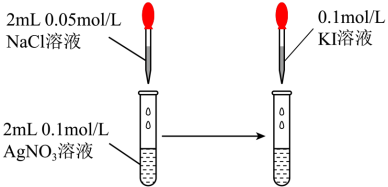 | 先产生白色沉淀,后变为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



