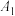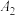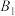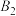1 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:

已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ 。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________ ;pH>9时,会导致___________ 。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为___________ 。

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,反应的离子方程式为
您最近一年使用:0次
2023-06-10更新
|
18684次组卷
|
18卷引用:新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题
新疆维吾尔自治区阿克苏地区第二中学2023-2024学年高三上学期第二次月考化学试题2023年高考新课标理综化学真题(已下线)T26-工业流程题(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题18 工艺流程题(已下线)2023年高考山东卷化学真题变式题(工业流程题)(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)四川省绵阳市高中理科突击班2023-2024学年高三上学期第零次诊断性考试理综化学试题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)四川省遂宁市第二中学校2023-2024学年高三上学期第一次诊断性考试理综试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省滨州市2023-2024学年高三上学期11月期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建
名校
解题方法
2 . 用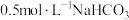 溶液滴定
溶液滴定 溶液,加入的碳酸氢钠溶液体积与溶液pH变化曲线如图所示,其中
溶液,加入的碳酸氢钠溶液体积与溶液pH变化曲线如图所示,其中 时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的
时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的 溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述错误的是
溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述错误的是

已知: ,
, 。
。
A.a点的混合溶液, |
| B.a→b的过程中,水的电离程度不断增大 |
C.总反应的化学方程式: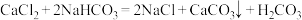 |
D.b点的混合溶液,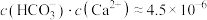 |
您最近一年使用:0次
2023-02-17更新
|
1381次组卷
|
8卷引用:新疆乌鲁木齐市2024届高三第一次质量监测化学试题
新疆乌鲁木齐市2024届高三第一次质量监测化学试题湖南省浏阳市第一中学2023届高三第六次月考化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)辽宁省部分学校2022-2023学年高三下学期三模化学试题 (已下线)2023年北京卷高考真题变式题(选择题11-14)辽宁省辽东南协作校2023届高三下学期第三次模拟考试化学试题河南省信阳高级中学2023-2024学年高三上学期11月一模考试化学试题四川省绵阳中学2023届高三三诊模拟考试理综-化学试题
3 . 已知: ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线如图所示。已知:
溶液的滴定曲线如图所示。已知: 。下列说法正确的是
。下列说法正确的是

 ,常温下向
,常温下向 溶液中滴加
溶液中滴加 溶液的滴定曲线如图所示。已知:
溶液的滴定曲线如图所示。已知: 。下列说法正确的是
。下列说法正确的是
A. 、 、 、 、 三点的 三点的 从大到小的顺序为 从大到小的顺序为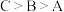 |
B.在 点的溶液中存在 点的溶液中存在 |
C.常温下,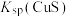 为 为 |
D.其他条件相同,若将 溶液换为同浓度、同体积的 溶液换为同浓度、同体积的 溶液,B点会平行向右移动 溶液,B点会平行向右移动 |
您最近一年使用:0次
2022-12-23更新
|
491次组卷
|
8卷引用:新疆昌吉回族自治州奇台县第一中学2022-2023学年高二上学期期末考试化学试题
新疆昌吉回族自治州奇台县第一中学2022-2023学年高二上学期期末考试化学试题河南省洛阳市2022-2023学年高三上学期期末测试化学试题河南省洛阳市2022-2023学年高三上学期普高联考测评(三)化学试题(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题安徽省淮北市第一中学2022-2023学年高二下学期第二次月考化学试题(已下线)选择题11-16云南省曲靖市第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
4 . 氯气及氯的化合物在生产生活中具有重要的作用,回答下列问题:
I.实验室制备少量的漂白液(装置如图)。

(1)图中盛装浓盐酸的仪器名称是__________ ,为了让液体顺利流下,滴加浓盐酸前的操作是__________ 。
(2)洗气瓶的导管口应__________ (填“长进短出”或“短进长出”),饱和食盐水的作用是____________ 。
(3)制备漂白液的离子方程式为______________________________ 。
II.室温下,实验室测定 的
的 并探究
并探究 浓度对
浓度对 沉淀溶解平衡的影响。
沉淀溶解平衡的影响。
已知: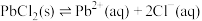 。
。
(4)将
 饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的
饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的 与树脂上的
与树脂上的 进行离子交换:
进行离子交换: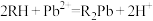 ,交换完成后,
,交换完成后, 随流出液流出,用
随流出液流出,用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 标准溶液的平均体积为
标准溶液的平均体积为 ,则
,则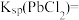
________ (用含b的代数式表示)。
(5)某实验小组同学往六个烧杯中分别加入不同体积的
 溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。
溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。
③该实验小组同学认为增大 的浓度,
的浓度, 沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是
沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是______________________________ 。
I.实验室制备少量的漂白液(装置如图)。

(1)图中盛装浓盐酸的仪器名称是
(2)洗气瓶的导管口应
(3)制备漂白液的离子方程式为
II.室温下,实验室测定
 的
的 并探究
并探究 浓度对
浓度对 沉淀溶解平衡的影响。
沉淀溶解平衡的影响。已知:
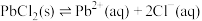 。
。(4)将

 饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的
饱和溶液以缓慢的流速通过阳离子交换树脂,此时溶液中的 与树脂上的
与树脂上的 进行离子交换:
进行离子交换: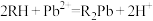 ,交换完成后,
,交换完成后, 随流出液流出,用
随流出液流出,用
 标准溶液滴定
标准溶液滴定 ,消耗
,消耗 标准溶液的平均体积为
标准溶液的平均体积为 ,则
,则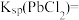
(5)某实验小组同学往六个烧杯中分别加入不同体积的

 溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。
溶液,测量对应的电导率(已知温度一定时,强电解质稀溶液的离子浓度越大,电导率越大),完成表格内容。烧杯及溶液 | 分别加入 | 电导率 |
三个装有 | 0 |
|
① |
| |
2 |
| |
三个装有 | 0 |
|
1 |
| |
2 |
|
 的浓度,
的浓度, 沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是
沉淀溶解平衡向生成沉淀的方向移动,支持他们观点的依据是
您最近一年使用:0次
2022-12-01更新
|
116次组卷
|
2卷引用:新疆兵团地州学校 2022-2023 学年高三上学期一轮期中调研考试化学试题
5 . 25℃时,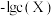 与pH的关系如图所示,X代表
与pH的关系如图所示,X代表 或
或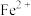 或
或 ,下列说法错误的是
,下列说法错误的是

已知:常温下, 的
的 ;强碱性溶液中Zn元素主要以
;强碱性溶液中Zn元素主要以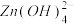 的形式存在。
的形式存在。
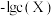 与pH的关系如图所示,X代表
与pH的关系如图所示,X代表 或
或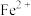 或
或 ,下列说法错误的是
,下列说法错误的是
已知:常温下,
 的
的 ;强碱性溶液中Zn元素主要以
;强碱性溶液中Zn元素主要以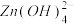 的形式存在。
的形式存在。A.曲线②代表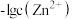 与pH的关系 与pH的关系 |
B.常温下, 的 的 的数量级为 的数量级为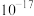 |
C.向等浓度的 和 和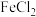 的混合溶液中滴入NaOH溶液, 的混合溶液中滴入NaOH溶液, 先沉淀 先沉淀 |
D.向 的溶液中加入等体积 的溶液中加入等体积 的HCl后,体系中Zn元素主要以 的HCl后,体系中Zn元素主要以 、 、 的形式存在 的形式存在 |
您最近一年使用:0次
2022-10-23更新
|
441次组卷
|
3卷引用:新疆兵团地州学校 2022-2023 学年高三上学期一轮期中调研考试化学试题
6 . LiMn2O4是一种锂离子电池的正极材料。用高锰酸钾废渣(主要成分为MnO2、Fe2O3、Al2O3、SiO2)和硫铁矿(主要成分为FeS2)制备LiMn2O4的工艺流程如图:
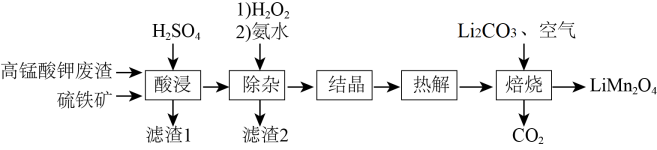
已知:①酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属间离子;
②25℃时,相关物质的Ksp见表。
(1)酸浸。MnO2与FeS2反应生成Fe3+和SO 的离子方程式为
的离子方程式为____ 。保持温度、浸取时间不变,能提高锰元素浸出率的措施有____ 。
(2)除杂。欲使溶液中的Al3+、Fe3+沉淀完全,调节溶液的pH最小值为____ (当溶液中某离子浓度c≤1×10-5mol·L-1时,可认为该离子沉淀完全)。
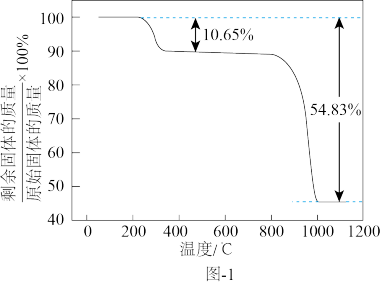
(3)热解。在真空中加热分解MnSO4•H2O,测得固体的质量随温度变化如图1所示。真空热解MnSO4•H2O制备Mn3O4,需控制的温度为_____ 。(写出计算推理过程)。
(4)焙烧。生成LiMn2O4的反应中,还原剂是____ (填化学式)。
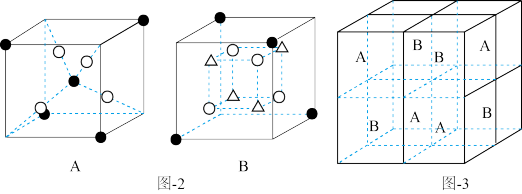
(5)一种LiMn2O4晶胞可看成由图2中A、B单元按图3方式构成。图2中“○”表示O2-,则“●”表示的微粒是____ (填离子符号)。

已知:①酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属间离子;
②25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
 的离子方程式为
的离子方程式为(2)除杂。欲使溶液中的Al3+、Fe3+沉淀完全,调节溶液的pH最小值为
(3)热解。在真空中加热分解MnSO4•H2O,测得固体的质量随温度变化如图1所示。真空热解MnSO4•H2O制备Mn3O4,需控制的温度为

(4)焙烧。生成LiMn2O4的反应中,还原剂是
(5)一种LiMn2O4晶胞可看成由图2中A、B单元按图3方式构成。图2中“○”表示O2-,则“●”表示的微粒是

您最近一年使用:0次
2022-09-08更新
|
413次组卷
|
2卷引用:新疆维吾尔自治区喀什第六中学2022-2023学年高三上学期9月月考化学试题
解题方法
7 . 在一定温度下,Mg(OH)2在水中的沉淀溶解平衡可用离子方程式表示为__________________ ,该平衡的Ksp可表示为____________________________ 。
您最近一年使用:0次
2021-12-02更新
|
574次组卷
|
2卷引用:新疆巴楚县第五中学等3校2022-2023学年高二上学期1月期末考试化学试题