1 . 已知常温时Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16,Ksp(Ag2CrO4)=1.1×10-12。下列说法中正确的是
| A.由于Ksp(AgCl)>Ksp(AgI),所以AgI可以转化为AgCl |
| B.向Ag2CrO4溶液中加入固体K2CrO4,溶解平衡逆向移动,所以Ag2CrO4的Ksp减小 |
| C.由于Ksp(Ag2CrO4)<Ksp(AgCl),所以沉淀AgCl容易转化为沉淀Ag2CrO4 |
| D.常温下,AgCl饱和溶液中加入NaI,若要使溶液中开始转化为AgI,则NaI的浓度必不低于0.75×10-11 mol·L-1 |
您最近一年使用:0次
2017-11-27更新
|
1294次组卷
|
4卷引用:同步君 选修4 第3章第4节 难溶电解质的溶解平衡
名校
2 . 25℃时,用0.1000 mol·L−1的AgNO3溶液分别滴定体积均为V0mL的且浓度均为0.1000mol·L−1的KCl、KBr及KI溶液,其滴定曲线入下图,已知25℃时,AgCl、AgBr及AgI溶度积常数依次为l.8×10-10、5.0×10-13、8.3×10-17,下列说法正确的是
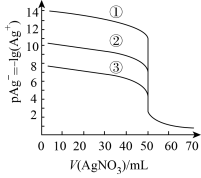

| A.V0= 45.00 |
| B.滴定曲线①表示KCl的滴定曲线 |
| C.滴定KCl时,可加入少量的KI作指示剂 |
| D.当AgNO3溶液滴定至60.00mL时,溶液中c(I-)<c(Br-)<c(Cl-) |
您最近一年使用:0次
2017-11-05更新
|
1068次组卷
|
6卷引用:山西实验中学、南海桂城中学2018届高三上学期联考化学试题
山西实验中学、南海桂城中学2018届高三上学期联考化学试题河北省定州中学2017-2018学年高二(承智班)上学期期中考试化学试题(已下线)黄金30题系列 高二化学(选修4) 小题易丢分陕西省高新中学2019届高三上学期月考化学试题(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析广东省深圳市光明区2023-2024学年高二上学期1月期末学业水平调研化学试题
名校
3 . 由下列实验及现象不能推出相应结论的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向Fe(NO3)3溶液中通入SO2,再滴加BaCl2溶液 | 产生白色沉淀 | 氧化性:NO3->Fe3+ |
| B | 将Na2O2粉末用脱脂棉包裹,向其中吹入CO2 | 粉末变白,脱脂棉燃烧 | Na2O2与CO2反应放热 |
| C. | 用铂丝蘸取某待测液在酒精灯上灼烧,透过蓝 色钴玻璃观察 | 火焰呈紫色 | 待测液中含钾元素 |
| D | 向2支盛有5 mL相同浓度氨水的试管中分别 加入5滴相同浓度的CuCl2溶液和CaCl2溶液 | 一支试管中产生蓝色沉 淀,另一支无明显现象 | Ksp[Cu(OH)2]< Ksp[Ca(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列根据实验现象得出的实验结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2样品中一定含有Fe3+ |
| B | 向KNO3和KOH混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸 | 试纸变为蓝色 | NO3-被还原NH3 |
| C | 向浓度均为0.1mol·L-1的Na2CO3和 Na2S混合溶液中滴入少量AgNO3溶液 | 产生黑色沉淀 | Ksp(Ag2S)>Ksp(Ag2CO3) |
| D | 向KI溶液中加入少量苯,然后加入FeCl3溶液 | 有机层呈橙红色 | 还原性:Fe2+>I- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 一定温度下,难溶电解质的饱和溶液中存在着沉淀溶解平衡,已知:

25℃时,对于含Fe2(SO4)3、FeSO4和CuSO4各0.5 mol的1L混合溶液,根据上表数据断,下列说法不正确的是

25℃时,对于含Fe2(SO4)3、FeSO4和CuSO4各0.5 mol的1L混合溶液,根据上表数据断,下列说法不正确的是
| A.在pH=5的溶液中.Fe3+不能大量存在 |
| B.混合溶液中c(SO42—):[c(Fe3+):c(Fe2+):c(Cu2+)]>5:4 |
| C.向混合溶液中逐滴加入0.1mol/LNaOH溶液,最先看到红褐色沉淀 |
| D.向混合溶液中加入适量氯水,并调节pH到3~4过滤,可获较纯净的CuSO4溶液 |
您最近一年使用:0次
名校
解题方法
6 . 未来脑教学云平台*按要求回答下列问题∶
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是___________ (填字母)。
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中 不变
不变
D. 溶液中 将减小
将减小
E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1∶V2=___________ (忽略溶液体积的变化)。
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是____________ (填字母)。
A.若混合后溶液呈中性,则c(H+)+c (OH-)=2×10-7h$mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有∶c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c (OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示∶
①写出向NaClO溶液中通入少量CO2的离子方程式___________________ 。
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是________ (填字母)。
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)= ________________ (填准确数值)。
(4)已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于_______________ 。
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中
 不变
不变D. 溶液中
 将减小
将减小E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1∶V2=
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是_
A.若混合后溶液呈中性,则c(H+)+c (OH-)=2×10-7h$mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有∶c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c (OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示∶
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)= _
(4)已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于
您最近一年使用:0次
2016-12-09更新
|
888次组卷
|
2卷引用:山西省康杰中学2017-2018学年高二上学期期中考试化学试题
名校
7 . 下列说法正确的是
| A.常温下向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| C.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| D.物质的溶解度都随温度的升高而增加,物质的溶解都是吸热的 |
您最近一年使用:0次
2016-12-09更新
|
489次组卷
|
9卷引用:2015届山西省临汾一中等四校高三第二次联考化学试卷
2015届山西省临汾一中等四校高三第二次联考化学试卷2015-2016学年山西省曲沃中学高二上学期12月月考化学试卷福建省惠安惠南中学2019届高三上学期期中考试化学试题【全国百强校】山东省泰安市第一中学2019届高三上学期12月学情诊断化学试题【全国百强校】四川省成都市石室中学2018-2019学年高二上学期期中考试化学试题四川省双流中学2019-2020学年高二3月月考化学试题四川省宜宾市叙州区第二中学校2019-2020学年高二下学期第二次月考化学试题四川省南充市南部县第二中学2021-2022学年高二下学期5月月考化学试题河南省确山县第二高级中学2021-2022学年高三上学期期中考试化学试题
13-14高三·浙江·开学考试
8 . 已知t ℃时AgCl的Ksp=2×10-10;在t ℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是

| A.在t ℃时,Ag2CrO4的Ksp为1×10-9 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| C.在t℃时,以0.01 mol/L AgNO3溶液滴定20 mL0.01 mol/LKCl和0.01 mol/L的K2CrO4的混和溶液,Cl-先沉淀 |
| D.在t ℃时,AgCl的溶解度大于Ag2CrO4 |
您最近一年使用:0次
2016-12-09更新
|
493次组卷
|
7卷引用:2015届山西省忻州市一中高三上学期期末理综化学试卷
2014·福建龙岩·一模
9 . 在K2CrO4溶液中存在着如下平衡2CrO42-+ 2H+ Cr2O72-+ H2O, K=1×1014。若用0.05mol K2Cr2O7配制成1LK2CrO4溶液,其中c(Cr2O72-)<10-5mol/L,则所配溶液的pH
Cr2O72-+ H2O, K=1×1014。若用0.05mol K2Cr2O7配制成1LK2CrO4溶液,其中c(Cr2O72-)<10-5mol/L,则所配溶液的pH
 Cr2O72-+ H2O, K=1×1014。若用0.05mol K2Cr2O7配制成1LK2CrO4溶液,其中c(Cr2O72-)<10-5mol/L,则所配溶液的pH
Cr2O72-+ H2O, K=1×1014。若用0.05mol K2Cr2O7配制成1LK2CrO4溶液,其中c(Cr2O72-)<10-5mol/L,则所配溶液的pH| A.>7 | B.<7 | C.=7 | D.无法确定 |
您最近一年使用:0次
2016-12-09更新
|
452次组卷
|
3卷引用:山西省晋中市平遥县第二中学2018-2019学年高二上学期12月月考化学试题
山西省晋中市平遥县第二中学2018-2019学年高二上学期12月月考化学试题(已下线)2013-2014福建龙岩市一级达标学校高中毕业联合考试理综化学试卷2016-2017学年山东省寿光现代中学高二12月月考化学卷2
10 . 20mL0.1mol/LFeCl3溶液中含有部分Fe2+,向其中滴加NaOH溶液至PH=4,溶液中有沉淀生成,过滤,得沉淀和滤液。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16。
下列说法错误的是
下列说法错误的是
| A.沉淀中只有Fe(OH)3 | B.沉淀中有Fe(OH)3和Fe(OH)2 |
| C.滤液c(Fe3+)=4.0×10-8mol/L | D.向滤液中滴加FeCl2溶液,无沉淀产生 |
您最近一年使用:0次
2016-12-09更新
|
893次组卷
|
6卷引用:山西省晋中市平遥县第二中学2018-2019学年高二上学期12月月考化学试题
山西省晋中市平遥县第二中学2018-2019学年高二上学期12月月考化学试题(已下线)2013-2014四川省绵阳市高三第三次诊断性考试理综化学试卷2016-2017学年山东省寿光现代中学高二12月月考化学卷22016-2017学年湖南省长沙市第一中学高二上学期期末考试化学试卷河南省洛阳市第一高级中学2019-2020学年高二12月月考化学试题(已下线)第10练 沉淀溶解平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)



