名校
解题方法
1 . Ⅰ.我国科学家利用CO2矿化反应释放能量设计出CO2矿化电池。不仅减碳发电,还能获得高附加值产品,其工作原理如图所示(Q是有机物;反应物和产物分别经过其它通道进入或排出电池容器)。

(1)通过离子交换膜的离子是___ ,正极区的电极反应式为:Q+2CO2+2H2O+2Na++2e—=2NaHCO3+QH2,在电极区溶液中可循环利用的物质是___ ,则电池的总反应方程式为____ 。
Ⅱ.以CO2为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二甲醚的合成塔中发生以下3个反应:
i.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=—49.01kJ·mol-1
CH3OH(g)+H2O(g) △H=—49.01kJ·mol-1
ii.2CH3OH(g) CH3OCH3(g)+H2O(g) △H=—24.52kJ·mol-1
CH3OCH3(g)+H2O(g) △H=—24.52kJ·mol-1
iii.CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.17kJ·mol-1
CO(g)+H2O(g) △H=+41.17kJ·mol-1
(2)2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)的△H=
CH3OCH3(g)+3H2O(g)的△H=___ kJ·mol-1。
(3)在压强3.0MPa、 =4条件下,CO2的平衡转化率和产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)。
=4条件下,CO2的平衡转化率和产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)。
①当温度超过290℃,CO2的平衡转化率随温度升高而增大的原因是___ 。除改变温度外,能提高二甲醚选择性的措施为____ (写一种即可)。
②根据图中的数据计算300℃上述反应达到平衡时CH3OCH3的物质的量分数为____ (保留三位有效数字)。

(4)在 =3时,反应CO2(g)+3H2(g)
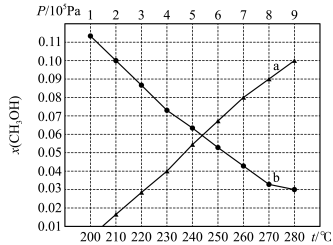
=3时,反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)在不同条件下达到平衡,设体系中甲醇物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~P、在P=5×105Pa下的x(CH3OH)~t如图所示。当CO2的平衡转化率为
CH3OH(g)+H2O(g)在不同条件下达到平衡,设体系中甲醇物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~P、在P=5×105Pa下的x(CH3OH)~t如图所示。当CO2的平衡转化率为 时,反应条件可能为
时,反应条件可能为____ 。

(1)通过离子交换膜的离子是
Ⅱ.以CO2为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二甲醚的合成塔中发生以下3个反应:
i.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=—49.01kJ·mol-1
CH3OH(g)+H2O(g) △H=—49.01kJ·mol-1ii.2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H=—24.52kJ·mol-1
CH3OCH3(g)+H2O(g) △H=—24.52kJ·mol-1iii.CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.17kJ·mol-1
CO(g)+H2O(g) △H=+41.17kJ·mol-1(2)2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)的△H=
CH3OCH3(g)+3H2O(g)的△H=(3)在压强3.0MPa、
 =4条件下,CO2的平衡转化率和产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)。
=4条件下,CO2的平衡转化率和产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的CO2占CO2消耗总量的百分比)。①当温度超过290℃,CO2的平衡转化率随温度升高而增大的原因是
②根据图中的数据计算300℃上述反应达到平衡时CH3OCH3的物质的量分数为

(4)在
 =3时,反应CO2(g)+3H2(g)
=3时,反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)在不同条件下达到平衡,设体系中甲醇物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~P、在P=5×105Pa下的x(CH3OH)~t如图所示。当CO2的平衡转化率为
CH3OH(g)+H2O(g)在不同条件下达到平衡,设体系中甲醇物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~P、在P=5×105Pa下的x(CH3OH)~t如图所示。当CO2的平衡转化率为 时,反应条件可能为
时,反应条件可能为
您最近半年使用:0次
2022-03-03更新
|
713次组卷
|
2卷引用:山东省淄博市2022届高三下学期第一次模拟考试化学试题
名校
解题方法
2 . I:磷酸氯喹是治疗新型肺炎的潜力药。磷酸是合成该药的初级原料之一,沸点高,难挥发。化学兴趣小组设计了合成磷酸的流程如图。回答下列问题
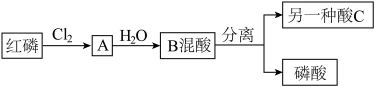
(1)将一定量的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如下图
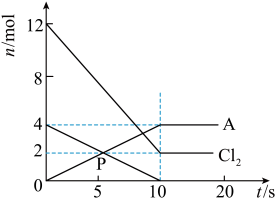
①该反应的化学方程式为___________ (A用化学式表示)
②前10s的平均反应速率v(Cl2)=_______
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是___________ (写名称)
②A与热水反应的化学方程式为____________ 。
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图______________ ,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)。
(2)该装置中负极的电极方程式为________ 。
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子__________ mol。

(1)将一定量的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如下图

①该反应的化学方程式为
②前10s的平均反应速率v(Cl2)=
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是
②A与热水反应的化学方程式为
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图
(2)该装置中负极的电极方程式为
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子
您最近半年使用:0次
名校
解题方法
3 . 任何化学反应都伴随着能量的变化,通过化学反应,化学能可转化为热能、电能等不同形式的能量。
(1)H2可用于工业合成氨气,已知拆开1molH—H、1molN≡N分别需要吸收的能量为436kJ、946kJ,形成1molN—H会放出能量391kJ,则在反应N2+3H2 2NH3中,每生成2molNH3,
2NH3中,每生成2molNH3,_______ (填“吸收”或“放出”)热量_______ kJ。当在相同的条件下向容器中充入1molN2和3molH2时,它们反应对应的热量_______ (填“大于”“等于”或“小于”)你所计算出的值。
(2)用图甲、乙所示装置进行实验,请回答下列问题。
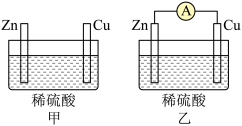
以下叙述中,正确的是_______ (填字母)。
a.甲中铜片是正极,乙中锌片是负极
b.两池中溶液的pH均增大
c.两池中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标准状况下的体积均为2.24L
(3)Mg、Al设计成如图所示原电池装置:
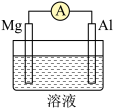
若溶液为氢氧化钠溶液,负极的电极反应为_______ 。
(4)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
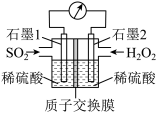
①石墨1为_______ (填“正极”或“负极”);正极的电极反应式为_______ 。
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为_______ 。
(1)H2可用于工业合成氨气,已知拆开1molH—H、1molN≡N分别需要吸收的能量为436kJ、946kJ,形成1molN—H会放出能量391kJ,则在反应N2+3H2
 2NH3中,每生成2molNH3,
2NH3中,每生成2molNH3,(2)用图甲、乙所示装置进行实验,请回答下列问题。

以下叙述中,正确的是
a.甲中铜片是正极,乙中锌片是负极
b.两池中溶液的pH均增大
c.两池中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标准状况下的体积均为2.24L
(3)Mg、Al设计成如图所示原电池装置:

若溶液为氢氧化钠溶液,负极的电极反应为
(4)电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。

①石墨1为
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
您最近半年使用:0次
2023-04-12更新
|
649次组卷
|
2卷引用:广西百色高级中学田林分校2022-2023学年高一下学期3月月考化学试题
解题方法
4 . 能量以多种不同的形式存在,并能相互转化。
I.化学反应伴随能量变化。
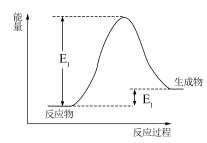
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,___________ 代表反应活化能(填“E1”或“E2”)。
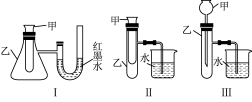
(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是___________ (填序号)。
(3)NH4HCO3和CH3COOH反应的离子方程式为___________ 。
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用 、
、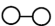 、
、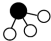 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。
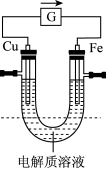
(5)电解质溶液为FeCl3时,图中箭头的方向表示___________ (填“电子”或“电流”)的流向,铁片上的电极反应式为___________ 。
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。
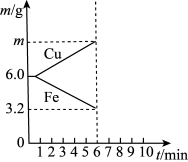
①X可以是___________ (填字母)。
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为___________ g。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,

(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是

(3)NH4HCO3和CH3COOH反应的离子方程式为
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用
 、
、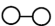 、
、 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)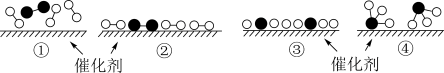
| A.反应过程存在非极性共价键的断裂和形成 |
| B.催化剂仅起到吸附N2和H2的作用,对化学反应速率没有影响 |
| C.②→③过程吸热 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。

(5)电解质溶液为FeCl3时,图中箭头的方向表示
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。

①X可以是
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为
您最近半年使用:0次
5 . γ-丁内酯为无色油状液体,高温时易分解,是重要的化工原料和医药中间体。工业利用1,4-丁二醇生产γ-丁内酯的主、副反应的化学方程式如下:
主反应: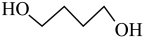 (g)
(g)
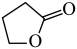 (g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
(g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
副反应: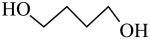 (g)
(g)
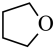 (g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(1)反应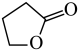 (g)+2H2(g)
(g)+2H2(g)
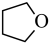 (g)+H2O(g)的△H=
(g)+H2O(g)的△H=_______ kJ•mol-1。
(2)由1,4-丁二醇合成γ-丁内酯的一种机理如图所示(“★”表示此微粒吸附在催化剂表面)
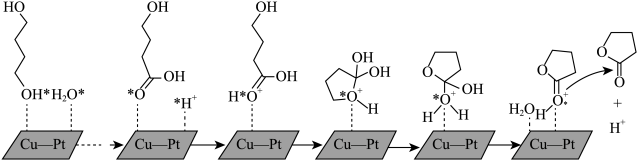
①步骤Ⅱ历程是质子化的过程,H+和氧原子间形成的作用力是______ 。
②H+在上述合成γ-丁内酯过程中的作用是_______ 。
③γ-丁内酯分子中σ键与π键数目之比为_______ 。
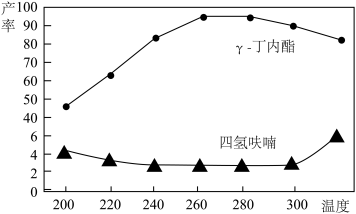
(3)将1,4-丁二醇与H2的混合气体以一定流速通过填充有催化剂的反应器,反应相同时间,测得γ-丁内酯和四氢呋喃的产率如图所示。
已知:1,4-丁二醇的沸点为228℃。
①当温度低于220℃,1,4-丁二醇的转化率较低,可能的原因是_______ 。
②当温度高于260℃,γ-丁内酯的产率下降,可能的原因是_______ 。
(4)铜基催化剂(Cu/Pt)能高效加快由1.4-丁二醇合成γ-丁内酯的合成速率,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。
①1,4-丁二醇中混有少量的1,4-丁二硫醇(HSCH2CH2CH2CH2SH)。合成时加入ZnO可有效避免铜基催化剂失活,其原理用化学反应方程式表示为_______ 。
②将失活的铜基催化剂分为两份,第一份直接在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化剂活性恢复。说明催化剂失活的另外可能的原因是______ 。
(5)含有1,4-丁二醇的强酸性污水可用“铁碳微电池”法处理,过程中两电极分别产生的Fe2+和活性氢原子(H•)都具有较高的化学活性,在厌氧条件下将1,4-丁二醇转化为甲烷,假设两电极只生成Fe2+和H•,且全部参与该转化过程,写出该过程的离子方程式:_______ 。
主反应:
 (g)
(g)
 (g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
(g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1副反应:
 (g)
(g)
 (g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1(1)反应
 (g)+2H2(g)
(g)+2H2(g)
 (g)+H2O(g)的△H=
(g)+H2O(g)的△H=(2)由1,4-丁二醇合成γ-丁内酯的一种机理如图所示(“★”表示此微粒吸附在催化剂表面)

①步骤Ⅱ历程是质子化的过程,H+和氧原子间形成的作用力是
②H+在上述合成γ-丁内酯过程中的作用是
③γ-丁内酯分子中σ键与π键数目之比为
(3)将1,4-丁二醇与H2的混合气体以一定流速通过填充有催化剂的反应器,反应相同时间,测得γ-丁内酯和四氢呋喃的产率如图所示。
已知:1,4-丁二醇的沸点为228℃。
①当温度低于220℃,1,4-丁二醇的转化率较低,可能的原因是
②当温度高于260℃,γ-丁内酯的产率下降,可能的原因是

(4)铜基催化剂(Cu/Pt)能高效加快由1.4-丁二醇合成γ-丁内酯的合成速率,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。
①1,4-丁二醇中混有少量的1,4-丁二硫醇(HSCH2CH2CH2CH2SH)。合成时加入ZnO可有效避免铜基催化剂失活,其原理用化学反应方程式表示为
②将失活的铜基催化剂分为两份,第一份直接在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化剂活性恢复。说明催化剂失活的另外可能的原因是
(5)含有1,4-丁二醇的强酸性污水可用“铁碳微电池”法处理,过程中两电极分别产生的Fe2+和活性氢原子(H•)都具有较高的化学活性,在厌氧条件下将1,4-丁二醇转化为甲烷,假设两电极只生成Fe2+和H•,且全部参与该转化过程,写出该过程的离子方程式:
您最近半年使用:0次
解题方法
6 . Ⅰ.中国积极推进低碳发展,力争在2030年前实现碳达峰,2060年前实现碳中和。
(1)已知反应 中相关的化学键键能数据如表:
中相关的化学键键能数据如表:
(已知:甲醇的结构为 ;CO的结构为
;CO的结构为 )
)
若有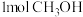 生成,反应需要
生成,反应需要___________ (填“吸收”或“放出”) ___________ kJ能量。
(2)工业上还常用 和
和 为原料合成甲醇
为原料合成甲醇 ,过程中发生如下两个反应:
,过程中发生如下两个反应:
反应Ⅰ.
反应Ⅱ.
温度为T℃时,在一个容积为2 L刚性容器中模拟工业上合成 ,往容器中通入
,往容器中通入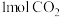 、
、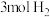 进行反应,反应过程中容器内的
进行反应,反应过程中容器内的 的物质的量随着时间变化如表所示。
的物质的量随着时间变化如表所示。
请计算反应20 min至40 min时, 的平均反应速率为
的平均反应速率为___________
Ⅱ.乙醇燃料电池可以作为笔记本电脑、汽车等的能量来源,其工作原理如图所示。请回答以下问题:
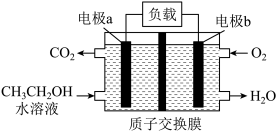
(3)电极a是___________ 极(填“正”或“负”)。
Ⅲ.对比燃料电池,简单原电池更便于我们了解电池工作原理。某同学用A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(4)装置甲溶液中的阴离子移向___________ (填“A”或“B”)极;
(5)装置乙中正极的电极反应式为___________ ;
(6)四种金属活动性由强到弱的顺序是___________ 。
(1)已知反应
 中相关的化学键键能数据如表:
中相关的化学键键能数据如表:(已知:甲醇的结构为
 ;CO的结构为
;CO的结构为 )
)| 化学键 | H-H | C-O |  | H-O | C-H |
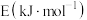 | 436 | 343 | 1076 | 465 | 413 |
若有
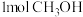 生成,反应需要
生成,反应需要(2)工业上还常用
 和
和 为原料合成甲醇
为原料合成甲醇 ,过程中发生如下两个反应:
,过程中发生如下两个反应:反应Ⅰ.

反应Ⅱ.

温度为T℃时,在一个容积为2 L刚性容器中模拟工业上合成
 ,往容器中通入
,往容器中通入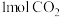 、
、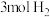 进行反应,反应过程中容器内的
进行反应,反应过程中容器内的 的物质的量随着时间变化如表所示。
的物质的量随着时间变化如表所示。| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
 的物质的量/mol 的物质的量/mol | 0 | 0.24 | 0.4 | 0.51 | 0.58 | 0.6 |
请计算反应20 min至40 min时,
 的平均反应速率为
的平均反应速率为Ⅱ.乙醇燃料电池可以作为笔记本电脑、汽车等的能量来源,其工作原理如图所示。请回答以下问题:

(3)电极a是
Ⅲ.对比燃料电池,简单原电池更便于我们了解电池工作原理。某同学用A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 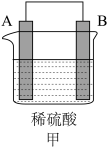 | 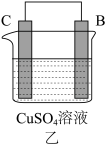 | 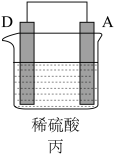 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(4)装置甲溶液中的阴离子移向
(5)装置乙中正极的电极反应式为
(6)四种金属活动性由强到弱的顺序是
您最近半年使用:0次
解题方法
7 . 2022年11月15日,二十国集团领导人第十七次峰会上,习近平主席发表题为《共迎时代挑战 共建美好未来》的重要讲话,其中提及应对气候变化挑战、向绿色低碳发展转型。回答下列问题:
(1)甲醚是一种重要的化工原料,可以用 为原料合成。已知下列反应:
为原料合成。已知下列反应:
ⅰ.
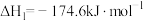
ⅱ.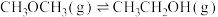
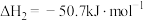
则

_______  。
。
(2)在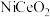 催化剂存在条件下,
催化剂存在条件下, 可转化为燃料
可转化为燃料 ,将一定比例的
,将一定比例的 、
、 混合气体通过
混合气体通过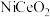 催化剂,发生下列反应:
催化剂,发生下列反应:
ⅲ.
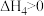
ⅳ.
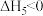
ⅴ.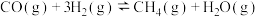
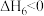
在相同时间内,测得 的转化率
的转化率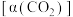 、
、 的选择性
的选择性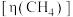 随温度的变化如图所示(不考虑催化剂失活):
随温度的变化如图所示(不考虑催化剂失活):

已知: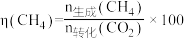 %。
%。
①对于反应ⅳ,N点正反应速率与逆反应速率比较:
_______  (填“>”“<”或“=”,下同),N点和M点正反应速率比较:
(填“>”“<”或“=”,下同),N点和M点正反应速率比较: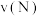
_______ 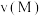 。
。
②由图像可知,升高温度, 的转化率先增大后减小,试解释产生这种变化的原因:
的转化率先增大后减小,试解释产生这种变化的原因:_______ 。
③高于400℃时,升高温度, 的选择性降低的原因是
的选择性降低的原因是_______ 。
(3)一定条件下,利用甲烷可将 还原为CO。在某密闭容器中充入
还原为CO。在某密闭容器中充入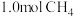 、
、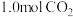 ,发生反应:
,发生反应:
 。测得
。测得 的平衡转化率随温度、压强的变化曲线如图所示:
的平衡转化率随温度、压强的变化曲线如图所示:
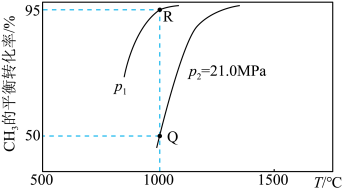

_______  (填“>”“<”或“=”)。Q点的压强平衡常数
(填“>”“<”或“=”)。Q点的压强平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)利用合适的催化剂和太阳光,以稀硫酸为电解质溶液,通过电化学装置也可将 转化为CO,装置原理如图所示:
转化为CO,装置原理如图所示:
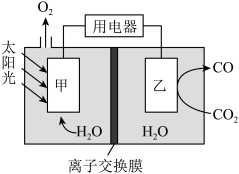
该装置中甲为_______ (填“正极”或“负极”),正极反应式为_______ 。
(1)甲醚是一种重要的化工原料,可以用
 为原料合成。已知下列反应:
为原料合成。已知下列反应:ⅰ.

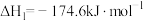
ⅱ.
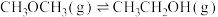
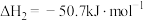
则


 。
。(2)在
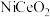 催化剂存在条件下,
催化剂存在条件下, 可转化为燃料
可转化为燃料 ,将一定比例的
,将一定比例的 、
、 混合气体通过
混合气体通过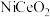 催化剂,发生下列反应:
催化剂,发生下列反应:ⅲ.

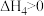
ⅳ.

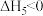
ⅴ.
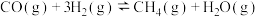
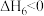
在相同时间内,测得
 的转化率
的转化率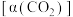 、
、 的选择性
的选择性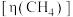 随温度的变化如图所示(不考虑催化剂失活):
随温度的变化如图所示(不考虑催化剂失活):
已知:
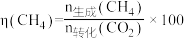 %。
%。①对于反应ⅳ,N点正反应速率与逆反应速率比较:

 (填“>”“<”或“=”,下同),N点和M点正反应速率比较:
(填“>”“<”或“=”,下同),N点和M点正反应速率比较: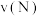
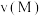 。
。②由图像可知,升高温度,
 的转化率先增大后减小,试解释产生这种变化的原因:
的转化率先增大后减小,试解释产生这种变化的原因:③高于400℃时,升高温度,
 的选择性降低的原因是
的选择性降低的原因是(3)一定条件下,利用甲烷可将
 还原为CO。在某密闭容器中充入
还原为CO。在某密闭容器中充入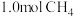 、
、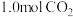 ,发生反应:
,发生反应:
 。测得
。测得 的平衡转化率随温度、压强的变化曲线如图所示:
的平衡转化率随温度、压强的变化曲线如图所示:

 (填“>”“<”或“=”)。Q点的压强平衡常数
(填“>”“<”或“=”)。Q点的压强平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)利用合适的催化剂和太阳光,以稀硫酸为电解质溶液,通过电化学装置也可将
 转化为CO,装置原理如图所示:
转化为CO,装置原理如图所示:
该装置中甲为
您最近半年使用:0次
8 . 我国科学家在“碳中和”项目上进行了如图相关深入研究,并取得一定效果。请按要求回答下列问题:
(1)将CO2转化为炭黑(C)并回收利用,反应原理如图所示。
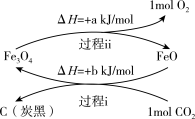
①FeO的作用是____ 。
②写出CO2转化为炭黑(C)和氧气的热化学方程式:____ 。
(2)常温下,CO2催化加氢的反应为2CO2+6H2=C2H4+4H2O △H<0。
①若该反应自发进行,反应适宜条件是____ (填“低温”或“高温”)。
②若利用该反应转化为电能,实现碳回收,负极反应物为____ 。
(3)以CO2和甲醇为原料直接合成碳酸二甲酯(CH3OCOOCH3)的反应为CO2(g)+2CH3OH(g) CH3OCOOCH3(g)+H2O(g)△H。在一定条件下,测定碳酸二甲酯的产率随温度变化的曲线如图a所示;其他条件一定时,改变压强(保持各物质气态),测定甲醇的平衡转化率随压强变化的曲线在图b(未画出)。
CH3OCOOCH3(g)+H2O(g)△H。在一定条件下,测定碳酸二甲酯的产率随温度变化的曲线如图a所示;其他条件一定时,改变压强(保持各物质气态),测定甲醇的平衡转化率随压强变化的曲线在图b(未画出)。
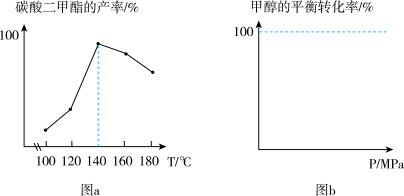
①每个碳酸二甲酯分子中最多有___ 原子共平面。
②在140~180℃之间,随着温度升高,碳酸二甲酯的产率降低,可能原因是(写一种)____ 。
③请绘制出图 b 曲线 ____ 。
(1)将CO2转化为炭黑(C)并回收利用,反应原理如图所示。

①FeO的作用是
②写出CO2转化为炭黑(C)和氧气的热化学方程式:
(2)常温下,CO2催化加氢的反应为2CO2+6H2=C2H4+4H2O △H<0。
①若该反应自发进行,反应适宜条件是
②若利用该反应转化为电能,实现碳回收,负极反应物为
(3)以CO2和甲醇为原料直接合成碳酸二甲酯(CH3OCOOCH3)的反应为CO2(g)+2CH3OH(g)
 CH3OCOOCH3(g)+H2O(g)△H。在一定条件下,测定碳酸二甲酯的产率随温度变化的曲线如图a所示;其他条件一定时,改变压强(保持各物质气态),测定甲醇的平衡转化率随压强变化的曲线在图b(未画出)。
CH3OCOOCH3(g)+H2O(g)△H。在一定条件下,测定碳酸二甲酯的产率随温度变化的曲线如图a所示;其他条件一定时,改变压强(保持各物质气态),测定甲醇的平衡转化率随压强变化的曲线在图b(未画出)。
①每个碳酸二甲酯分子中最多有
②在140~180℃之间,随着温度升高,碳酸二甲酯的产率降低,可能原因是(写一种)
③请
您最近半年使用:0次
名校
解题方法
9 . 甲醛是重要的有机合成原料,大量用于生产树脂、合成纤维、药物及涂料等。
上表为各化学键的键能(单位: 。)
。)
I.工业上常用甲醇在催化剂作用下脱氢制甲醛:
主反应: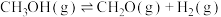
 反应①
反应①
副反应: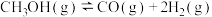
 反应②
反应②
(1)下列关于反应①说法正确的是_______ 。
A.降低体系压力对平衡有利
B.在较低温度下可以自发进行
C.应快速冷凝反应产物,以减少产物的分解
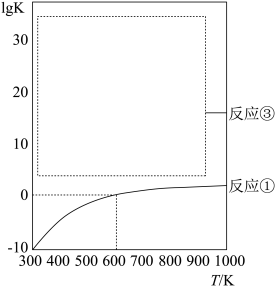
(2)制甲醛反应的lgK(K为反应平衡常数)随温度T的变化如图所示。向温度为600K,体积为1L的密闭容器中通入8.5mol甲醇(g),仅发生反应①、②,平衡后容器中含 3mol,则该条件下甲醇转化率为
3mol,则该条件下甲醇转化率为_______ ,甲醛选择性为_______ 。(选择性=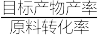 ×100%)
×100%)
II.另一种改进方法是甲醇氧化法制甲醛: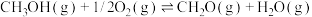
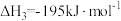 反应③
反应③
(3)试在虚框内画出反应③在300~900K内lgK随温度升高的变化趋势_____________ 。
(4)对比脱氢法,氧化法制甲醛技术的优势在于:_______ (写出两条)
(5)可用电化学甲醛传感器检测制甲醛后所排放废水废气是否合格。某传感器原理如下:在酸性介质中,以催化剂Pt和助催化剂纳米 ,将甲醛直接氧化为
,将甲醛直接氧化为 ,请写出此电极方程式:
,请写出此电极方程式:_______ ;
| 化学键 | C-H | C-O | O-H | C=O | H-H | O=O |
| 键能 | 413 | 351 | 463 | 745 | 436 | 498 |
上表为各化学键的键能(单位:
 。)
。)I.工业上常用甲醇在催化剂作用下脱氢制甲醛:
主反应:
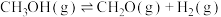
 反应①
反应①副反应:
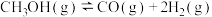
 反应②
反应②(1)下列关于反应①说法正确的是
A.降低体系压力对平衡有利
B.在较低温度下可以自发进行
C.应快速冷凝反应产物,以减少产物的分解
(2)制甲醛反应的lgK(K为反应平衡常数)随温度T的变化如图所示。向温度为600K,体积为1L的密闭容器中通入8.5mol甲醇(g),仅发生反应①、②,平衡后容器中含
 3mol,则该条件下甲醇转化率为
3mol,则该条件下甲醇转化率为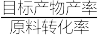 ×100%)
×100%)
II.另一种改进方法是甲醇氧化法制甲醛:
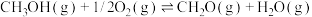
 反应③
反应③(3)试在虚框内画出反应③在300~900K内lgK随温度升高的变化趋势
(4)对比脱氢法,氧化法制甲醛技术的优势在于:
(5)可用电化学甲醛传感器检测制甲醛后所排放废水废气是否合格。某传感器原理如下:在酸性介质中,以催化剂Pt和助催化剂纳米
 ,将甲醛直接氧化为
,将甲醛直接氧化为 ,请写出此电极方程式:
,请写出此电极方程式:
您最近半年使用:0次
10 . 我国提出争取在2030年前实现“碳达峰”,2060年前实现“碳中和”,这对于改善环境,实现绿色发展至关重要。“碳中和”是指将人类经济社会活动所必需的碳排放,通过植树造林和其他人工技术或工程加以捕集利用或封存,从而使排放到大气中的二氧化碳净增量为零。下列各项措施能够有效促进“碳中和”。回答下列问题:
Ⅰ.将CO2转化为炭黑进行回收利用,反应原理如图所示。
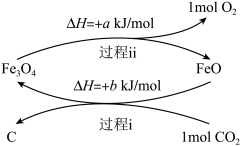
(1)从能量角度分析FeO的作用是_______ 。
(2)写出炭黑和氧气转化为CO2的热化学方程式:_______ 。
Ⅱ.以CO2和甲醇为原料直接合成碳酸二甲酯(CH3OCOOCH3)的反应为:
CO2(g)+2CH3OH(g) CH3OCOOCH3(g)+H2O(g) ΔH
CH3OCOOCH3(g)+H2O(g) ΔH
在不同的实验条件下,测定甲醇的转化率。温度的数据结果为图a,压强的数据结果在图b中未画出。
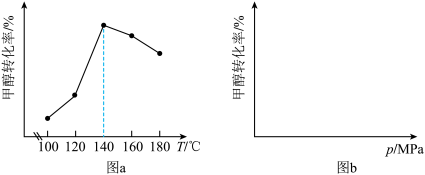
(3)该反应的ΔH_______ 0(填“>”或“<”)。
(4)在100~140℃之间,随着温度升高,甲醇转化率增大的原因是_______ 。
(5)在图b中绘制出压强和甲醇转化率之间的关系(作出趋势即可)。_______
Ⅲ.利用Al-CO2电池(工作原理如下图所示)能有效地将CO2转化成化工原料草酸铝。
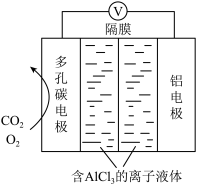
(6)电池的总反应式为_______ 。
(7)电池的正极反应式:2CO2+2e-=C2O (草酸根)正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根)正极反应过程中,O2是催化剂,催化过程可表示为:
①6O2+6e-=6O
②……
写出反应②的离子方程式:_______
Ⅰ.将CO2转化为炭黑进行回收利用,反应原理如图所示。

(1)从能量角度分析FeO的作用是
(2)写出炭黑和氧气转化为CO2的热化学方程式:
Ⅱ.以CO2和甲醇为原料直接合成碳酸二甲酯(CH3OCOOCH3)的反应为:
CO2(g)+2CH3OH(g)
 CH3OCOOCH3(g)+H2O(g) ΔH
CH3OCOOCH3(g)+H2O(g) ΔH在不同的实验条件下,测定甲醇的转化率。温度的数据结果为图a,压强的数据结果在图b中未画出。

(3)该反应的ΔH
(4)在100~140℃之间,随着温度升高,甲醇转化率增大的原因是
(5)在图b中绘制出压强和甲醇转化率之间的关系(作出趋势即可)。
Ⅲ.利用Al-CO2电池(工作原理如下图所示)能有效地将CO2转化成化工原料草酸铝。

(6)电池的总反应式为
(7)电池的正极反应式:2CO2+2e-=C2O
 (草酸根)正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根)正极反应过程中,O2是催化剂,催化过程可表示为:①6O2+6e-=6O

②……
写出反应②的离子方程式:
您最近半年使用:0次



