解题方法
1 . 锂离子浓差电池工作原理如图所示。电池总反应为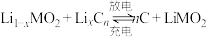 。下列说法正确的是
。下列说法正确的是
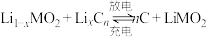 。下列说法正确的是
。下列说法正确的是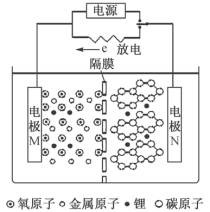
| A.充电时,电极N为电池的阳极 |
| B.该电池隔膜为阴离子交换膜 |
C.放电时,负极电极反应式为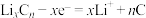 |
D.放电时,若导线有4 电子通过,则正极质量增加14g 电子通过,则正极质量增加14g |
您最近半年使用:0次
解题方法
2 . 我国某大学科研团队通过超快电脉冲热还原法开发了一种新型碳载钌镍合金纳米催化剂(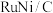 ),并基于此催化剂制备出一种极具竞争力的高能量镍氢气
),并基于此催化剂制备出一种极具竞争力的高能量镍氢气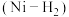 电池,其工作原理如图所示。下列说法错误的是
电池,其工作原理如图所示。下列说法错误的是
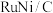 ),并基于此催化剂制备出一种极具竞争力的高能量镍氢气
),并基于此催化剂制备出一种极具竞争力的高能量镍氢气 电池,其工作原理如图所示。下列说法错误的是
电池,其工作原理如图所示。下列说法错误的是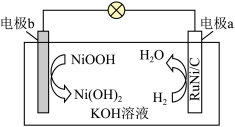
A.放电时, 向电极 向电极 移动 移动 |
B.放电一段时间后, 溶液的浓度增大 溶液的浓度增大 |
C.放电时, |
D.外电路中每转移 ,理论上电极 ,理论上电极 上消耗 上消耗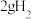 |
您最近半年使用:0次
解题方法
3 . 锌-空气电池被认为是替代锂离子电池、满足电动汽车爆炸性需求的下一代候选电池。用光照充电的锌-空气电池的工作原理如图所示。光照时,光电极 (空穴),驱动阴极和阳极反应。下列叙述不正确的是
(空穴),驱动阴极和阳极反应。下列叙述不正确的是
 (空穴),驱动阴极和阳极反应。下列叙述不正确的是
(空穴),驱动阴极和阳极反应。下列叙述不正确的是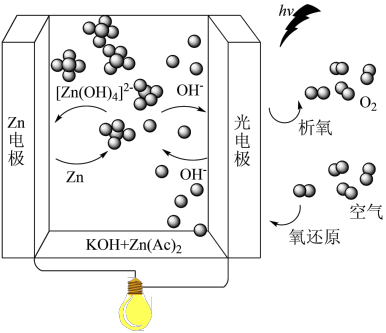
A.放电时, 向光电极迁移 向光电极迁移 | B.充电时的阳极反应为 |
C.放电时,光电子经电解液向 极移动 极移动 | D. 是配离子,配位数是4 是配离子,配位数是4 |
您最近半年使用:0次
4 . 人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,完成下面题目。
(1) 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移
,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_____________ mol电子。
(2)将铝片和铜片用导线相连,插入浓硝酸中,形成原电池,其中正极为_____________ (填“铜”或“铝”,下同),若将其插入烧碱溶液中,形成原电池,负极为_____________ 。
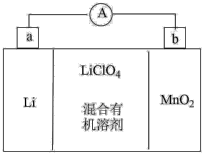
(3)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质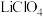 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成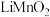 。
。_____________ (填字母,下同)极流向_____________ 极。
②电池正极反应式为___________________ ,每转移2mol电子,生成__________ g 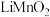 。
。
③不能用水代替电池中的混合有机溶剂,原因是__________________________ 。
④ 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为_________ 。
(4)在新能源体系下,氢能被视为与电能互补的优质二次能源。氢燃料电池能量转换率远高于氢气直接燃烧。
①碱性氢氧燃料电池工作时,负极反应式为____________________ 。
②氢氧熔融碳酸盐燃料电池是一种以熔融态碳酸盐为电解质的电池,其工作原理如图所示,有关该电池说法正确的是_____________ (填字母)。
B.该电池可利用工厂中排出的 ,减少温室气体的排放
,减少温室气体的排放
C.电子流向:氢电极—负载—氧电极—熔融碳酸盐—氢电极
D.电池工作时,外电路中流过0.2mol电子,消耗1.6g
(1)
 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移
,若将此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移(2)将铝片和铜片用导线相连,插入浓硝酸中,形成原电池,其中正极为
(3)锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质
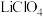 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成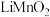 。
。
②电池正极反应式为
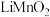 。
。③不能用水代替电池中的混合有机溶剂,原因是
④
 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为(4)在新能源体系下,氢能被视为与电能互补的优质二次能源。氢燃料电池能量转换率远高于氢气直接燃烧。
①碱性氢氧燃料电池工作时,负极反应式为
②氢氧熔融碳酸盐燃料电池是一种以熔融态碳酸盐为电解质的电池,其工作原理如图所示,有关该电池说法正确的是
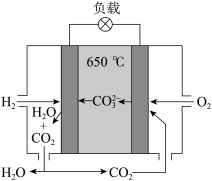
B.该电池可利用工厂中排出的
 ,减少温室气体的排放
,减少温室气体的排放C.电子流向:氢电极—负载—氧电极—熔融碳酸盐—氢电极
D.电池工作时,外电路中流过0.2mol电子,消耗1.6g

您最近半年使用:0次
名校
解题方法
5 . 形形色色的电池在生产生活中有着重要的作用,请回答下列问题:
(1)碱性锌锰电池适合需要大电流供电的设备使用如照相机、野外摄像机、无线电控制的航模与海模、电动工具、电动玩具、收录机等,其结构如图所示,总反应为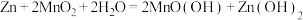 。该电池的正极为
。该电池的正极为__________ (填“Zn”或“ ”),其电极反应式为
”),其电极反应式为__________ 。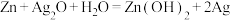 ,放电时,
,放电时, 发生
发生__________ (填“氧化”或“还原”)反应。一种废旧纽扣电池回收工艺流程如图所示,稀硫酸溶解时需要在无氧环境下进行,原因是__________ ;加入稀硝酸溶解银时,产物为 、NO和
、NO和 ,该反应的化学方程式为
,该反应的化学方程式为__________ ,调浆后,加入葡萄糖制备银粉,葡萄糖的作用为__________ 。__________ ,电路中每转移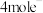 ,两极共消耗
,两极共消耗__________ L(换算成标准状况下)气体。
(1)碱性锌锰电池适合需要大电流供电的设备使用如照相机、野外摄像机、无线电控制的航模与海模、电动工具、电动玩具、收录机等,其结构如图所示,总反应为
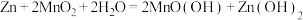 。该电池的正极为
。该电池的正极为 ”),其电极反应式为
”),其电极反应式为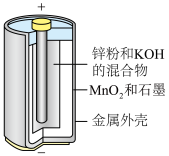
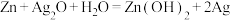 ,放电时,
,放电时, 发生
发生 、NO和
、NO和 ,该反应的化学方程式为
,该反应的化学方程式为
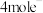 ,两极共消耗
,两极共消耗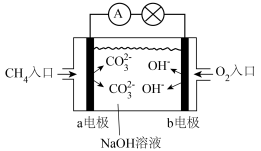
您最近半年使用:0次
2024-04-21更新
|
387次组卷
|
2卷引用:河北省沧州市沧县中学等校2023-2024学年高一下学期3月联考化学试题
6 . 如图所示,把a、b插入c的溶液中,闭合开关后电流表的指针会发生偏转,且b上有气泡产生。则a、b、c可能是以下哪组物质

| A.a—Fe、b—Cu、c—稀硫酸 | B.a—Mg、b—Al、c—NaOH溶液 |
| C.a—石墨、b—Zn、c—稀硫酸 | D.a—Cu、b—Ag、c—酒精 |
您最近半年使用:0次
名校
解题方法
7 . 化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据原电池的本质判断,下列化学(或离子)方程式正确,且能设计成原电池的是___________。
(2)利用反应“ ”设计一个原电池,正极的电极反应式:
”设计一个原电池,正极的电极反应式:___________ 。
(3)以Pt为电极的氢氧燃料电池的工作原理示意图如图所示,稀 为电解质溶液。
为电解质溶液。___________ 极,发生___________ 反应(“氧化”或“还原”),写出b极的电极反应式___________ 。
②该电池提供 ,理论上消耗的氢气在标准状况下的体积为
,理论上消耗的氢气在标准状况下的体积为___________ L。
(1)根据原电池的本质判断,下列化学(或离子)方程式正确,且能设计成原电池的是___________。
A.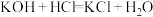 | B.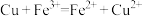 |
C.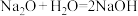 | D.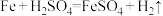 |
(2)利用反应“
 ”设计一个原电池,正极的电极反应式:
”设计一个原电池,正极的电极反应式:(3)以Pt为电极的氢氧燃料电池的工作原理示意图如图所示,稀
 为电解质溶液。
为电解质溶液。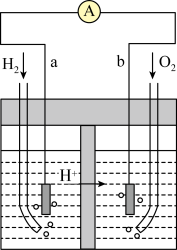
②该电池提供
 ,理论上消耗的氢气在标准状况下的体积为
,理论上消耗的氢气在标准状况下的体积为
您最近半年使用:0次
名校
解题方法
8 . 如图所示,电流计G发生偏转,同时A极逐渐变细,B极逐渐变粗,C为电解质溶液,则A、B、C应是下列各组中的
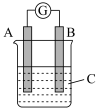
| A.A是Zn、B是Zn、C为稀硫酸 | B.A是Cu、B是Ag、C为稀硫酸 |
C.A是Fe、B是Ag、C为 溶液 溶液 | D.A是Ag、B是Fe、C为 溶液 溶液 |
您最近半年使用:0次
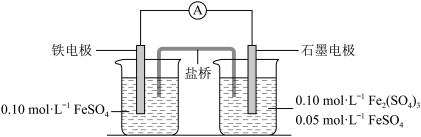
9 . 利用下图电池装置可验证不同化合价铁元素的相关性质。 (如下表)应尽可能地相近;两烧杯中溶液体积相等。
(如下表)应尽可能地相近;两烧杯中溶液体积相等。
下列说法正确的是
 (如下表)应尽可能地相近;两烧杯中溶液体积相等。
(如下表)应尽可能地相近;两烧杯中溶液体积相等。| 离子 | Li+ | Na+ | Ca2+ | K+ |  |  | Cl- |  |
 | 4.07 | 5.19 | 6.59 | 7.62 | 4.61 | 7.40 | 7.91 | 8.27 |
| A.根据上表数据,盐桥中应选择KNO3作为电解质 |
B.石墨电极上对应的电极反应式为: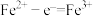 |
C.反应一段时间后,当右池中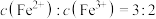 时,左池中 时,左池中 |
| D.盐桥中的阴离子进入石墨电极一侧溶液中 |
您最近半年使用:0次
名校
10 . 任何化学反应都伴随着能量的变化,通过化学反应化学能可转化为热能、电能等不同形式的能量。
(1) 可用于工业合成氨气,已知常温常压下拆开1mol
可用于工业合成氨气,已知常温常压下拆开1mol 键、1mol
键、1mol 键分别需要吸收的能量为436kJ、946kJ,形成1mol
键分别需要吸收的能量为436kJ、946kJ,形成1mol 键会放出391kJ能量。
键会放出391kJ能量。
根据上述数据判断工业合成氨的反应是______ (填“吸热”或“放热”)反应;
若消耗1mol 和3mol
和3mol ,理论上放出或吸收热量为
,理论上放出或吸收热量为 ,则
,则 为
为______ kJ;
(2)用图甲、乙所示装置进行实验,以下叙述中,正确的是___。
b.两烧杯中溶液的 均增大
均增大
c.两烧杯中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标况下的体积均为2.24L
(3)某同学依据氧化还原反应: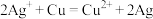 设计的原电池如下图所示:
设计的原电池如下图所示:______ ,发生的电极反应为______ 。
当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是______ 。
(1)
 可用于工业合成氨气,已知常温常压下拆开1mol
可用于工业合成氨气,已知常温常压下拆开1mol 键、1mol
键、1mol 键分别需要吸收的能量为436kJ、946kJ,形成1mol
键分别需要吸收的能量为436kJ、946kJ,形成1mol 键会放出391kJ能量。
键会放出391kJ能量。根据上述数据判断工业合成氨的反应是
若消耗1mol
 和3mol
和3mol ,理论上放出或吸收热量为
,理论上放出或吸收热量为 ,则
,则 为
为(2)用图甲、乙所示装置进行实验,以下叙述中,正确的是___。

b.两烧杯中溶液的
 均增大
均增大c.两烧杯中铜片表面均有气泡产生
d.若反应过程中有0.2mol电子转移,生成的氢气在标况下的体积均为2.24L
(3)某同学依据氧化还原反应:
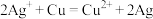 设计的原电池如下图所示:
设计的原电池如下图所示: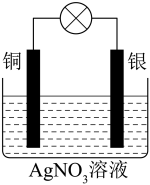
当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移的电子数目是
您最近半年使用:0次



