名校
1 . 如图是一个化学过程的示意图。已知甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O请回答:
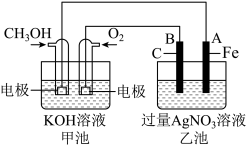
(1)甲池是_______ (填“原电池”或“电解池”),通入O2的电极作为_______ 极,该电极反应式为_______ 。
(2)乙池是_______ (填“原电池”或“电解池”),B电极名称为_______ 极,电极反应式为_______ 。
(3)甲池中溶液的pH_______ (填“增大”、“减小”或“不变”);乙池中溶液的pH_______ (填“增大”、“减小”或“不变”)。
(4)当乙池中A(Fe)极的质量增加5.40g时,电路中转移电子的物质的量是_______ mol,甲池中理论上消耗O2_______ mL(标准状况下)。

(1)甲池是
(2)乙池是
(3)甲池中溶液的pH
(4)当乙池中A(Fe)极的质量增加5.40g时,电路中转移电子的物质的量是
您最近半年使用:0次
名校
解题方法
2 . 光催化微生物燃料电池的工作原理如图所示:

已知:电极a在光激发条件下会产生电子(e-)—空穴(h+)。下列说法错误的是

已知:电极a在光激发条件下会产生电子(e-)—空穴(h+)。下列说法错误的是
| A.电极电势:电极a>电极b |
| B.电极b发生的电极反应式为(C6H10O5)n-24e-+7H2O=6CO2↑+24H+ |
| C.光激发时,光生电子会与O2结合,光生空穴会与电极b产生的电子结合 |
| D.电池工作一段时间后,右侧溶液pH保持不变(不考虑CO2的溶解) |
您最近半年使用:0次
2023-06-07更新
|
394次组卷
|
3卷引用:海南省海南中学2022-2023学年高二下学期第二次月考化学试题
海南省海南中学2022-2023学年高二下学期第二次月考化学试题安徽省芜湖市第一中学2023届高三下学期最后一卷理科综合化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)
3 . 有甲乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/L的硫酸溶液,乙同学将电极放入6mol/L的氢氧化钠溶液中,如图所示:
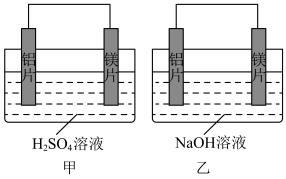
(1)写出甲电池中正极的电极反应式:_______ ;在标准状况下,正极产生33.6L气体得_______ mol电子。
(2)乙中负极为_______ ,总反应的离子方程式:_______ 。
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则负极材料的金属应比正极材料的金属活泼”,则甲会判断出_______ 活动性更强,而乙会判断出_______ 活动性更强。(填写元素符号)
(4)由此实验,可得到如下哪些正确结论_______。

(1)写出甲电池中正极的电极反应式:
(2)乙中负极为
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则负极材料的金属应比正极材料的金属活泼”,则甲会判断出
(4)由此实验,可得到如下哪些正确结论_______。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属性不一定比铝的强 |
| C.该实验说明金属活动性顺序表已过时,已没有利用价值 |
| D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析 |
您最近半年使用:0次
名校
4 . 锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O=2Zn(OH) 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.充电时,电解质溶液中K+向阳极移动 |
| B.充电时,电解质溶液中c(OH-)逐渐减小 |
| C.放电时,负极反应为:Zn+2OH–−2e–=Zn(OH)2 |
| D.放电时,电路中通过4mol电子,消耗氧气22.4L(标准状况) |
您最近半年使用:0次
2023-06-07更新
|
520次组卷
|
4卷引用:广东省华南师范大学附属中学2022-2023学年高二上学期1月期末化学试题
名校
解题方法
5 . pH计的工作原理(如图所示)是通过测定电池电动势E(即玻璃电极和参比电极的电势差)而确定待测溶液的pH。电池电动势E与待测溶液pH关系为:E=0.059pH+K(E的单位为V,K为常数)。下 列说法正确的是
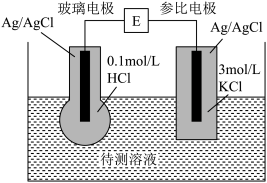

| A.参比电极一定是正极 |
| B.一定温度下,电池电动势越小,待测液中c(H+ )越大 |
| C.pH计工作时,若玻璃电极电势比参比电极低,则玻璃电极反应上每得lmol 电子,生成1molAg单质 |
| D.pH计可以长期浸泡在碱性缓冲液中 |
您最近半年使用:0次
解题方法
6 . 过氧化氢溶液可用于医用伤口消毒、环境消毒和食品消毒。科技工作者研究电化学时,采用空气和水通过电解法可制备H2O2,其装置如图所示,乙中管道将d极产生的气体送至c极。已知溶液的pH过高时H2O2会分解。下列有关说法正确的是
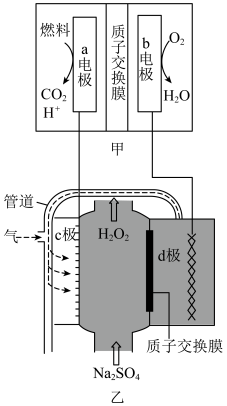

| A.甲为原电池装置,其中的b电极是负极 |
| B.乙中c极为阴极,电极反应为O2+2e-+2H2O= H2O2 +2OH- |
C.若甲中燃料是甲烷,a电极反应为CH4-8e-+ 10OH-= +7H2O +7H2O |
| D.反应进行一段时间后,乙中d极附近溶液pH明显增大 |
您最近半年使用:0次
解题方法
7 . 某同学设计的原电池装置如图,下列说法错误的是
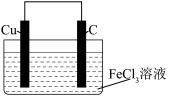

A.电池总反应为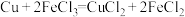 | B.Cu极为负极 |
C. 移向Cu极 移向Cu极 | D.电流从C极流向Cu极 |
您最近半年使用:0次
2023-06-05更新
|
244次组卷
|
2卷引用:2022年夏季山东普通高中学业水平考试化学试题
8 . 我国某科研机构设计下图装置,利用K2Cr2O7实现含苯酚废水的有效处理(达到可排放标准 ) ,一段时间后,中间室中NaCl溶液的浓度减小。下列说法不正确 的是
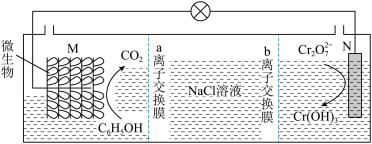

| A.该装置不适合在高温下处理含苯酚废水 |
| B.M电极的的电极反应式为:C6H5OH-28e-+11H2O=6CO2↑+28H+ |
| C.a为阳离子交换膜,b为阴离子交换膜 |
D.N电极反应式为:Cr2O +6e-+8H+=2Cr(OH)3↓+H2O +6e-+8H+=2Cr(OH)3↓+H2O |
您最近半年使用:0次
名校
9 . 某原电池装置如图所示,装置中盐桥的作用是使整个装置形成一个闭合回路,电解质溶液足量,闭合开关,观察到电流计指针发生偏转,回答下列问题。
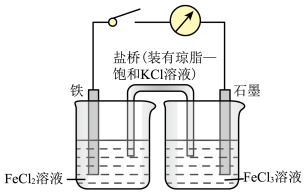
(1)该原电池工作过程中,电池的负极上的电极反应式为___________ ,石墨电极上发生了___________ (填“氧化”或“还原”)反应。
(2)该原电池工作时,下列说法正确的是___________(填标号)。
(3)当铁电极减少 时,外电路中转移的电子数目为
时,外电路中转移的电子数目为___________  ,右侧烧杯中
,右侧烧杯中 的物质的量改变了
的物质的量改变了___________  。
。
(4)原电池工作时能量转化形式为_______ ,根据原电池形成条件,下列反应理论上可以设计成原电池的是_______ (填标号)。
A. 与
与 的反应 B.
的反应 B. 和
和 的反应
的反应
C. 和
和 的反应 D.
的反应 D. 和
和 的反应
的反应
(5)以 为原理设计燃枓电池,其利用率高,装置如图所示。
为原理设计燃枓电池,其利用率高,装置如图所示。
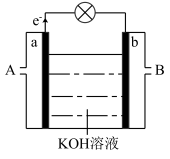
①A处加入的是___________ ,a处的电极反应式是_______ 。
②当消耗标准状况下3.36L 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是___________ mol。

(1)该原电池工作过程中,电池的负极上的电极反应式为
(2)该原电池工作时,下列说法正确的是___________(填标号)。
A.电子移动的方向:石墨 铁 铁 |
B.盐桥中的 会向右侧烧杯移动 会向右侧烧杯移动 |
C. 溶液的颜色会逐渐变浅 溶液的颜色会逐渐变浅 |
D.将 盐桥换成 盐桥换成 盐桥,该装置不能长时间正常工作 盐桥,该装置不能长时间正常工作 |
 时,外电路中转移的电子数目为
时,外电路中转移的电子数目为 ,右侧烧杯中
,右侧烧杯中 的物质的量改变了
的物质的量改变了 。
。(4)原电池工作时能量转化形式为
A.
 与
与 的反应 B.
的反应 B. 和
和 的反应
的反应C.
 和
和 的反应 D.
的反应 D. 和
和 的反应
的反应(5)以
 为原理设计燃枓电池,其利用率高,装置如图所示。
为原理设计燃枓电池,其利用率高,装置如图所示。
①A处加入的是
②当消耗标准状况下3.36L
 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是
您最近半年使用:0次
解题方法
10 . I.化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列△H表示物质标准燃烧热的是_____ ;表示中和反应反应热的是_____ 。(填“△H1”、“△H2”、“△H3”等)
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+ O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
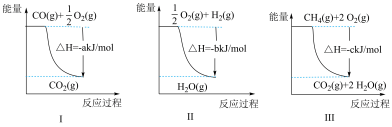
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g) CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=______ (用含a、b、c的式子表示)。
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
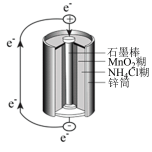
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少______ g。
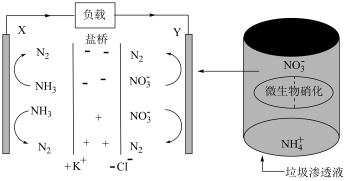
(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:______ 。
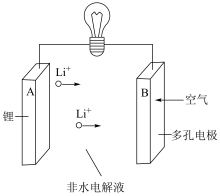
“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是______ 极(填“A”或“B”)。
(1)下列△H表示物质标准燃烧热的是
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+
 O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少

(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:

“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2
 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
您最近半年使用:0次



