1 . 在“双碳”目标的推动下,回收利用 成为研究热点,如利用
成为研究热点,如利用 合成甲醛。
合成甲醛。
(1)已知:①
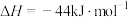 ;
;
②常温常压下, 、
、 的燃烧热[在
的燃烧热[在 时,
时, 纯物质完全燃烧生成指定产物时所放出的热量,称为该物质的燃烧热。碳元素变为
纯物质完全燃烧生成指定产物时所放出的热量,称为该物质的燃烧热。碳元素变为 ,氢元素变为
,氢元素变为 ]如表:
]如表:
则 制取甲醛的热化学方程式为
制取甲醛的热化学方程式为

___________  。若该反应有
。若该反应有 转移,则需要
转移,则需要___________ (填“吸收”或“释放”)___________ kJ能量。
(2)甲醛是纺织品业、木材加工业等重要的化工原料。居室中某些材料会向空气中散发甲醛,而利用光触媒可以解决这一问题。其原理如图。
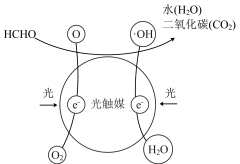
①用反应式表示 在光触媒表面的变化:
在光触媒表面的变化:___________ 。
②写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
(3)我国某科研团队开发出以铜纳米片阵列电极为高活性阳极,实现甲醛燃料电池直接在发电的同时产生甲酸盐(原理如图)。已知双极板是燃料电池的重要部件之一、其能分隔燃料与氧化剂,阻止气体透过;收集、传导电流,可将气体均匀分配到电极的反应层进行电极反应并排出热量。
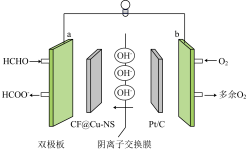
①a极为电池的___________ (填“正”或“负”)极,电极反应式为___________ 。
②电池工作时, 向
向___________ (填“a”或“b”)极移动。
③若以该电池为电源实现在铁器上镀铜,则纯铜应连接___________ (填“a”或“b”)极。
 成为研究热点,如利用
成为研究热点,如利用 合成甲醛。
合成甲醛。(1)已知:①

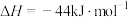 ;
;②常温常压下,
 、
、 的燃烧热[在
的燃烧热[在 时,
时, 纯物质完全燃烧生成指定产物时所放出的热量,称为该物质的燃烧热。碳元素变为
纯物质完全燃烧生成指定产物时所放出的热量,称为该物质的燃烧热。碳元素变为 ,氢元素变为
,氢元素变为 ]如表:
]如表:| 物质 | 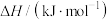 |
 | 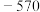 |
 |  |
 制取甲醛的热化学方程式为
制取甲醛的热化学方程式为

 。若该反应有
。若该反应有 转移,则需要
转移,则需要(2)甲醛是纺织品业、木材加工业等重要的化工原料。居室中某些材料会向空气中散发甲醛,而利用光触媒可以解决这一问题。其原理如图。

①用反应式表示
 在光触媒表面的变化:
在光触媒表面的变化:②写出
 与
与 反应的化学方程式:
反应的化学方程式:(3)我国某科研团队开发出以铜纳米片阵列电极为高活性阳极,实现甲醛燃料电池直接在发电的同时产生甲酸盐(原理如图)。已知双极板是燃料电池的重要部件之一、其能分隔燃料与氧化剂,阻止气体透过;收集、传导电流,可将气体均匀分配到电极的反应层进行电极反应并排出热量。

①a极为电池的
②电池工作时,
 向
向③若以该电池为电源实现在铁器上镀铜,则纯铜应连接
您最近一年使用:0次
名校
解题方法
2 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
(1)工业合成氨反应:N2(g)+3H2(g) 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量_____ (填“大于”“小于”或“等于”)920kJ。
(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成10molNH3,用N2表示的化学反应速率为_____ 。
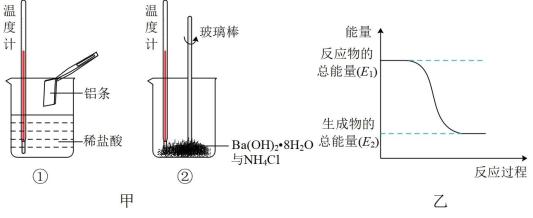
(3)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度______ (填“升高”或“降低”)。反应过程_____ (填“①”或“②”)的能量变化可用图乙表示。
(4)如图为原电池装置示意图。A为Cu,B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2。
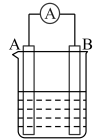
①写出A的电极名称______ 。
②B电极反应式:______ 。
③该电池在工作时,溶液中Fe3+向______ (填“A”、“B”)移动,A电极的质量将______ (填“增加”、“减小”或“不变”)。
(1)工业合成氨反应:N2(g)+3H2(g)
 2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量
2NH3(g)是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2(g)完全反应生成NH3(g)可放出92kJ热量。如果将10molN2(g)和足量H2(g)混合,使其充分反应,放出的热量(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成10molNH3,用N2表示的化学反应速率为
(3)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度

(4)如图为原电池装置示意图。A为Cu,B为石墨,电解质为FeCl3溶液,工作时的总反应为2FeCl3+Cu=2FeCl2+CuCl2。

①写出A的电极名称
②B电极反应式:
③该电池在工作时,溶液中Fe3+向
您最近一年使用:0次
3 . 某小组研究化学反应中的能量变化,进行了如下实验。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L﹣1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,Cu片表面无明显变化。Zn片与稀硫酸反应的离子方程式为_______ 。
(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L﹣1稀硫酸的烧杯中。
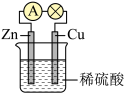
锌片上电极反应式为___________ ;铜片上能够观察到的现象是___________ ;电子流向 ___________ 填“锌片−导线−铜片”或“铜片−导线−锌片”)
(3)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是___________ 。
(1)实验 I:将Zn片和Cu片分别插入盛有50mL 2mol•L﹣1稀硫酸的烧杯中。

观察到Zn片表面产生气泡,Cu片表面无明显变化。Zn片与稀硫酸反应的离子方程式为
(2)实验Ⅱ:用导线将电流表、小灯泡与Zn片、Cu片相连接,插入盛有50mL2mol•L﹣1稀硫酸的烧杯中。

锌片上电极反应式为
(3)将Zn片和Cu片换成Fe片和石墨棒,重复实验Ⅱ,判断电流表指针是否发生偏转。若不偏转,说明理由;若偏转,写出Fe片表面发生的电极反应式,理由或电极反应式是
您最近一年使用:0次
4 .  的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝
(1)汽车尾气中 生成过程中的能量变化如图所示。
生成过程中的能量变化如图所示。 和
和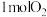 完全反应生成NO会吸收
完全反应生成NO会吸收___________  的能量。
的能量。
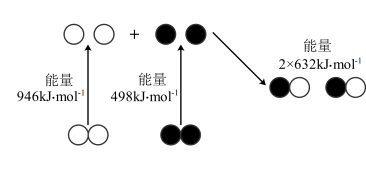
(2) 催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同
催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氨率如图所示,当温度为
对应的脱氨率如图所示,当温度为___________ ℃,
___________ ,脱氮效果最佳。
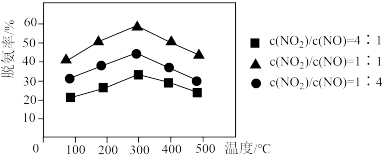
Ⅱ.脱碳
(3)一定条件下 和
和 反应合成
反应合成 进行脱碳处理,其方程式为:
进行脱碳处理,其方程式为: 。在2L密闭容器中,该反应过程中的部分数据如下表:
。在2L密闭容器中,该反应过程中的部分数据如下表:
①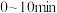 ,以
,以 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为___________  。
。
②下列情况能说明该反应达到化学平衡状态的是___________ 。
A. 浓度之比为
浓度之比为 B.该密闭容器内压强保持不变
B.该密闭容器内压强保持不变
C.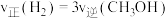 D.该密闭容器内混合气体的密度保持不变
D.该密闭容器内混合气体的密度保持不变
③平衡时, 的体积分数为
的体积分数为___________ (结果保留三位有效数字)。
Ⅲ.脱硫
(4)将 转化为重要的化工原料
转化为重要的化工原料 进行脱硫的原理示意图。
进行脱硫的原理示意图。
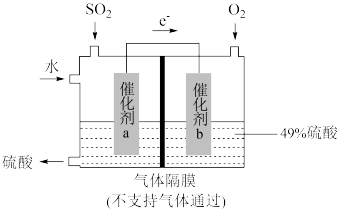
催化剂a表面的电极反应式为___________ ,若得到的硫酸质量分数仍为49%,则理论上参加反应的 与加入的
与加入的 的物质的量之比为
的物质的量之比为___________ 。
 的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
的排放与燃烧化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。Ⅰ.脱硝
(1)汽车尾气中
 生成过程中的能量变化如图所示。
生成过程中的能量变化如图所示。 和
和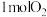 完全反应生成NO会吸收
完全反应生成NO会吸收 的能量。
的能量。
(2)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同
催化还原氮氧化物(SCR)技术是目前应用最广泛的脱硝技术,用Fe做催化剂时,在氨气足量的情况下,不同 对应的脱氨率如图所示,当温度为
对应的脱氨率如图所示,当温度为

Ⅱ.脱碳
(3)一定条件下
 和
和 反应合成
反应合成 进行脱碳处理,其方程式为:
进行脱碳处理,其方程式为: 。在2L密闭容器中,该反应过程中的部分数据如下表:
。在2L密闭容器中,该反应过程中的部分数据如下表:反应时间/ | 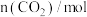 | 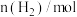 | 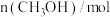 | 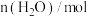 |
| 0 | 3 | 9 | 0 | 0 |
| 10 | 6 | |||
| 20 | 1.5 | |||
| 30 | 1.5 |
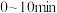 ,以
,以 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为 。
。②下列情况能说明该反应达到化学平衡状态的是
A.
 浓度之比为
浓度之比为 B.该密闭容器内压强保持不变
B.该密闭容器内压强保持不变C.
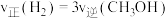 D.该密闭容器内混合气体的密度保持不变
D.该密闭容器内混合气体的密度保持不变③平衡时,
 的体积分数为
的体积分数为Ⅲ.脱硫
(4)将
 转化为重要的化工原料
转化为重要的化工原料 进行脱硫的原理示意图。
进行脱硫的原理示意图。
催化剂a表面的电极反应式为
 与加入的
与加入的 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
5 . 填空。
(1)某温度时,在容积为2L的密闭容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。
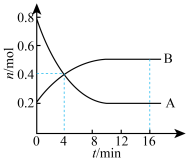
①该反应的化学方程式为___________ 。
②该反应进行到4min时,B的平均反应速率为___________ ,A的转化率为___________ 。
③4min时,反应是否达到平衡?___________ (填“是”或“否”);16min时,正反应速率___________ 逆反应速率(填“>”“<”或“=”)。
(2)如图所示。
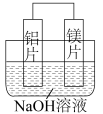
负极为___________ (填“铝片”或“镁片”)写出其电极反应式:___________ 。
(3)根据下列信息判断氢气燃烧生成水时的热量变化:
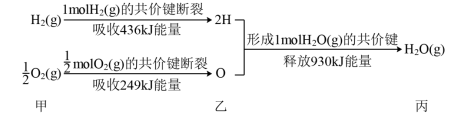
①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为___________ kJ;
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:___________ 。
(1)某温度时,在容积为2L的密闭容器中发生A、B两种物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。请分析图中数据,回答下列问题。

①该反应的化学方程式为
②该反应进行到4min时,B的平均反应速率为
③4min时,反应是否达到平衡?
(2)如图所示。

负极为
(3)根据下列信息判断氢气燃烧生成水时的热量变化:

①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:
您最近一年使用:0次
名校
解题方法
6 . 化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d.铜溶于浓硝酸 e.氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)H2O2分解时的能量变化关系如图所示,则H2O2分解反应为_______ 反应(选填:吸热、放热)。
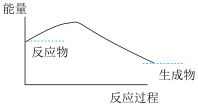
查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和___________ 。
(3)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图所示。
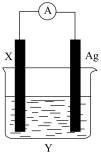
①电极X的材料是___________ 。
②X电极的电极反应式为___________ ;
Ag电极上发生的是___________ (填“氧化”或“还原”)反应。
③当有2.8 g铁溶解时,Ag电极增重___________ g。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.浓硫酸稀释 c.碳酸氢钠固体溶于盐酸
d.铜溶于浓硝酸 e.氯化铵固体与氢氧化钡晶体混合搅拌 f.过氧化钠溶于水
(2)H2O2分解时的能量变化关系如图所示,则H2O2分解反应为

查阅资料得知:将作为催化剂的Fe2(SO4)3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是:2Fe3++H2O2=2Fe2++O2↑+2H+和
(3)依据氧化还原反应Fe+2Ag+=Fe2++2Ag设计的原电池如图所示。

①电极X的材料是
②X电极的电极反应式为
Ag电极上发生的是
③当有2.8 g铁溶解时,Ag电极增重
您最近一年使用:0次
解题方法
7 . I.化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列△H表示物质标准燃烧热的是_____ ;表示中和反应反应热的是_____ 。(填“△H1”、“△H2”、“△H3”等)
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+ O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
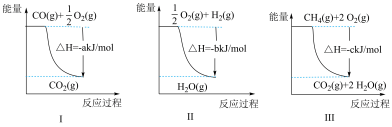
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g) CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=______ (用含a、b、c的式子表示)。
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
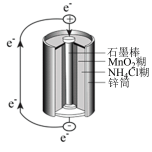
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少______ g。
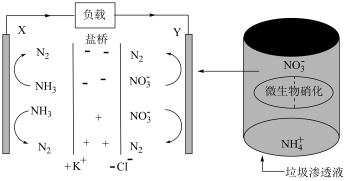
(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:______ 。
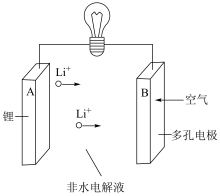
“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是______ 极(填“A”或“B”)。
(1)下列△H表示物质标准燃烧热的是
A.2H2(g)+O2(g)=2H2O(l) △H1
B.C(s)+
 O2(g)=CO(g) △H2=-Q1kJ•mol-1
O2(g)=CO(g) △H2=-Q1kJ•mol-1C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3
D.C(s)+O2(g)=CO2(g) △H4=-Q2kJ•mol-1
E.Ba(OH)2(aq)+H2SO4(aq)=BaSO4(aq)+2H2O(l) △H5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H6
(2)工业上可通过天然气跟水蒸气反应制取H2,有关反应的能量变化如图所示,则该反应的CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=
CO(g)+3H2(g) △H=
Ⅱ.电池的研发与生产、生活、军事等领域的发展密切相关。
(3)锌锰干电池是最早使用的化学电池,其基本构造如图所示:电路中每通过0.4mole-,负极质量减少

(4)一种利用垃圾渗透液实现发电装置示意图如图,当该装置工作时,Y极发生的电极反应式为:

“锂-空气”电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(5)“锂-空气”电池的反应原理可表示为:2Li+O2
 Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
Li2O2,其放电时的工作原理如图所示:电池工作时,发生氧化反应的是
您最近一年使用:0次
解题方法
8 . 已知在1×105Pa,298 K时断裂1 mol H—H键吸收的能量为436kJ ,断裂l mol N—H键吸收的能量为391kJ,断裂1 mol N≡N键吸收的能量是945kJ。
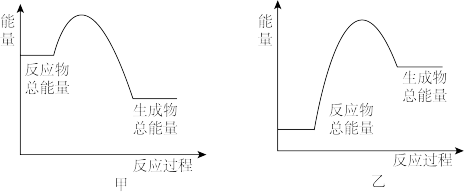
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g) 2NH3(g)是
2NH3(g)是________ (填“吸热”或“放热”)反应。该反应的能量变化可用图______ 表示(填"甲”或”乙“)。
(2)H2还原CO电化学法制备甲醇(CO +2H2 CH3OH)的工作原理如图所示。
CH3OH)的工作原理如图所示。

①通入H2的一端是电池的____ 极(填”正”或“负”),电池工作过程中H+通过质子交换膜向______ (填”左”或"右”)移动,通入CO的一端发生的电极反应为_______ 。
②若电池中氢气(H2)通入量为224 mL(标准状况),且反应完全,则理论上通过电流表的电量为______ C(法拉第常数F=9.65×104C/mol)。
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g)
 2NH3(g)是
2NH3(g)是
(2)H2还原CO电化学法制备甲醇(CO +2H2
 CH3OH)的工作原理如图所示。
CH3OH)的工作原理如图所示。
①通入H2的一端是电池的
②若电池中氢气(H2)通入量为224 mL(标准状况),且反应完全,则理论上通过电流表的电量为
您最近一年使用:0次
9 . 完成下列问题
(1)2mol (g)被氧化为2mol
(g)被氧化为2mol  (g)时放出热量198kJ,反应
(g)时放出热量198kJ,反应 的能量变化如图。
的能量变化如图。
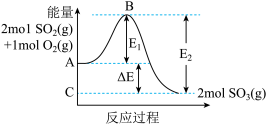
①B的大小对该反应的热量变化___________ (填“有”或“无”)影响。
②2mol (g)和1mol
(g)和1mol  (g)充分反应放出的热量
(g)充分反应放出的热量___________ 198kJ(填“>”、“<”或“=”)。
(2)一定温度下,在体积为2L的密闭容器中,充入1mol 和3mol
和3mol  发生如下反应:
发生如下反应: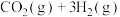
 。测得
。测得 (g)和
(g)和 (g)的物质的量随时间变化如图。
(g)的物质的量随时间变化如图。
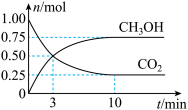
①从反应开始到平衡, 的平均反应速率
的平均反应速率
___________ 。
②达到平衡时, 的转化率为
的转化率为___________ 。(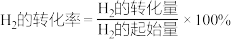 )
)
③下列措施不能提高化学反应速率的是___________ 。
A.升高温度 B.加入适当催化剂 C.缩小体积,增大压强 D.恒温、恒压下通入氦气
④下列叙述中不能说明上述反应达到平衡状态的是___________ 。
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C.反应中 与
与 的物质的量之比为1:1
的物质的量之比为1:1
D.单位时间每消耗1mol 同时生成1mol
同时生成1mol 
(3)如图,左侧石墨上通入 ,右侧石墨上通入
,右侧石墨上通入 ,电解质溶液为KOH溶液。
,电解质溶液为KOH溶液。
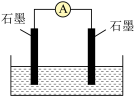
①通入 为
为___________ (填“正”或“负”)极。
②当外电路通过7mol电子时,通入 在标准状况下的体积为
在标准状况下的体积为___________ (列式即可,假设能量全部转化为电能)。
(1)2mol
 (g)被氧化为2mol
(g)被氧化为2mol  (g)时放出热量198kJ,反应
(g)时放出热量198kJ,反应 的能量变化如图。
的能量变化如图。
①B的大小对该反应的热量变化
②2mol
 (g)和1mol
(g)和1mol  (g)充分反应放出的热量
(g)充分反应放出的热量(2)一定温度下,在体积为2L的密闭容器中,充入1mol
 和3mol
和3mol  发生如下反应:
发生如下反应: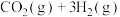
 。测得
。测得 (g)和
(g)和 (g)的物质的量随时间变化如图。
(g)的物质的量随时间变化如图。
①从反应开始到平衡,
 的平均反应速率
的平均反应速率
②达到平衡时,
 的转化率为
的转化率为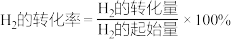 )
)③下列措施不能提高化学反应速率的是
A.升高温度 B.加入适当催化剂 C.缩小体积,增大压强 D.恒温、恒压下通入氦气
④下列叙述中不能说明上述反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变
B.混合气体的压强不随时间的变化而变化
C.反应中
 与
与 的物质的量之比为1:1
的物质的量之比为1:1D.单位时间每消耗1mol
 同时生成1mol
同时生成1mol 
(3)如图,左侧石墨上通入
 ,右侧石墨上通入
,右侧石墨上通入 ,电解质溶液为KOH溶液。
,电解质溶液为KOH溶液。
①通入
 为
为②当外电路通过7mol电子时,通入
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
解题方法
10 . 原电池揭示了氧化还原反应的本质是电子转移,实现了化学能转化成电能,使氧化还原反应在现代生活中获得重大应用,从而改变了人们的生活方式。
某兴趣小组为探究原电池工作原理,利用金属Zn与稀 反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作______ (填“正”或“负”)极,Zn电极上的电极反应式______ 。
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“离子导体”中主要离子的移动方向可描述为______ 。
(3)从能量转化的角度来看,装置A中反应物的总能量______ (填“高于”、“低于”或“=”)生成物的总能量;从反应速率的角度上看,可以观察到A中反应比B中______ (填“快”或“慢”)。
(4)装置B中稀 用足量
用足量 溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为
溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为______ 。
(5)该小组同学由此得出的结论错误的是______。(多选)
某兴趣小组为探究原电池工作原理,利用金属Zn与稀
 反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“离子导体”中主要离子的移动方向可描述为
(3)从能量转化的角度来看,装置A中反应物的总能量
(4)装置B中稀
 用足量
用足量 溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为
溶液代替,起始时Zn电极和Cu电极的质量相等,当导线中有0.2mol电子转移时,Zn电极和Cu电极的质量差为(5)该小组同学由此得出的结论错误的是______。(多选)
| A.任何自发进行的氧化还原反应均可以设计成原电池 |
| B.装置B中Cu电极不可用碳棒代替 |
| C.原电池的负极发生还原反应 |
| D.原电池装置中化学能全部转化为电能 |
您最近一年使用:0次



