1 . 钼及其化合物正越来越多的受到人们的关注 ,其中钼酸钠(Na2MoO4)可溶于水,是一种重要的金属缓蚀剂;钼酸钙(CaMoO4)微溶于水,常用作钼合金添加剂;钼酸属于弱酸,微溶于水,常用于制取高纯同多酸盐。工业上利用辉钼矿(主要成分为MoS2)制备金属钼和钼酸钠晶体的流程如图所示。
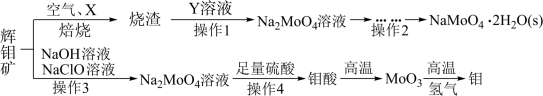
回答下列问题:
(1)辉钼矿在空气中焙烧时,加入X是为了减少空气污染,焙烧后Mo元素以CaMoO4存在,则X是________ ;焙烧时发生反应的化学方程式为__________ 。
(2)已知25℃时,钼酸钙的Ksp=1.6×10-5,则钼酸钙在该温度下的溶解度为_______ g/100g水,但钼酸钙实际溶解度比计算值大许多,其原因是_______ ,操作2中得到的钼酸钠晶体中常混有Y,进一步提纯钼酸钠晶体的方法为__________ 。
(3)辉钼矿中MoS2含量测定:取辉钼矿0.2500g,经在空气中焙烧、操作1、操作2得到钼酸钠晶体0.1210g(Mr=242g/mol),辉钼矿中MoS2的质量分数不低于______ %。
(4)操作3发生反应的离子方程式为_________________ 。
(5)用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如下图所示。b电极的材料为______ (填“镍”或“钼”),电极反应为___________ 。


回答下列问题:
(1)辉钼矿在空气中焙烧时,加入X是为了减少空气污染,焙烧后Mo元素以CaMoO4存在,则X是
(2)已知25℃时,钼酸钙的Ksp=1.6×10-5,则钼酸钙在该温度下的溶解度为
(3)辉钼矿中MoS2含量测定:取辉钼矿0.2500g,经在空气中焙烧、操作1、操作2得到钼酸钠晶体0.1210g(Mr=242g/mol),辉钼矿中MoS2的质量分数不低于
(4)操作3发生反应的离子方程式为
(5)用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如下图所示。b电极的材料为

您最近一年使用:0次
名校
解题方法
2 . 金属在社会生活中的应用很广泛,常用金属表面往往生锈,用盐酸对其表面氧化物进行清洗,会产生酸洗废水。pH在1.5左右的某酸洗废水中含铁元素质量分数约3%,还有如铜、镍、锌、 铬浓度较低的金属也有,工业上综合利用酸洗废水可制备三氯化铁。制备过程如下:
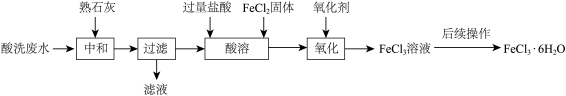
相关金属离子生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)“中和”操作中发生的主要反应的化学方程式为_________ ,调节pH范围为________ ,有利于后续制备得纯度较高的产品。
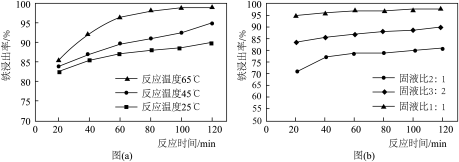
(2)酸溶处理中和后的滤渣,使铁元素浸出。滤渣和工业盐酸反应时,不同反应温度下铁浸出率随时间变化如图(a)所示,可知酸溶的最佳温度为_________ 。按照不同的固液比(滤渣和工业盐酸的投入体积比)进行反应时,铁浸出率随时间变化如图(b)所示,实际生产中固液比选择3:2的原因是_________ 。
(3)氧化时,可选氯酸钠或过氧化氢为氧化剂,若100L“酸溶”所得溶液中Fe 2+含量为1.2mol∙L−1,则需投入的氧化剂过氧化氢的质量为_______ 。
(4)氧化时,除可外加氧化剂外,也可采用惰性电极电解的方法,电解总反应的离子方程式是_____ 。
(5)将得到的FeCl3溶液______ 、过滤、洗涤、干燥得FeCl3∙6H2O晶体。

相关金属离子生成氢氧化物沉淀的pH如下表所示:
氢氧化物 | Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 | Cr(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 7.1 | 5.4 | 4.3 | 7.6 |
| 沉淀完全的pH | 3.7 | 6.7 | 9.2 | 8.0 | 5.6 | 9.6 |
(1)“中和”操作中发生的主要反应的化学方程式为
(2)酸溶处理中和后的滤渣,使铁元素浸出。滤渣和工业盐酸反应时,不同反应温度下铁浸出率随时间变化如图(a)所示,可知酸溶的最佳温度为

(3)氧化时,可选氯酸钠或过氧化氢为氧化剂,若100L“酸溶”所得溶液中Fe 2+含量为1.2mol∙L−1,则需投入的氧化剂过氧化氢的质量为
(4)氧化时,除可外加氧化剂外,也可采用惰性电极电解的方法,电解总反应的离子方程式是
(5)将得到的FeCl3溶液
您最近一年使用:0次
3 . 工业上用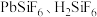 ;混合溶液作电解液,用电解法实现粗铅(主要杂质为
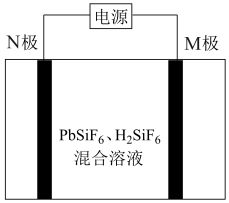
;混合溶液作电解液,用电解法实现粗铅(主要杂质为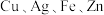 ,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
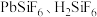 ;混合溶液作电解液,用电解法实现粗铅(主要杂质为
;混合溶液作电解液,用电解法实现粗铅(主要杂质为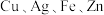 ,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
| A.M极与电源的负极相连 | B.电子由M极流出,经电源流回N极 |
C.N极发生的电极反应之一为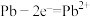 | D.工作一段时间后,溶液中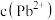 减小 减小 |
您最近一年使用:0次
名校
解题方法
4 . 废电池粉[锂、铁、磷、铜、铝和碳(碳粉)的质量分数分别为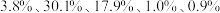 和
和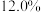 ]回收处理的工艺流程如下:
]回收处理的工艺流程如下: 转化为难溶于水
转化为难溶于水 和可溶于水硫酸锂,写出该反应的化学方程式:
和可溶于水硫酸锂,写出该反应的化学方程式:______________ 。哪些途径可以提高转化的效率(写两条):______________ 。
(2)“净化”步骤可以去除滤液中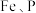 等元素,沉渣1中含
等元素,沉渣1中含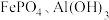 、
、_______ 。沉渣2的主要成分为_______ 。
(3)“电解”可以将溶液中的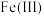 转化为
转化为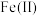 ,溶液中
,溶液中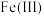 完全转化为
完全转化为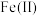 的标志是
的标志是______________ 。甲醇在阳极发生反应生成甲醛,阳极电极反应方程式为_______ 。在电解完成后向溶液中加入 溶液可以将溶液中的
溶液可以将溶液中的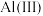 沉淀。
沉淀。
(4)称取一定量的二水磷酸铁,用硝酸溶解后再用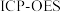 进行分析,得到部分杂质的质量分数
进行分析,得到部分杂质的质量分数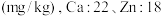 ,评价该制备过程
,评价该制备过程_______ (填“是”或“否”)符合均满足 《电池用磷酸铁》的Ⅱ型标准
《电池用磷酸铁》的Ⅱ型标准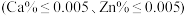 。
。
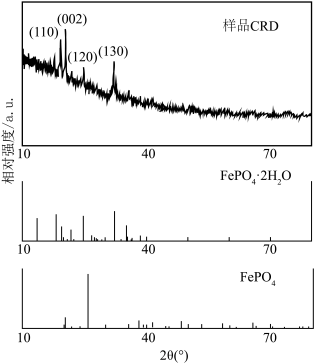
(5) 衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、
衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、 和
和 的标准卡片的
的标准卡片的 衍射实验图谱,结合图像内容判断获的样品
衍射实验图谱,结合图像内容判断获的样品_______ (填“是”或“否”) 。
。
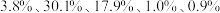 和
和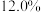 ]回收处理的工艺流程如下:
]回收处理的工艺流程如下: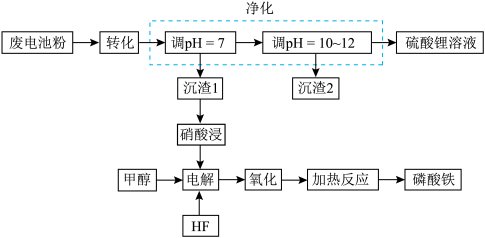
 转化为难溶于水
转化为难溶于水 和可溶于水硫酸锂,写出该反应的化学方程式:
和可溶于水硫酸锂,写出该反应的化学方程式:(2)“净化”步骤可以去除滤液中
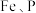 等元素,沉渣1中含
等元素,沉渣1中含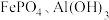 、
、(3)“电解”可以将溶液中的
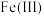 转化为
转化为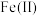 ,溶液中
,溶液中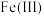 完全转化为
完全转化为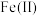 的标志是
的标志是 溶液可以将溶液中的
溶液可以将溶液中的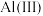 沉淀。
沉淀。(4)称取一定量的二水磷酸铁,用硝酸溶解后再用
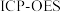 进行分析,得到部分杂质的质量分数
进行分析,得到部分杂质的质量分数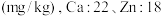 ,评价该制备过程
,评价该制备过程 《电池用磷酸铁》的Ⅱ型标准
《电池用磷酸铁》的Ⅱ型标准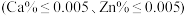 。
。(5)
 衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、
衍射实验图谱与标准卡片进行对比分析,可判断样品晶体类型。下图分别为样品、 和
和 的标准卡片的
的标准卡片的 衍射实验图谱,结合图像内容判断获的样品
衍射实验图谱,结合图像内容判断获的样品 。
。
您最近一年使用:0次
5 . 研究表明,由于人类活动的影响,过量的二氧化碳排放已将海洋表层水的pH值降低了0.2.海水酸性的增强,使多种海洋生物乃至生态系统面临巨大威胁.用如图所示装置可以降低温室气体二氧化碳的含量.下列说法错误的是
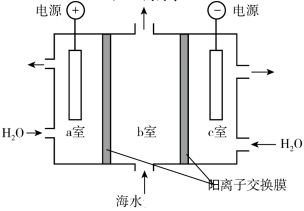
A.a室中发生的电极反应: |
| B.c室中的部分阳离子会迁移到b室 |
C.b室发生的反应: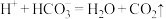 |
D.可以利用上述方法从海水中提取 |
您最近一年使用:0次
2024-05-28更新
|
130次组卷
|
2卷引用:河北省衡水市2024届高三下学期高考预测卷化学试题
6 . NO是大气主要污染物之一。有效去除大气中的NO是环境保护的重要课题。回答下列问题:
I.反应:
 可用于去除汽车尾气中的有害气体,该反应为自发反应。
可用于去除汽车尾气中的有害气体,该反应为自发反应。
(1)
_______ 0(填“>”“<”或“=”)。
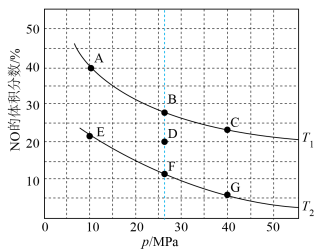
(2)在密闭容器中充入8molNO和10molCO发生反应,平衡时NO的体积分数与温度T、压强p的关系如图所示:
_______  (填“>”或“<”)。
(填“>”或“<”)。
②A点时NO的转化率为_______ 。
③若反应在D点达到平衡,此时对反应容器降温的同时压缩体积,重新达到的平衡状态可能是图中A~G点中的_______ 点。
(3)探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:_______ 。
②温度低于200℃时,图中催化剂I的曲线脱氮率随温度升高变化不大的主要原因是_______ 。
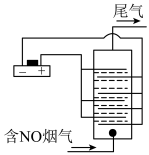
Ⅱ.以铂为电极,加入少量NaOH的饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO进入电解液被阳极产生的氧化性气体氧化为 。
。_______ 。
I.反应:

 可用于去除汽车尾气中的有害气体,该反应为自发反应。
可用于去除汽车尾气中的有害气体,该反应为自发反应。(1)

(2)在密闭容器中充入8molNO和10molCO发生反应,平衡时NO的体积分数与温度T、压强p的关系如图所示:

 (填“>”或“<”)。
(填“>”或“<”)。②A点时NO的转化率为
③若反应在D点达到平衡,此时对反应容器降温的同时压缩体积,重新达到的平衡状态可能是图中A~G点中的
(3)探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:

②温度低于200℃时,图中催化剂I的曲线脱氮率随温度升高变化不大的主要原因是
Ⅱ.以铂为电极,加入少量NaOH的饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO进入电解液被阳极产生的氧化性气体氧化为
 。
。
您最近一年使用:0次
解题方法
7 . 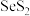 (二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含
(二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含 、
、 及少量
及少量 )制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:
)制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:

已知: 可溶于水
可溶于水 和
和 都是酸性氧化物。
都是酸性氧化物。
(1)“焙烧”时, 与
与 反应生成
反应生成 、
、 、
、 和
和 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)硒与硝酸反应产生的尾气可以用_______ (填化学式)溶液吸收。
(3) 是弱酸,
是弱酸, ,
, 和
和 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
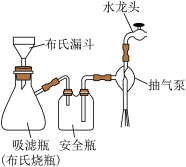
(4)分离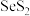 的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是
的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是_______ ,洗涤产品的操作是_______ 。
已知:布氏漏斗是漏斗上面板上有很多小孔,上面板上放滤纸。抽滤的原理是水龙头冲水排气,使瓶内压强小于外界大气压,从而在漏斗上方形成压力加快抽滤速率。
(5)以石墨为阳极,“电解”时阴极的电极反应式为_______ ,阳极产生的气体是_______ (填化学式)。
(6)已知阳极泥中Se的质量分数为2%,100t该阳极泥在上述转化中硒的总提取率为80%,得到的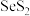 的质量为
的质量为_______ kg(结果保留1位小数)。
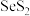 (二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含
(二硫化硒)难溶于水和有机物,广泛应用于各类洗护产品中。以精炼铜的阳极泥(主要含 、
、 及少量
及少量 )制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:
)制备二硫化硒并回收副产物碲和蓝矾的工艺流程如图所示(部分产物和条件省略)。回答下列问题:
已知:
 可溶于水
可溶于水 和
和 都是酸性氧化物。
都是酸性氧化物。(1)“焙烧”时,
 与
与 反应生成
反应生成 、
、 、
、 和
和 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为(2)硒与硝酸反应产生的尾气可以用
(3)
 是弱酸,
是弱酸, ,
, 和
和 溶液反应的离子方程式为
溶液反应的离子方程式为(4)分离
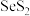 的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是
的“一系列操作”包括抽滤、洗涤、干燥。用如图所示装置抽滤,准备就绪后,抽滤前的操作是已知:布氏漏斗是漏斗上面板上有很多小孔,上面板上放滤纸。抽滤的原理是水龙头冲水排气,使瓶内压强小于外界大气压,从而在漏斗上方形成压力加快抽滤速率。

(5)以石墨为阳极,“电解”时阴极的电极反应式为
(6)已知阳极泥中Se的质量分数为2%,100t该阳极泥在上述转化中硒的总提取率为80%,得到的
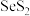 的质量为
的质量为
您最近一年使用:0次
2022-12-17更新
|
270次组卷
|
2卷引用:河北省唐山市部分学校2022-2023学年高三上学期12月月考化学试题
名校
解题方法
8 . 随着现代工农业的发展,水体内氮的含量超标会引发水华现象。科学家探索使用电化学原理,用铁和石墨作电极进行污水除氮,其工作原理如图所示。下列说法正确的是
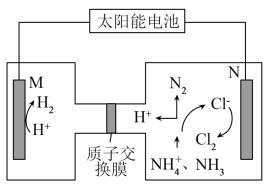

| A.M极材料为铁,连接太阳能电池的正极 |
B.氨气在阳极上的电极反应式为 |
C.制得1mol ,理论上溶液中迁移了6mol电子 ,理论上溶液中迁移了6mol电子 |
| D.电解一段时间后,阳极室的酸性增强 |
您最近一年使用:0次
9 . NO是人体不可缺少的“健康信使”,在心脑血管疾病的治疗中起到重要作用。但NO也是一种有毒的物质,如果在空气中含量过高,存在一定的危害。研究NO的无害化处理对治理大气污染、建设生态文明具有重要意义。请按要求回答下列问题:
(1)汽车发动机工作时会引发N2(g)+O2(g) 2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
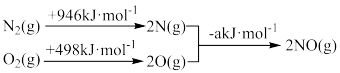
则断开1molNO中化学键所需要的能量为______ 。
(2)已知2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0.
N2(g)+2CO2(g) ΔH<0.
①在密闭容器中充入一定量CO和NO,发生反应,图甲为平衡时NO的体积分数与温度、压强的关系。
温度:T1______ T2(填“<”或“>”);若反应在D点达到平衡,此时对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的______ 点。
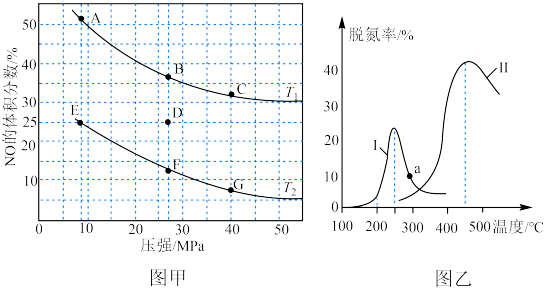
②探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如上图乙所示。曲线上a点的脱氮率______ (填“是>”、“<”或“=”)对应温度下的平衡脱氮率。催化剂Ⅱ条件下,450℃后,脱氮率随温度升高而下降的原因可能是______ ;
(3)T3K时,在刚性密闭容器中充入物质的量之比为2∶2∶1的CO、NO和N2的混合气体,起始气体总压强为P0kPa,达平衡时气体总压强为0.9P0kPa.则CO的平衡转化率为______ ,用气体分压表示KP=______ (用含有P0的代数式表示)。
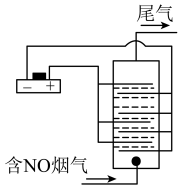
(4)以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为______ 。
(1)汽车发动机工作时会引发N2(g)+O2(g)
 2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
2NO(g) △H=+180kJ•mol﹣1,其能量变化为:
则断开1molNO中化学键所需要的能量为
(2)已知2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0.
N2(g)+2CO2(g) ΔH<0.①在密闭容器中充入一定量CO和NO,发生反应,图甲为平衡时NO的体积分数与温度、压强的关系。
温度:T1

②探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如上图乙所示。曲线上a点的脱氮率
(3)T3K时,在刚性密闭容器中充入物质的量之比为2∶2∶1的CO、NO和N2的混合气体,起始气体总压强为P0kPa,达平衡时气体总压强为0.9P0kPa.则CO的平衡转化率为
(4)以铂为电极,饱和食盐水作电解液,对含有NO的烟气进行脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为
,尾气经NaOH溶液吸收后排入空气。NO被阳极产生的氧化性气体氧化的离子方程式为
您最近一年使用:0次
10 . 利用库仑测硫仪测定气体中 的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后,
的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解至
还原,测硫仪便立即自动进行电解至 又回到原定值,测定结束后,通过测定电解消耗的电量进行计算
又回到原定值,测定结束后,通过测定电解消耗的电量进行计算 的含量(忽略检测前后溶液体积的变化).下列说法正确的是
的含量(忽略检测前后溶液体积的变化).下列说法正确的是
 的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后,
的含量的电解原理如图,检测前(此时电解池不工作)电解质溶液中保持定值,待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解至
还原,测硫仪便立即自动进行电解至 又回到原定值,测定结束后,通过测定电解消耗的电量进行计算
又回到原定值,测定结束后,通过测定电解消耗的电量进行计算 的含量(忽略检测前后溶液体积的变化).下列说法正确的是
的含量(忽略检测前后溶液体积的变化).下列说法正确的是
| A.X极应该和电源的负极相连 |
B.电解时消耗的电量越多,待测气体中 的含量越低 的含量越低 |
C.当通入 时溶液中 时溶液中 向X极移动 向X极移动 |
D.若有 被处理,则电解质溶液中约增加 被处理,则电解质溶液中约增加 |
您最近一年使用:0次



