名校
解题方法
1 . 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
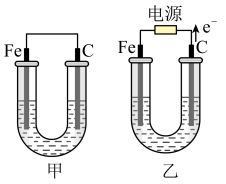
(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的________ 棒,乙池中的________ 棒。
②乙池中阳极的电极反应式是__________________________________ 。
(2)若两池中电解质溶液均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式_______________________________ 。
②甲池中碳极上电极反应式是____________________________ ,乙池碳极上电极反应属于______________ (填“氧化反应”或“还原反应”)。
③将湿润的KI淀粉试纸放在乙池碳极附近,发现试纸变蓝,反应的化学方程式为________________________________________ 。
④若乙池转移0.02 mol e-后停止实验,池中电解质溶液体积是200 mL,则溶液混合均匀后的c(OH—)=________ 。

(1)若两池中电解质溶液均为CuSO4溶液,则反应一段时间后:
①有红色物质析出的是甲池中的
②乙池中阳极的电极反应式是
(2)若两池中电解质溶液均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式
②甲池中碳极上电极反应式是
③将湿润的KI淀粉试纸放在乙池碳极附近,发现试纸变蓝,反应的化学方程式为
④若乙池转移0.02 mol e-后停止实验,池中电解质溶液体积是200 mL,则溶液混合均匀后的c(OH—)=
您最近半年使用:0次
2016-12-09更新
|
1144次组卷
|
4卷引用:安徽省天长市天长二中2018-2019学年高二第一学期12月月考化学试题
安徽省天长市天长二中2018-2019学年高二第一学期12月月考化学试题(已下线)2011-2012学年辽宁省开原高中高二第三次月考化学试卷【全国百强校】福建省仙游第一中学2017-2018学年高二上学期期中考试化学试题上海市嘉定区交附2018-2019学年高二上学期开学摸底考化学试题
名校
解题方法
2 . 如右图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为_____ 极,A极的电极反应式为_______________ 。若所盛溶液为KCl溶液:则B极的电极反应式为________________ , K+移向___ 极(填A、B)
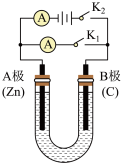
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:①A电极附近可观察到的现象是_________________________ 。
②B电极上的电极反应式为________________ ,总反应化学方程式是_______________________________________ 。
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为_________ 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的___________ 。
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是_______ ,电极反应式是____________________ ,反应一段时间后电解质溶液中Cu2+浓度______ (填“增大”、“减小”、“不变”)。
(1)打开K2 ,合并K1 ,若所盛溶液为CuSO4溶液:则A为

(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则:①A电极附近可观察到的现象是
②B电极上的电极反应式为
③反应一段时间后打开K2 , 若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL, 将溶液充分混合,溶液的pH约为
(3)如要用电解方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是
您最近半年使用:0次
2016-12-09更新
|
524次组卷
|
4卷引用:安徽省阜阳市临泉县第一中学2016-2017学年高二下学期学科竞赛化学试题
安徽省阜阳市临泉县第一中学2016-2017学年高二下学期学科竞赛化学试题(已下线)2011-2012学年浙江省诸暨中学高二上学期期中考试化学(理)试卷湖北省宜昌市部分示范高中教学协作体2016-2017学年高二下学期期中考试化学试题湖北省宜昌市示范高中协作体2016-2017学年高二下学期期中考试化学试题
2010·安徽安庆·三模
3 . 如图:X为铁棒,Y为铜棒,当K闭合后,下列有关分析不正确的是


| A.当a为电流表,b为浓硝酸时:Y为负极 |
| B.当a为电流表,b为稀硫酸时:X电极反应为:Fe-2e-=Fe2+ |
| C.当a为直流电源,b为硫酸铜溶液时:X、Y两电极附近的SO42-浓度相等 |
| D.当a为直流电源,b为NaOH溶液,X极附近产生白色沉淀时:电子从X极流入a |
您最近半年使用:0次
4 . 市场上经常见锂离子电池,它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应式为:
Li + 2Li0.35NiO2 2Li0.85NiO2。下列说法不正确的是
2Li0.85NiO2。下列说法不正确的是
Li + 2Li0.35NiO2
 2Li0.85NiO2。下列说法不正确的是
2Li0.85NiO2。下列说法不正确的是 | A.放电时,负极的电极反应式:Li — e-= Li+ |
| B.该电池不能用水溶液作为电解质 |
| C.充电时,Li0.5NiO2既发生氧化反应又发生还原反应 |
| D.放电过程中Li+向负极移动 |
您最近半年使用:0次
2016-12-09更新
|
298次组卷
|
16卷引用:2020年安徽省全省教学质量检测统一考试(练习检测一)
2020年安徽省全省教学质量检测统一考试(练习检测一)2009年普通高等学校招生统一考试理综试题化学部分(浙江卷)2009高考真题汇编-碱金属元素及其化合物(已下线)2010年天津一中高二下学期期中考试化学试题(已下线)2010—2011学年黑龙江省鹤岗一中高一下学期期末考试化学试卷(已下线)2012-2013学年山东省冠县武训高中高二10月月考化学试卷(已下线)2012-2013学年山东省冠县武训高中高二10月月考化学试卷(已下线)2014届海南省琼海市嘉积中学高三上学期教学质量监测化学试卷2015-2016学年河南省安阳三十六中高二上学期期中考试化学试卷2016届黑龙江省哈尔滨师大附属中学高三上12月月考化学试卷2016-2017学年吉林省长春实验中学高二上9月月考化学卷(已下线)同步君 选修4 第4章 第2节 化学电源高中化学人教版 选修四 第四章 电化学基础 第二节 化学电源 化学电源四川省南充市白塔中学2019-2020学年高二下学期开学考试化学试题(已下线)【南昌新东方】江西省九江第一中学2018-2019学年高二上学期第二次月考化学试题福建省仙游县第二中学2022-2023学年高二上学期期中考试(选考班)化学试题
真题
名校
5 . 请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______ (要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________ (填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
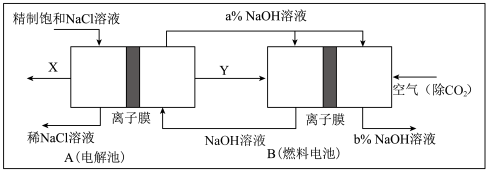
①图中X、Y分别是_____ 、_______ (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________ ;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______ ;负极:_____ ;
③这样设计的主要节(电)能之处在于(写出2处)____________ 、____________ 。
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X、Y分别是
②分别写出燃料电池B中正极、负极上发生的电极反应正极:
③这样设计的主要节(电)能之处在于(写出2处)
您最近半年使用:0次
2016-12-09更新
|
192次组卷
|
7卷引用:2020年安徽省全省教学质量检测统一考试(练习检测一)
2020年安徽省全省教学质量检测统一考试(练习检测一)2009年普通高等学校招生统一考试理综试题化学部分(宁夏卷)2009年高考真题汇编-卤 素(已下线)2010年陕西省五校高三第一次模拟考试理综化学试题(已下线)2011-2012学年河南省平顶山市高一上学期期末调研考试化学试卷2016-2017学年江苏省如东高级中学高一下学期第一次(3月)阶段检测化学试卷云南省普洱市景东彝族自治县第一中学2019-2020学年高二下学期期中考试理综化学试题
名校
6 . 用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是


| A.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
您最近半年使用:0次
2016-07-25更新
|
855次组卷
|
14卷引用:安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题
安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题(已下线)2012届山东省泰安市高三上学期期末检测化学试卷2015-2016学年河北省唐山市高二上学期期末考试化学试卷2016届甘肃省武威六中高三一轮复习阶段测(五)化学试卷2015-2016学年湖南省娄底市重点中学高二下学期期末化学试卷【全国百强校】北京市第四中学2017-2018学年高一下学期期末考试化学(选考)试题【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题云南省临沧市双江县第一中学2019-2020学年高二上学期12月月考化学试题云南省通海三中2019-2020学年高二上学期期末考试化学试题广西壮族自治区田阳高中2019-2020学年高二下学期6月月考理科综合化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记湖南省益阳市2020-2021学年高三上学期复学摸底考试化学试题河北省石家庄一中东校区2020-2021学年高一第二学期教学质量检测(二)化学试题黑龙江省黑河市五校(嫩江市第一中学,嫩江市职业高中,黑河七中,伊拉哈中学,海江中学)2021-2022学年高二上学期期末联考化学试题
7 . 铁铬氧化还原液流电池是一种低成本的储能二次电池,电池放电时的结构如下图所示,充放电过程涉及的反应为:Fe3+ + Cr2+  Fe2+ + Cr3+。下列说法一定正确的是
Fe2+ + Cr3+。下列说法一定正确的是
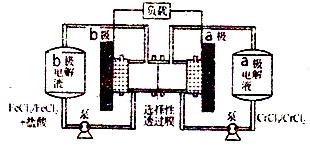
 Fe2+ + Cr3+。下列说法一定正确的是
Fe2+ + Cr3+。下列说法一定正确的是
| A.氧化性:Cr3+>Fe3+ |
| B.电池充电时,b极的电极反应式为Fe3++e-═Fe2+ |
| C.a、b电极材料均可以用碳棒或铜片 |
| D.电池放电时,a极c(Cl-)增大 |
您最近半年使用:0次
8 . 利用如图所示装置进行下列实验,下表中对应叙述正确的是
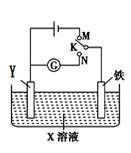

| A | X为硫酸氢钠,Y为石墨 K与M连接时;K与N连接时 | 一段时间后溶液的pH均增大 |
| B | X为氯化钠,Y为石墨 K与M连接时; K与N连接时 | 石墨电极反应均为: 4OH--4e-===2H2O+O2↑ |
| C | X为硫酸氢钠,Y为锌 K与M连接时; K与N连接时 | 铁电极反应均为: 2H++2e-===H2↑ |
| D | X为氯化钠,Y为锌 K与M连接时; K与N连接时 | 铁电极的保护方法均为: 牺牲阳极的阴极保护法 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 关于如图所示①、②两个装置的评价正确的是


| 选择 | 叙 述 | 评价 |
| A | 装置名称:①电解池,②原电池 | 错误 |
| B | 硫酸浓度变化:①增大,②减小 | 错误 |
| C | 电极反应式①阳极:4OH--4e-=2H2O+O2↑,②正极:Zn-2e-=Zn2+ | 正确 |
| D | 离子移动方向:①H+向阴极移动,②H+向正极移动 | 正确 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2015-03-05更新
|
212次组卷
|
4卷引用:安徽省滁州市定远县育才学校2021-2022学年高二上学期期中考试(实验班)化学试题
安徽省滁州市定远县育才学校2021-2022学年高二上学期期中考试(实验班)化学试题(已下线)2013-2014宁夏银川市第一中学高三第二次模拟考试理综化学试卷2015届宁夏银川市九中高三上学期第四次月考理综化学试卷2015届江西省上高二中高三上学期第五次月考理综化学试卷



