1 . 有机化合物在生活中随处可见。请根据题意填空:
(1)利用食醋能除去水垢(主要含碳酸钙),说明醋酸的酸性___________ (填“>”或“<”)碳酸的。
(2)淀粉和纤维素都属于多糖,鉴别它们的试剂可选用___________ (填“氯水”或“碘水”)。
(3)聚乙烯制品用途很广。由乙烯制取聚乙烯的化学方程式为
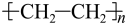 ,该反应类型属于
,该反应类型属于___________ (填“取代”或“加聚”)反应。
(1)利用食醋能除去水垢(主要含碳酸钙),说明醋酸的酸性
(2)淀粉和纤维素都属于多糖,鉴别它们的试剂可选用
(3)聚乙烯制品用途很广。由乙烯制取聚乙烯的化学方程式为

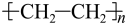 ,该反应类型属于
,该反应类型属于
您最近一年使用:0次
23-24高二下·全国·课前预习
2 . 淀粉
(1)存在与物理性质
①存在:在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。天然淀粉由___________ 淀粉和___________ 淀粉组成。___________ 淀粉含量很高的一些谷物,如糯米、糯玉米等有比较黏的口感。
②物理性质:淀粉是白色粉末状物质,___________ 甜味,___________ 溶于冷水。在热水中淀粉会___________ ,形成胶状的淀粉糊。
(2)化学性质——淀粉属于非还原糖
①酯化反应:分子中葡萄糖单元中有___________ ,与羧酸发生酯化反应。
②在酸或酶的作用下水解,其水解反应方程式为___________ 。
③淀粉遇___________ 变蓝,可以用碘水检验淀粉。
(3)应用——食物和工业原料。
(1)存在与物理性质
①存在:在种子、块根和块茎中含量丰富,谷类和薯类含淀粉较多。天然淀粉由
②物理性质:淀粉是白色粉末状物质,
(2)化学性质——淀粉属于非还原糖
①酯化反应:分子中葡萄糖单元中有
②在酸或酶的作用下水解,其水解反应方程式为
③淀粉遇
(3)应用——食物和工业原料。
您最近一年使用:0次
3 . 葡萄糖、淀粉和蛋白质的特性实验
(1)葡萄糖的特征反应:
①葡萄糖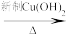
_____ (填现象)
②葡萄糖
_____ (填现象)
注意:新制Cu(OH)2和银氨溶液都是碱性的。上列两反应,常用于鉴别葡萄糖。
(2)淀粉的特征反应:在常温下,淀粉遇碘变_____
注意:淀粉遇到I2(碘单质)才变蓝色,而遇到化合态的碘如I-、 等不变色。可用碘检验淀粉的存在,也可用淀粉检验碘的存在。
等不变色。可用碘检验淀粉的存在,也可用淀粉检验碘的存在。
(3)蛋白质的特征反应:
①颜色反应:蛋白质
_____ (填现象)
②灼烧反应:灼烧蛋白质,产生烧焦羽毛的气味
| 实验内容 | 实验现象 |
| 葡萄糖+新制Cu(OH)2加热至沸腾 | 出现砖红色沉淀 |
| 淀粉+碘酒 | 变蓝色 |
| 蛋白质+浓HNO3 | 显黄色 |
(1)葡萄糖的特征反应:
①葡萄糖
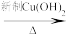
②葡萄糖

注意:新制Cu(OH)2和银氨溶液都是碱性的。上列两反应,常用于鉴别葡萄糖。
(2)淀粉的特征反应:在常温下,淀粉遇碘变
注意:淀粉遇到I2(碘单质)才变蓝色,而遇到化合态的碘如I-、
 等不变色。可用碘检验淀粉的存在,也可用淀粉检验碘的存在。
等不变色。可用碘检验淀粉的存在,也可用淀粉检验碘的存在。(3)蛋白质的特征反应:
①颜色反应:蛋白质

②灼烧反应:灼烧蛋白质,产生烧焦羽毛的气味
您最近一年使用:0次
名校
解题方法
4 . I.氰化钠(NaCN)是一种重要的基本化工原料,用于化学合成、电镀、冶金和有机合成医药、农药,同时也是一种剧毒物质,一旦泄漏需要及时处理。一般可以用二氧化氯(ClO2)水溶液或硫代硫酸钠(Na2S2O3)溶液来处理,以减轻环境污染。
(1)NaCN用二氧化氯(ClO2)水溶液处理后,CN-被氧化为CO2和N2,该反应的离子方程式为____ 。
II.工业制备硫代硫酸钠的反应原理:2Na2S+Na2CO3+4SO2=3Na2S2O3 +CO2。某化学小组利用上述原理在实验室制备硫代硫酸钠,并用硫代硫酸钠溶液处理含氰化钠废水。
【实验一】实验室通过如图所示装置制备硫代硫酸钠。
关闭K1,打开K2,打开分液漏斗,缓慢滴加硫酸,控制好反应速率。

(2)①装置A中盛放浓硫酸的仪器名称是____ ;②装置B的作用是____ ;③实验结束后装置D烧杯中的溶质除NaOH之外,还可能有____ 。
(3)实验结束后,在E处可连接盛有____ (填序号)溶液的注射器,再关闭K2,打开K1,以防止拆除装置时装置中的有害气体逸出污染空气。
【实验二】测定硫代硫酸钠产品纯度并处理废水中的氰化钠。
制备的硫代硫酸钠产品一般为Na2S2O3•5H2O,一般可用I2的标准溶液测定产品纯度原理为:2Na2S2O3+I2= Na2S4O6+2NaI。
(4)上述滴定操作中应该选用____ 作为反应的指示剂。
(1)NaCN用二氧化氯(ClO2)水溶液处理后,CN-被氧化为CO2和N2,该反应的离子方程式为
II.工业制备硫代硫酸钠的反应原理:2Na2S+Na2CO3+4SO2=3Na2S2O3 +CO2。某化学小组利用上述原理在实验室制备硫代硫酸钠,并用硫代硫酸钠溶液处理含氰化钠废水。
【实验一】实验室通过如图所示装置制备硫代硫酸钠。
关闭K1,打开K2,打开分液漏斗,缓慢滴加硫酸,控制好反应速率。

(2)①装置A中盛放浓硫酸的仪器名称是
(3)实验结束后,在E处可连接盛有
| A.BaCl2溶液 | B.浓硫酸 | C.酸性KMnO4溶液 | D.NaOH溶液 |
【实验二】测定硫代硫酸钠产品纯度并处理废水中的氰化钠。
制备的硫代硫酸钠产品一般为Na2S2O3•5H2O,一般可用I2的标准溶液测定产品纯度原理为:2Na2S2O3+I2= Na2S4O6+2NaI。
(4)上述滴定操作中应该选用
您最近一年使用:0次
5 . 如图为C、H、O、N、P等元素构成大分子物质甲~丙的示意图。

(1)若图中物质甲能与碘液发生反应显蓝色,则单体3为___________ ,由物质甲生成单体3的化学方程式为___________ 。
(2)若图中丁是由蛋白质和核糖核酸组成的细胞器,则单体1为___________ ,单体2为___________ 。
(3)若物质丙可控制物质乙的合成,则物质丙通常为___________ ,物质丙水解得到的糖为___________ 。

(1)若图中物质甲能与碘液发生反应显蓝色,则单体3为
(2)若图中丁是由蛋白质和核糖核酸组成的细胞器,则单体1为
(3)若物质丙可控制物质乙的合成,则物质丙通常为
您最近一年使用:0次
6 . 按要求回答下列问题。
(1)粽子由糯米等制作而成,糯米中的淀粉是否水解完全,可用___________ 来检验。
(2)与甲烷互为同系物,且含有10个碳原子的有机物分子式为___________ 。
(3)海洋资源的利用具有广阔前景。
①海水淡化的方法有___________ (填一种)。
②下图是从海水中提取镁的简单流程:
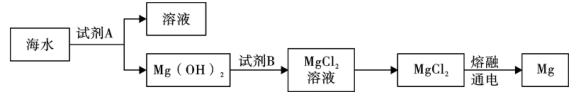
工业上常用于沉淀Mg2+的试剂A的俗名是___________ ,Mg(OH)2转化为MgCl2的离子方程式是___________ 。
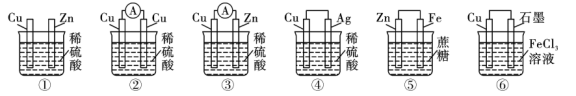
(4)如图所示是某同学设计的几种装置,其中能构成原电池的是___________ (填序号)。
(1)粽子由糯米等制作而成,糯米中的淀粉是否水解完全,可用
(2)与甲烷互为同系物,且含有10个碳原子的有机物分子式为
(3)海洋资源的利用具有广阔前景。
①海水淡化的方法有
②下图是从海水中提取镁的简单流程:

工业上常用于沉淀Mg2+的试剂A的俗名是
(4)如图所示是某同学设计的几种装置,其中能构成原电池的是

您最近一年使用:0次
7 . 下列七种有机物中:
A.CH4 B.CH2=CH2 C. D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
(1)酸性比碳酸强的是___________ (填字母编号,下同)。
(2)易发生银镜反应的是___________ 。
(3)具有正四面体结构的是___________ 。
(4)通常用于检验碘单质的是___________ 。
(5)可用于合成聚乙烯塑料的是___________ 。
(6)可与浓硝酸发生颜色反应的是___________ 。
(7)在空气中燃烧产生带浓烟火焰的是___________ 。
A.CH4 B.CH2=CH2 C.
 D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质(1)酸性比碳酸强的是
(2)易发生银镜反应的是
(3)具有正四面体结构的是
(4)通常用于检验碘单质的是
(5)可用于合成聚乙烯塑料的是
(6)可与浓硝酸发生颜色反应的是
(7)在空气中燃烧产生带浓烟火焰的是
您最近一年使用:0次
2021-05-28更新
|
236次组卷
|
2卷引用:江西省上高二中2020-2021学年高一下学期第五次月考化学试题
名校
8 . 亚硝酸钠可使肉制品色泽粉红,外观上好看诱人,大量食用会致癌。
(1)NaNO2 俗称“工业盐”,外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如 向 NaNO2 的酸性溶液中加入 KI 固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 NO2 。
①该反应中被氧化的元素是_______ (填符号)。
②完成下列反应的化学方程式并配平。
____ NaNO2+____ KI+____ H2SO4=____ +_____ +____ I2+____ NO↑+____
③标准状况下,该反应中每转移 1 mol e-,生成气体的体积是_______ 。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为: 2NO2+Na2CO3=NaNO2+NaNO3+CO2↑氧化剂与还原剂的物质的量之比为_______ 。每产生 33.6 L(标准状况下)CO2,吸收液质量将增加 _______ g。
(3)某同学把 NaNO2 加到硫酸酸化的 KMnO4 溶液中,观察到 KMnO4 溶液褪色且无沉 淀生成,同时生成 KNO3 和 MnSO4,写出该反应的离子方程式:_______
(1)NaNO2 俗称“工业盐”,外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如 向 NaNO2 的酸性溶液中加入 KI 固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 NO2 。
①该反应中被氧化的元素是
②完成下列反应的化学方程式并配平。
③标准状况下,该反应中每转移 1 mol e-,生成气体的体积是
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为: 2NO2+Na2CO3=NaNO2+NaNO3+CO2↑氧化剂与还原剂的物质的量之比为
(3)某同学把 NaNO2 加到硫酸酸化的 KMnO4 溶液中,观察到 KMnO4 溶液褪色且无沉 淀生成,同时生成 KNO3 和 MnSO4,写出该反应的离子方程式:
您最近一年使用:0次
9 . 有A、B、C三种无色溶液,它们分别是葡萄糖、淀粉、甲酸乙酯中的一种。
经实验测得:
①B、C均能与新制 悬浊液反应生成砖红色沉淀;
悬浊液反应生成砖红色沉淀;
②A遇碘水变蓝;
③A、C在稀硫酸、加热的条件下均能水解,水解液加碱后均能与新制 悬浊液反应生成砖红色沉淀。
悬浊液反应生成砖红色沉淀。
(1)判断它们各是什么物质:A__________ ,B__________ ,C__________ 。
(2)写出有关水解反应的化学方程式。
A水解:__________________________________________________ ;
C水解:__________________________________________________ 。
经实验测得:
①B、C均能与新制
 悬浊液反应生成砖红色沉淀;
悬浊液反应生成砖红色沉淀;②A遇碘水变蓝;
③A、C在稀硫酸、加热的条件下均能水解,水解液加碱后均能与新制
 悬浊液反应生成砖红色沉淀。
悬浊液反应生成砖红色沉淀。(1)判断它们各是什么物质:A
(2)写出有关水解反应的化学方程式。
A水解:
C水解:
您最近一年使用:0次
2020-09-25更新
|
276次组卷
|
2卷引用:鲁科版(2019)高一必修第二册 第3章 简单有机化合物 第3节 饮食中的有机化合物 作业帮
10 . 下列五种有机物中:A.CH4;B.CH2=CH2;C.CH3CH2OH;D.CH3COOH;E.淀粉。
(1)C分子中含有的官能团的名称是_____ ;
(2)A分子的结构式是_____ ;
(3)水溶液显酸性的是_____ (填编号);
(4)可用于合成聚乙烯塑料的是_____ (填编号),化学反应方程式为_____________________ ;
(5)通常用于检验碘单质的是_____ (填编号)。
(1)C分子中含有的官能团的名称是
(2)A分子的结构式是
(3)水溶液显酸性的是
(4)可用于合成聚乙烯塑料的是
(5)通常用于检验碘单质的是
您最近一年使用:0次
2019-07-13更新
|
150次组卷
|
2卷引用:新疆沙雅县第二中学2018-2019学年高一下学期期末考试化学试题



