名校
1 . 元素X、Y、Z在周期表中的相对位置如图。已知X元素原子的价层电子排布式为 ,则下列说法错误的是
,则下列说法错误的是
 ,则下列说法错误的是
,则下列说法错误的是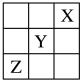
| A.Y元素原子核外d能级无电子填充 |
| B.电负性:X>Y>Z |
| C.元素的最高正价:X>Y>Z |
| D.基态Z原子的核外电子占据的最高能级的电子云轮廓图的形状为哑铃形 |
您最近一年使用:0次
2023-07-10更新
|
139次组卷
|
5卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题
2 . 下列关于原子结构及元素周期表的说法错误的是
| A.所含元素种类最多的族是第ⅢB族 |
| B.同一原子中,2p、3p、4p能级的能量依次升高 |
| C.在元素周期表中,ds区只有6种自然形成的元素,且均为金属元素 |
| D.基态原子价层电子排布式为ns2的元素一定是第IIA族元素(n为周期数) |
您最近一年使用:0次
2023-07-10更新
|
121次组卷
|
4卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题
解题方法
3 . 下列关于核外电子排布及运动状态的说法正确的是
| A.电子云图中的小点越密,表示电子在原子核外某处单位体积内出现的概率越大 |
B.基态N原子的核外电子排布式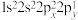 违反了能量最低原理 违反了能量最低原理 |
C.基态 的核外电子存在25种运动状态 的核外电子存在25种运动状态 |
D.在原子中第n电子层含有的原子轨道数为 |
您最近一年使用:0次
2023-07-10更新
|
178次组卷
|
3卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题
解题方法
4 . 化学学科的发展离不开科学家的贡献,下列科学家与其贡献不匹配的是
| A.泡利——能量最低原理 | B.玻尔——原子结构模型 |
| C.鲍林——杂化轨道理论 | D.门捷列夫——元素周期律 |
您最近一年使用:0次
2023-07-10更新
|
78次组卷
|
3卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题
名校
解题方法
5 . 氨硼烷( )的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是
)的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是
 )的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是
)的分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法,错误的是A.第一电离能: |
| B.N和B元素都位于周期表的P区 |
| C.氨硼烷是极性分子 |
| D.氨硼烷中N原子和B原子之间形成了配位键 |
您最近一年使用:0次
2023-07-08更新
|
161次组卷
|
3卷引用:云南省玉溪市2022-2023学年高二下学期期末考试化学试题
云南省玉溪市2022-2023学年高二下学期期末考试化学试题云南省玉溪第三中学2022-2023学年高二下学期期末教学质量检测化学试题(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
6 . 短周期主族元素X、Y、Z、W原子序数依次增大,X的简单气态氢化物溶于水呈碱性,基态Y原子无未成对电子,Z的某种氧化物具有漂白性。下列说法正确的是
| A.电负性:W<Z<X |
B.原子半径: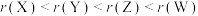 |
| C.最高价氧化物对应水化物的酸性:W<Z |
| D.Y的单质与X、Z、W的单质均能发生反应 |
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
(1)氟原子激发态的电子排布式有_______ (填标号,后同),其中能量较高的是_______ 。
a. b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为_______ 。
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图_______ (填标号),判断的根据是_______ ;第三电离能的变化图是图_______ (填标号)。

(4)短周期元素X、Y、Z、W的原子序数依次增大。
①元素的电负性:Z_______ (填“大于”“小于”或“等于”)W。
②简单离子半径:W_______ (填“大于”“小于”或“等于”)Y。
③氢化物的稳定性:X_______ (填“大于”“小于”或“等于”)Z。
(1)氟原子激发态的电子排布式有
a.
 b.
b. c.
c. d.
d.
(2)某元素原子位于周期表的第四周期,该原子的最外层只有一个电子,其次外层内的所有轨道电子均成对。写出该基态原子电子排布式为
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是图

(4)短周期元素X、Y、Z、W的原子序数依次增大。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | 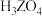 | |||
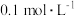 溶液对应的 溶液对应的 | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
名校
解题方法
8 . 下列图示或化学用语表示错误的是
| A | B | C | D |
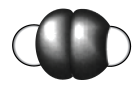 | 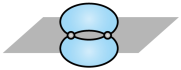 |  | 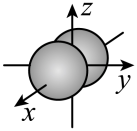 |
| 乙炔的空间填充模型 | 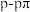 键电子云轮廓图 键电子云轮廓图 |  的结构示意图 的结构示意图 | 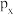 轨道的电子云轮廓图 轨道的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 草酸钴在化学中应用广泛,可以用于制取催化剂和指示剂。用水钴矿(主要成分为Co2O3,还含有少量SiO2、Al2O3、CuO、FeO及MnO2杂质)制取草酸钴晶体(CoC2O4·2H2O)的工艺流程如图所示:

常温下,有关沉淀数据如下表(“完全沉淀”时,金属离子浓度≤1.0×10-5mol·L-1)。
回答下列问题:
(1)下列状态的钴中,电离最外层一个电子所需能量最大的是 (填序号)。
(2)“酸浸”时Co2O3发生反应的化学方程式为___________________ 。
(3)“氧化”时发生反应的离子方程式为___________________________ 。
(4)滤渣②的主要成分有_______________________ ,常温下,若“调节pH”后,溶液中c(Co2+)=0.1 mol·L-1,则需调节溶液pH的范围是______________________ ( 忽略溶液的体积变化)。
(5)“提纯”分为萃取和反萃取两步进行,先向除杂后的溶液中加入某有机酸萃取剂(HA)2,发生反应:Co2++n(HA)2 CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是
CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是_________________________ ;反萃取时,应加入的物质是_____ ( 填溶液名称)。
(6)某含钴配合物的组成为CoCl3·5NH3·H2O,该配合物中钴离子的配位数是6。1 mol该配合物可以与足量的硝酸银反应生成3 mol AgCl沉淀,则该配合物的配体是________ ,若NH3分子与钴离子形成配合物后,H-N- H键角会____________ (填“变大”“变小”或“不变”),并说明理由:_______________ 。

常温下,有关沉淀数据如下表(“完全沉淀”时,金属离子浓度≤1.0×10-5mol·L-1)。
| 沉淀 | Mn(OH)2 | Co(OH)2 | Cu(OH)2 | Fe(OH)3 | Al(OH)3 |
| 恰好完全沉淀时pH | 10.1 | 9.4 | 6.7 | 2.8 | 5.2 |
(1)下列状态的钴中,电离最外层一个电子所需能量最大的是 (填序号)。
| A.[Ar]3d74s1 | B.[ Ar]3d74s2 |
| C.[Ar]3d74s14p1 | D.[Ar]3d74p1 |
(3)“氧化”时发生反应的离子方程式为
(4)滤渣②的主要成分有
(5)“提纯”分为萃取和反萃取两步进行,先向除杂后的溶液中加入某有机酸萃取剂(HA)2,发生反应:Co2++n(HA)2
 CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是
CoA2·(n-1)(HA)2+2H+。当溶液pH处于4.5到6.5之间时,Co2+萃取率随着溶液pH增大而增大,其原因是(6)某含钴配合物的组成为CoCl3·5NH3·H2O,该配合物中钴离子的配位数是6。1 mol该配合物可以与足量的硝酸银反应生成3 mol AgCl沉淀,则该配合物的配体是
您最近一年使用:0次
名校
解题方法
10 . 已知:BF3熔点-127°C,沸点-100°C,水解生成H3BO3(一元弱酸,结构如图所示)和HBF4,与氨气相遇立即生成白色的BF3·NH3(氨合三氟化硼)固体。下列说法错误的是
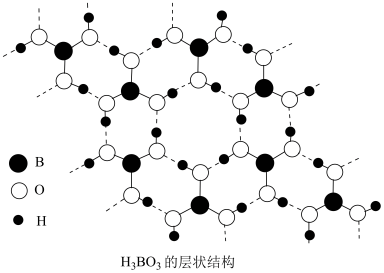

| A.电负性:F>N>H>B |
B. 的空间结构为三角锥形 的空间结构为三角锥形 |
| C.H3BO3中存在分子间氢键,BF3·NH3中存在配位键 |
D.H3BO3的电离方程式为:H3BO3+H2O H+ + H+ + |
您最近一年使用:0次



