名校
解题方法
1 . 如图化合物Q是一种表面涂层材料,其中W、X、Y、Z是分别处于三个短周期的主族元素,原子序数依次增大且不相邻,下列有关说法不正确 的是
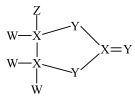
| A.电负性:Y>Z>X>W |
| B.X的基态原子有6种空间运动状态的电子 |
| C.Y的氢化物的沸点较高,主要是因为分子间存在氢键 |
| D.Q在酸性条件下水解生成的气体为非极性分子 |
您最近一年使用:0次
2023-08-27更新
|
237次组卷
|
3卷引用:云南省开远市第一中学校2023-2024学年高二下学期期中考试化学试题
云南省开远市第一中学校2023-2024学年高二下学期期中考试化学试题Z20名校联盟(浙江省名校新高考研究联盟)2023-2024学年高三第一次联考(返校考)化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
名校
解题方法
2 . 化学科学需要借助化学专用语言来描述,下列化学用语表达正确的是
A.基态氧原子的价层电子排布式:2s22p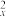 2p 2p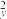 |
B.H2S的电子式: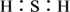 |
C.Be的原子结构示意图: |
D.基态Cr的价层电子的轨道表示式: |
您最近一年使用:0次
名校
解题方法
3 . 如图所示为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是
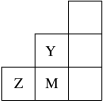

| A.电负性:Y>Z>M |
| B.简单离子半径:M>Z>Y |
| C.ZM2分子中各原子的最外层均满足8电子稳定结构 |
| D.氢化物的稳定性HY>H2Z>HM |
您最近一年使用:0次
2023-08-11更新
|
82次组卷
|
2卷引用:云南省昭通市云天化中学教研联盟2023-2024学年高二上学期期中考试化学试题
名校
解题方法
4 . 下列说法正确的是
| A.氯化氢的分子式是HCl而不是H2Cl,是由共价键的方向性决定的 |
| B.H3O+的存在说明共价键不具有饱和性 |
| C.电子云在两个原子核间重叠后,电子在两核间出现的概率增大 |
| D.分子中共价键的键长越长,键能越大,则分子越稳定 |
您最近一年使用:0次
名校
5 . 长式周期表共有18个纵列,从左到右排为1~18列,即碱金属元素为第1列,稀有气体元素为第18列。按这种规定,下列说法正确的是
| A.第14列元素中未成对电子数是同周期元素中最多的 |
| B.只有第2列的元素原子最外层电子排布为ns2 |
| C.第四周期第8列元素是铁元素 |
| D.第15列元素原子的价电子排布为ns2np3 |
您最近一年使用:0次
名校
解题方法
6 . 下列有关氯元素及其化合物的表示正确的是
A.质子数为17、中子数为20的氯原子: Cl Cl |
B.氯离子(Cl-)的结构示意图: |
C.氯分子的电子式: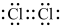 |
| D.基态氯原子的价层电子排布式:1s22s22p63s23p5 |
您最近一年使用:0次
名校
解题方法
7 . DF-31洲际弹道导弹是我国大国地位和国防实力的象征,其制作材料包含了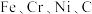 等多种元素。回答下列问题:
等多种元素。回答下列问题:
(1)基态铁原子的电子排布式为_______ , 具有较强的还原性,原因是
具有较强的还原性,原因是_______ 。
(2) 的第二电离能
的第二电离能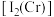 和
和 的第二电离能
的第二电离能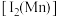 分别为
分别为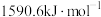 、
、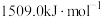 ,
, 的原因是
的原因是_______ ;过氧化铬 中
中 的化合价为
的化合价为 ,则分子中
,则分子中 键、π键的数目之比为
键、π键的数目之比为_______ 。
(3)下图中表示的碳原子能量最高的是_______(填字母)。
(4)超临界流体是物质介于气态和液态之间的新状态,目前应用最广泛的是超临界 。超临界
。超临界 流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。 中C原子的杂化方式为
中C原子的杂化方式为_______ ,分子中的化学键为_______ (填“极性键”或“非极性键”),分子属于_______ (填“极性”或“非极性”)分子。
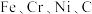 等多种元素。回答下列问题:
等多种元素。回答下列问题:(1)基态铁原子的电子排布式为
 具有较强的还原性,原因是
具有较强的还原性,原因是(2)
 的第二电离能
的第二电离能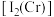 和
和 的第二电离能
的第二电离能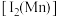 分别为
分别为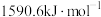 、
、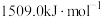 ,
, 的原因是
的原因是 中
中 的化合价为
的化合价为 ,则分子中
,则分子中 键、π键的数目之比为
键、π键的数目之比为(3)下图中表示的碳原子能量最高的是_______(填字母)。
A. | B.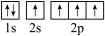 |
C.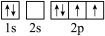 | D.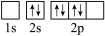 |
 。超临界
。超临界 流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。
流体是一种具有和水相似能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”。 中C原子的杂化方式为
中C原子的杂化方式为
您最近一年使用:0次
名校
解题方法
8 . 氯吡苯脲是一种常用的膨大剂,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。其结构简式如下:
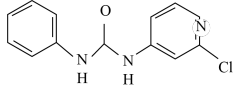
回答下列问题:
(1)基态氯原子价电子排布式为_______ 。
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为_______ ,该物质易溶于水的原因是_______ 。
(3)氯吡苯脲晶体中,微粒间的作用力类型有_______ (填字母)。
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

反应过程中,每生成 氯吡苯脲,形成
氯吡苯脲,形成_______ 个 键、断裂
键、断裂_______ 个π键。
(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有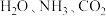 等,请用共价键理论解释
等,请用共价键理论解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:_______ 。

回答下列问题:
(1)基态氯原子价电子排布式为
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为
(3)氯吡苯脲晶体中,微粒间的作用力类型有
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

反应过程中,每生成
 氯吡苯脲,形成
氯吡苯脲,形成 键、断裂
键、断裂(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有
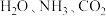 等,请用共价键理论解释
等,请用共价键理论解释 分子比
分子比 分子稳定的原因:
分子稳定的原因:
您最近一年使用:0次
名校
9 .  的配位化合物较稳定且应用广泛。
的配位化合物较稳定且应用广泛。 可与
可与 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的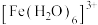 、红色的
、红色的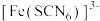 、无色的
、无色的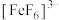 等配离子。某同学按如下步骤进行实验:
等配离子。某同学按如下步骤进行实验:

已知:大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 。下列说法正确的是
。下列说法正确的是
 的配位化合物较稳定且应用广泛。
的配位化合物较稳定且应用广泛。 可与
可与 、
、 、
、 等配体形成使溶液呈浅紫色的
等配体形成使溶液呈浅紫色的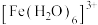 、红色的
、红色的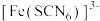 、无色的
、无色的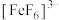 等配离子。某同学按如下步骤进行实验:
等配离子。某同学按如下步骤进行实验:
已知:大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为 。下列说法正确的是
。下列说法正确的是A. 的第一电离能 的第一电离能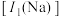 大于 大于 的第一电离能 的第一电离能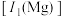 |
B. 与 与 均为直线形结构, 均为直线形结构, 中存在大π键,可表示为 中存在大π键,可表示为 |
C.基态 和基态 和基态 的核外电子排布中,未成对电子数之比 的核外电子排布中,未成对电子数之比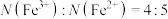 |
D. 中 中 的键角小于 的键角小于 分子中 分子中 的键角 的键角 |
您最近一年使用:0次
2023-07-10更新
|
377次组卷
|
6卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题
10 . 我国科学家开发了一种新型手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物( )作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和
)作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和 )的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
)的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
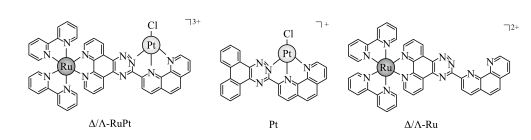
已知:Ru(Ⅱ)表示+2价Ru,Pt(Ⅱ)的配位数为4。
 )作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和
)作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和 )的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
)的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
已知:Ru(Ⅱ)表示+2价Ru,Pt(Ⅱ)的配位数为4。
A.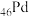 与 与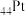 位于同一周期,基态Pd的价层电子排布式为 位于同一周期,基态Pd的价层电子排布式为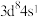 |
| B.单一核配合物Pt中的配位原子只有N原子 |
C. 中Ru原子与Pt原子的配位数相同 中Ru原子与Pt原子的配位数相同 |
D.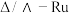 中Ru提供空轨道形成配位键 中Ru提供空轨道形成配位键 |
您最近一年使用:0次
2023-07-10更新
|
94次组卷
|
4卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题



