1 . 废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近半年使用:0次
名校
解题方法
2 . 元素X、Y、Z在周期表中的相对位置如图所示。已知Y元素原子的价电子排布式为nsn-1npn+1,则下列说法不正确的是
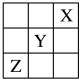
| A.Y元素原子的价电子排布式为4s24p4 |
| B.Y元素在元素周期表的第三周期VIA族 |
| C.X元素所在周期中所含非金属元素最多 |
| D.Z元素原子的核外电子排布式为1s22s22p63s23p63d104s24p3 |
您最近半年使用:0次
2024-05-04更新
|
102次组卷
|
43卷引用:云南省玉溪市新平彝族傣自治县第一中学2020-2021学年高三上学期开学考试化学试题
云南省玉溪市新平彝族傣自治县第一中学2020-2021学年高三上学期开学考试化学试题2014-2015福建省宁德市五校教学联合体高二下学期期中化学试卷2015-2016学年新疆伊犁州伊宁二中高二下期末化学试卷2016-2017学年四川省资阳市高二上学期期末化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第1课时黑龙江省齐齐哈尔市第八中学2018-2019学年高二下学期期中考试化学试题人教化学选修3第一章第二节课时1课时2 核外电子排布与元素周期表、原子半径——A学习区 夯实基础(鲁科版选修3)四川省越西中学2019-2020学年高二5月月考化学试题吉林省通化市通化县综合高级中学2019-2020学年高二下学期期中考试化学试题河北省衡水市桃城区第十四中学2019-2020学年高二下学期摸底考试化学试题山西省太原市山西大学附属中学2019-2020学年高二下学期5月化学试题山西省朔州市怀仁市第一中学校云东校区2019-2020学年高二下学期期末考试化学试题宁夏大学附属中学2020-2021学年高二上学期期中考试化学试题四川省巴中市平昌县驷马中学2020-2021学年高二上学期 十一月月考化学试题河南省驻马店市2020-2021学年高二上学期期终考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质 课时1 原子结构与元素周期表(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质鲁科版2019选择性必修2第1章 原子结构与元素性质 第2节 原子结构与元素周期表 第2课时 核外电子排布与元素周期表(已下线)1.1 原子结构(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)(已下线)第1章 原子结构与元素性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)(已下线)1.2.2 核外电子排布与元素周期表-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)新疆乌苏市第一中学2020-2021学年高二3月月考化学(4-21班)试题四川省邻水实验学校2020-2021学年高二下学期第一次月考化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题贵州省凯里市第三中学2020-2021学年高二下学期第一次月考化学试题(已下线)作业02 原子结构与元素的性质-2021年高二化学暑假作业(人教版2019)河北省石家庄市第一中学2020-2021学年高二下学期学情反馈(一)化学试题(已下线)考向36 原子结构与性质-备战2022年高考化学一轮复习考点微专题四川省广安市第二中学2021-2022学年高二下学期第一次月考化学试题新疆乌鲁木齐市第四中学2021-2022学年高二下学期期中考试化学试题陕西省宝鸡市金台区2021-2022学年高二下学期期中考试化学试题第二节 原子结构与元素的性质 第1课时 原子结构与元素周期表吉林省长春外国语学校2021-2022学年高二下学期阶段测试化学试题四川省遂宁市射洪中学2022-2023学年高二上学期第一次月考(10月)化学试题江苏省盐城市东台创新高级中学2021-2022学年高二2月份月检测化学试题浙江省绍兴蕺山外国语学校2021-2022学年高二下学期第一次月考化学试题天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题四川省南充市嘉陵第一中学2022-2023学年高二下学期6月月考化学试题河北省张家口市宣化第一中学2022-2023学年高二下学期6月月考化学试题江苏省无锡市市北高级中学2023-2024学年高二上学期期末检测化学试卷安徽省蚌埠第二中学2023-2024学年高二下学期3月月考化学试题江苏省镇江市句容高级中学2023-2024学年高二下学期3月考试化学试题
3 . 一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是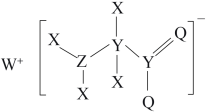
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近半年使用:0次
2024-04-25更新
|
53次组卷
|
2卷引用:云南省大理州实验中学2021-2022学年高二下学期化学期中考试题
解题方法
4 . 离子液体有独特的优良性能。某离子液体 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是
 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是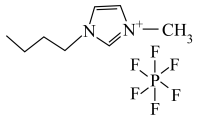
A.第一电离能: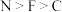 | B. 原子的杂化轨道类型均为 原子的杂化轨道类型均为 |
C. 中所含 中所含 键的数目为 键的数目为 | D.最简单氢化物的沸点: |
您最近半年使用:0次
名校
5 . 黑火药的主要成分为木炭(C)、硫黄(S)和火硝(KNO3).请回答下列问题。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为___________ 形。
(2)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为___________ 。
(3)C、N、O、K四种元素的第一电离能由大到小的顺序为___________ 。
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为___________ ;
②H2Se的中心原子杂化类型是:___________ , SeO32-的立体构型是___________ ;
③比较H2S与H2O沸点高低,并说明原因:___________ 。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为
(2)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为(3)C、N、O、K四种元素的第一电离能由大到小的顺序为
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为
②H2Se的中心原子杂化类型是:
③比较H2S与H2O沸点高低,并说明原因:
您最近半年使用:0次
名校
6 . 下列解释不正确的是
| 选项 | 物质的结构或性质或者实验目的 | 解释 |
| A | 键角: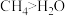 | CH4中C原子与H2O中O原子杂化不同 |
| B | CH4、SiH4、GeH4熔点逐渐升高 | 相对分子质量逐渐增大 |
| C | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
| D | 水中溶解性;苯<吡啶( | 吡啶能与水形成分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 下列化学用语或图示表达正确的是
| A.基态25Mn的价电子3d44s2 |
| B.PCl3分子的空间结构模型:正四面体 |
C.2pz的电子云轮廓图: |
D.基态氧原子的轨道表示式: 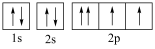 |
您最近半年使用:0次
8 . 黄铵铁矾 和
和 常用作净水剂。
常用作净水剂。
已知: 热分解过程发生的反应如下:
热分解过程发生的反应如下:
①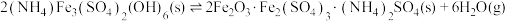
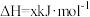
②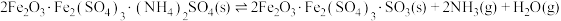
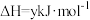
③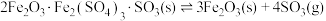
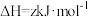
回答下列问题:
(1)基态 的M层电子排布式为
的M层电子排布式为_______ , 中N原子的
中N原子的_______ 轨道与H原子的s轨道重叠形成σ键。
(2) 的
的
_______  。
。
(3)一定温度下,在恒容密闭容器中加入一定量的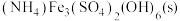 ,只发生反应:
,只发生反应: ,下列可判断该反应达到平衡状态的是_______(填序号)。
,下列可判断该反应达到平衡状态的是_______(填序号)。
(4)500℃时,在体积可变的密闭容器中加入一定量的 固体,只发生反应:
固体,只发生反应: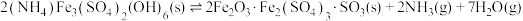 ,达到平衡时测得
,达到平衡时测得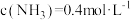 。保持温度不变,将容器体积变为原来的一半,达到新平衡时
。保持温度不变,将容器体积变为原来的一半,达到新平衡时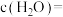
_______  。
。
(5)一定温度下,总压强恒定时,向体积可变的密闭容器中加入一定量的 和
和 氩气,仅发生反应②。测得平衡状态下
氩气,仅发生反应②。测得平衡状态下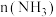 与
与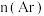 的关系如下图所示。随着通入的
的关系如下图所示。随着通入的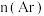 增大,
增大,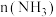 也增大的原因是
也增大的原因是_______ 。 的分解过程会发生下列反应:
的分解过程会发生下列反应:
主反应:

副反应:

两个反应的平衡常数比值 随反应温度升高而
随反应温度升高而_______ (填“增大”“减小”或“不变”);若平衡时总压为25kPa, 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
_______ 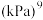 。
。
 和
和 常用作净水剂。
常用作净水剂。已知:
 热分解过程发生的反应如下:
热分解过程发生的反应如下:①
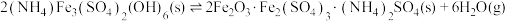
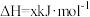
②
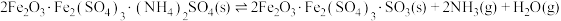
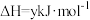
③
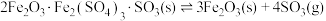
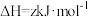
回答下列问题:
(1)基态
 的M层电子排布式为
的M层电子排布式为 中N原子的
中N原子的(2)
 的
的
 。
。(3)一定温度下,在恒容密闭容器中加入一定量的
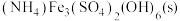 ,只发生反应:
,只发生反应: ,下列可判断该反应达到平衡状态的是_______(填序号)。
,下列可判断该反应达到平衡状态的是_______(填序号)。A. 质量不随时间变化 质量不随时间变化 | B. 体积分数不随时间变化 体积分数不随时间变化 |
| C.混合气体密度不随时间变化 | D.气体平均摩尔质量不随时间变化 |
(4)500℃时,在体积可变的密闭容器中加入一定量的
 固体,只发生反应:
固体,只发生反应: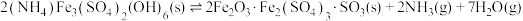 ,达到平衡时测得
,达到平衡时测得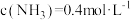 。保持温度不变,将容器体积变为原来的一半,达到新平衡时
。保持温度不变,将容器体积变为原来的一半,达到新平衡时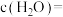
 。
。(5)一定温度下,总压强恒定时,向体积可变的密闭容器中加入一定量的
 和
和 氩气,仅发生反应②。测得平衡状态下
氩气,仅发生反应②。测得平衡状态下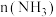 与
与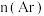 的关系如下图所示。随着通入的
的关系如下图所示。随着通入的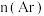 增大,
增大,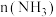 也增大的原因是
也增大的原因是
 的分解过程会发生下列反应:
的分解过程会发生下列反应:主反应:


副反应:


两个反应的平衡常数比值
 随反应温度升高而
随反应温度升高而 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
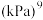 。
。
您最近半年使用:0次
2024-04-18更新
|
81次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
解题方法
9 . 尿素 可与正烷烃形成超分子,原理如图所示。下列说法错误的是
可与正烷烃形成超分子,原理如图所示。下列说法错误的是
 可与正烷烃形成超分子,原理如图所示。下列说法错误的是
可与正烷烃形成超分子,原理如图所示。下列说法错误的是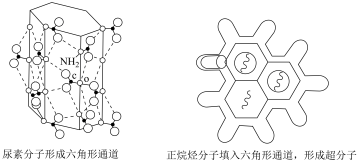
| A.尿素分子中各元素的电负性:O>N>C>H |
| B.尿素分子通过分子间氢键形成六角形通道结构 |
| C.依据分子直径的大小差异可分离同碳数正烷烃和支链烷烃 |
| D.该超分子能稳定存在的原因是尿素分子和正烷烃分子通过共价键结合使能量降低、熵减小 |
您最近半年使用:0次
2024-04-18更新
|
122次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
名校
解题方法
10 . 现有A、B、C、D、E、F六种元素,均为前4周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)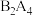 的电子式为
的电子式为___________ (用元素符号表示,下同)。
(2)C元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)某同学推断D元素基态原子的轨道表示式为: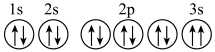 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了___________ (填序号)。
a.泡利不相容原理 b.洪特规则
(4)C、D、E三种元素的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(5)其中五种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈狭长的八面体结构(如下图所示)。阳离子中存在的化学键类型有___________ (填序号)。
该化合物加热时阳离子首先失去的组分是___________ (填化学式),判断理由是___________ 。
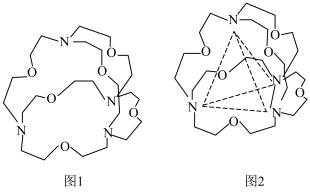
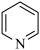
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________ (填标号)。 b.
b. c.
c. d.
d.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素基态原子的核外p电子数比s电子数少1 |
| C元素基态原子的核外p轨道中有两个未成对电子 |
D元素的气态基态原子的第一至第四电离能分别是: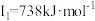 , ,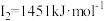 , ,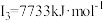 , ,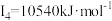 |
| E元素的主族序数比周期数大3 |
| F元素位于元素周期表中的第11列 |
(1)
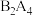 的电子式为
的电子式为(2)C元素的原子核外共有
(3)某同学推断D元素基态原子的轨道表示式为:
 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了a.泡利不相容原理 b.洪特规则
(4)C、D、E三种元素的简单离子半径由大到小的顺序是
(5)其中五种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈狭长的八面体结构(如下图所示)。阳离子中存在的化学键类型有

该化合物加热时阳离子首先失去的组分是
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
 b.
b. c.
c. d.
d.
您最近半年使用:0次

 )
)

