名校
解题方法
1 . X、Y、Z三种元素基态原子的价电子排布式分别为 、
、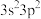 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是
 、
、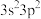 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是A. | B.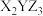 | C.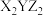 | D. |
您最近一年使用:0次
2024-04-04更新
|
145次组卷
|
10卷引用:云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题
云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题2014-2015河南省实验中学高二下学期期中考试化学试卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题湖南省汨罗市楚雄中学2021-2022学年高二12月月考化学试题四川省广元中学2021-2022学年高二下学期第一次段考化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题甘肃省武山县第一高级中学2023-2024学年高二下学期第一次月考化学试卷
2 . B、N、F、Ti、Fe、As、Se等元素及其化合物的研究对工农业生产意义重大,回答下列问题:
(1)写出Ti基态原子的电子排布式_____ 。
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为_____ 。
(3)VIA族元素中O、S、Se的电负性由大到小的顺序为_____ 。
(4)BF3的空间构型为_____ ;其中B原子采用_____ 杂化,根据对角线规则,B的一些化学性质与元素_____ 的相似。
(5)元素As与N同族。As的氢化物的沸点比NH3的_____ (填“高”或“低”),其判断理由是_____ 。
(1)写出Ti基态原子的电子排布式
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)VIA族元素中O、S、Se的电负性由大到小的顺序为
(4)BF3的空间构型为
(5)元素As与N同族。As的氢化物的沸点比NH3的
您最近一年使用:0次
2023-05-04更新
|
277次组卷
|
2卷引用:云南省丽江市2022-2023学年高二上学期期末考试化学试题
名校
3 . W、X、Y、Z是原子序数依次增大的4种短周期元素,其原子结构如表:
下列说法不正确的是
| 元素 | 原子结构 |
| W | 基态原子L层电子数是K层电子数的2倍 |
| X | 原子核外p电子数比s电子数少1 |
| Y | 原子的最外层2p轨道上有2个未成对电子 |
| Z | 原子核外的M层中只有两对成对电子 |
| A.原子半径:Z>X>Y |
| B.第一电离能:X>Y>W |
| C.W的最简单气态氢化物比X的最简单气态氢化物稳定 |
| D.ZY2和WY2在水中的溶解度较大的是ZY2 |
您最近一年使用:0次
2023-05-04更新
|
188次组卷
|
3卷引用:云南省丽江市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
4 . 下列说法中,正确的是
| A.除短周期外,其他周期都有18种元素 |
| B.周期表中ⅢB~ⅡB族为过渡元素,全部为金属元素 |
| C.价电子数与最高正价相等的元素一定是主族元素 |
| D.s区都是金属元素,p区元素都是非金属元素 |
您最近一年使用:0次
2023-02-01更新
|
233次组卷
|
3卷引用:云南省丽江市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
5 . 现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是
| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高正化合价:④>③=②>① |
您最近一年使用:0次
2022-12-21更新
|
3988次组卷
|
210卷引用:云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题
云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题(已下线)09—10年锦州市高二下学期期末考试化学卷(已下线)2010-2011学年山东省兖州市高二下学期期中考试化学试卷(已下线)2011-2012学年福建省泉州一中高二下学期期中考试化学试卷(已下线)2012--2013学年新疆乌鲁木齐市一中高二下学期期中考试化学试卷(平行班)(已下线)2012-2013学年山东省淄博市沂源一中高二下学期期中模块检测化学卷(已下线)2012-2013学年宁夏银川一中高二下学期期末考试化学试卷(已下线)2012-2013学年黑龙江省牡丹江一中高二下学期期末考试化学试卷(已下线)2012-2013学年福建省四地六校高二下学期第二次联考化学试卷(已下线)2013-2014学年浙江省瑞安中学高二上学期期中化学试卷(实验班)(已下线)2013-2014学年浙江省杭州及周边重点中学高二下学期期中化学试卷(已下线)2013-2014学年辽宁省鞍山市高二下学期期末考试化学(B卷)试卷2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2014-2015福建省宁德市五校教学联合体高二下学期期中化学试卷2014-2015学年山东省淄博市高二下学期期末统考化学试卷2015-2016学年四川省雅安市天全中学高二9月月考化学试卷2015-2016学年四川省雅安中学高二上10月月考化学试卷2015-2016学年山西省太原五中高二下3月周练化学试卷2015-2016学年吉林省前郭县五中高二下学期第一次月考化学试卷2015-2016学年山西省康杰中学高二下期中化学试卷2015-2016学年山西省怀仁一中高二下第三次月考化学试卷2015-2016学年辽宁省五校协作体高二下学期期中考试化学试卷2015-2016学年四川省成都市新都一中高二下4月月考化学试卷2015-2016学年新疆哈密二中高二下期末化学试卷2016-2017学年四川省三台中学校高二上月考化学试卷2017届山西省重点中学协作体高三上期中化学试卷2016-2017学年福建省三明市第一中学高二下学期第一次月考化学试卷2016-2017学年山西省太原市外国语学校高二下学期第一次月考化学试卷河北省石家庄市第一中学2016-2017学年高二下学期期中考试化学试题江西省玉山县第一中学2017届高三化学板块复习测试:物质结构与性质2018版化学(苏教版)高考总复习专题十一课时跟踪训练--原子结构与元素的性质宁夏石嘴山市第三中学2016-2017学年高二下学期期末(2018届高三入学)考试化学试题湖北省孝感市八所重点高中教学协作体2016-2017学年高二7月联合考试化学试题(B)安徽省蚌埠市第二中学2017-2018学年高二上学期期中考试化学试题福建省晋江市季延中学2017-2018学年高二上学期期中考试(理)化学试题黑龙江省哈尔滨市第六中学2017-2018学年高二12月月考化学试题黑龙江省哈尔滨六中2017-2018学年高二12月月考化学试卷四川省凉山木里中学2017-2018学年高二上学期期中考试化学试卷内蒙古赤峰二中2017-2018学年高二上学期期末考试化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时河南省豫西名校2017-2018学年高二下学期第一次联考化学试题山西省祁县中学2017-2018学年高二4月月考化学试题【全国校级联考】辽宁省抚顺市六校2017-2018学年高二下学期期末考试化学试题内蒙古阿拉善左旗高级中学2017-2018学年高二下学期期末考试化学试题陕西省黄陵中学2017-2018学年高二(重点班)下学期期末考试化学试题【全国百强校】福建省厦门外国语学校2018-2019学年高二上学期第一次月考化学试题四川省德阳市第五中学2018-2019学年高二上学期10月月考化学试题甘肃省玉门市第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2018年12月2日 《每日一题》 一轮复习-每周一测贵州省息烽县一中2018-2019学年高二11月份考试化学试题山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题云南省玉溪市峨山一中2018-2019学年高二12月份考试化学考试福建省华安县第一中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】山西省实验中学2018-2019学年高二下学期第一次月考化学试题广西蒙山县第一中学2018-2019学年高二下学期第一次月考化学试题福建省罗源市第一中学2018-2019学年高二下学期3月月考化学试题吉林省乾安县第七中学2018-2019学年高二下学期第一次质量检测化学试题吉林省长春汽车经济开发区第三中学2018-2019学年高二下学期4月月考化学试题云南省景谷一中2018-2019学年高二下学期第一次月考化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题步步为赢 高二化学暑假作业:作业十四 物质结构与性质(选修3)新疆维吾尔自治区北京大学附属中学新疆分校2018-2019学年高二下学期期中考试化学试题【全国百强校】天津市静海区第一中学2018-2019学年高二下学期5月月考化学试题福建省莆田第八中学2018-2019学年高二下学期第二次月考化学试题福建省莆田第六中学2018-2019学年高二下学期期中考试(B卷)化学试题吉林省公主岭市范家屯镇第一中学2018-2019学年高二下学期期中考试化学试题辽宁省瓦房店市高级中学2018-2019学年高二下学期期末考试化学试题广西壮族自治区蒙山县第一中学2019-2020学年高二下学期期末考试化学试题广西蒙山一中2018-2019学年高二下学期期末考试化学试题(已下线)2019年11月22日 《每日一题》2020年高考化学一轮复习——电离能和电负性海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2019-2020学年高二上学期期末考试化学试题四川省广元川师大万达中学2019-2020学年高二上学期期末教学质量检测化学试题四川省绵阳市三台县芦溪中学2017-2018学年高二上学期第五次月考化学试题2020届高三化学二轮物质结构题型专攻——基态原子核外电子排布【选择基础专练】2020届高中化学第一轮复习第十二章《物质结构与性质》测试卷人教化学选修3第一章第二节课时3内蒙古包头市包钢第四中学2018-2019学年高二下学期4月月考化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题第3节 原子结构与元素性质——A学习区 夯实基础(鲁科版选修3)四川省武胜烈面中学校2019-2020学年高二下学期开学考试化学试题四川省阆中中学2019-2020学年高一(仁智班)下学期开学考试化学试题安徽省蚌埠二中2019-2020学年高二下学期开学检测化学试题甘肃省兰州市第一中学2019-2020学年高二下学期4月月考化学试题安徽省滁州市明光市明光中学2019-2020高二下学期第二次月考化学试题河南省郑州市外国语学校2019-2020学年下学期高二第一次月考化学试题四川省越西中学2019-2020学年高二5月月考化学试题辽宁省营口市部分重点高中2017-2018学年高二下学期期末考试化学试题山西省朔州市第一中学2019-2020高二下学期5月月考化学试题山西省太原市阳曲县第一中学2019-2020学年高二5月复学检测化学试题湖北宜城市第二中学2019-2020学年高二下学期期中考试化学试题江苏省震泽中学2019-2020学年高一下学期期中考试(杨班)化学试题新疆昌吉回族自治州第二中学2019-2020学年高二下学期期中考试化学试题安徽省池州市第一中学2019-2020学年高二下学期期中教学质量检测化学试题河北省沧州市任丘市第一中学2019-2020学年高二下学期开学考试化学试题甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(实验班)贵州省思南中学2019-2020学年高二下学期期中考试化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题安徽省安庆市太湖县太湖中学2019-2020学年高二下学期3月线上考试化学试题海南省海口市2019-2020学年高二下学期期中考试化学试题吉林省辽源市田家炳高级中学等友好学校2019-2020学年高二下学期期末考试化学试题宁夏回族自治区吴忠市吴忠中学2019-2020学年高二下学期期末考试化学试题福建省龙岩市一级达标校2019-2020学年高二下学期期末质检化学试题(已下线)第34讲 原子结构与性质-2021年高考化学一轮复习名师精讲练四川省成都外国语学校2019-2020学年高二5月月考化学试题江苏省上冈高级中学2019-2020学年高二上学期期中考试化学(选修)试题湖北省武汉市五校联合体2019-2020学年高一下学期期末考试化学试题江苏宿迁泗阳县众兴中学2021届高三上学期调研考试化学试题四川省乐山沫若中学2020-2021学年高二上学期第一次月考化学试题四川省遂宁市安居区2020-2021学年高二上学期期中考试化学试题(已下线)第35讲 原子结构与性质(精练)-2021年高考化学一轮复习讲练测四川省遂宁市第二中学2020-2021学年高二上学期期中考试化学试题山东潍坊高密一中2020-2021学年高二上学期12月化学月考试题新疆哈密市第八中学2019-2020学年高二下学期期中考试化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质湖北省孝感市高级中学2020—2021学年高二下学期2月调研考试化学试题(已下线)第01章 原子结构与元素性质(B卷能力提升篇)-2020-2021学年高二化学选择性必修2同步单元AB卷(新教材鲁科版)福建省泉州市四校(晋江磁灶中学等)2019-2020学年高二下学期期中联考化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练宁夏吴忠市吴忠中学2020-2021学年高二3月月考化学试题新疆乌苏市第一中学2020-2021学年高二3月月考化学(4-21班)试题福建省福州市福清西山学校2020-2021学年高二下学期3月月考化学试题福建省连城县第一中学2020-2021学年高二下学期第一次月考化学试题福建省莆田第二十五中学2020-2021学年高二下学期第一次月考化学试题四川省成都七中实验学校2020-2021学年高二下学期3月阶段性考试化学试题四川省成都市阳安中学2020-2021学年高二下学期3月月考化学试题福建省永安市第三中学2020-2021学年高二3月月考化学试题黑龙江省齐齐哈尔市第一中学2020-2021学年高二下学期4月月考化学试题湖北省鄂西北六校联考2020-2021学年高二下学期期中考试化学试题贵州省凯里市第三中学2020-2021学年高二下学期第一次月考化学试题湖北省宜城一中等五校联考2020-2021学年高二下学期期中考试化学试题四川省眉山市仁寿县四校2020-2021学年高二5月月考化学试题福建省莆田第十五中学2019-2020学年高二下学期期末考试化学试题江苏省常州市礼嘉中学2020-2021学年高二下学期第二次阶段质量调研化学试题(已下线)第36讲 原子结构与性质(精讲)-2022年一轮复习讲练测人教2019选择性必修2第一章 原子结构与性质复习与提高宁夏石嘴山市平罗中学2021-2022学年高二上学期期中考试化学试题天津市和平区2021-2022学年高二上学期线上期末质量检测化学试题山西省名校联考2021-2022学年高二上学期期末考试化学试题(已下线)解密13 物质结构与性质(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)湖南省邵阳市邵东市2021-2022学年高二上学期期末统考化学试题(已下线)第1.2.2讲 元素周期律-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)湖北省鄂州市2021-2022学年高二上学期期末质量监测化学试题河南省郑州市第四高级中学2021-2022学年高二下学期第二次调研考试西藏班化学试题云南省通海县第一中学2021-2022学年高二下学期3月月考化学试题云南省景东彝族自治县第一中学2021-2022学年高二下学期3月份考试化学试题广东省十五校联盟2021-2022学年高二下学期第一次联考化学试题宁夏青铜峡市宁朔中学2021-2022学年高二3月月考化学试题重庆市育才中学2021-2022学年上学期高二上学期第六次定时练习化学试题内蒙古赤峰市元宝山区第一中学2021-2022学年高二下学期4月月考化学试题海南省东方中学2021-2022学年高二下学期第一次月考化学试题广东省揭阳市榕城区仙桥中学2021-2022学年高二下学期期中考试化学试题河南省开封市五县部分校2021-2022学年高二下学期期中考试化学试题安徽省蚌埠第三中学2021-2022学年高二下学期4月阶段测试化学试题重庆市朝阳中学2021-2022学年高二下学期第一次月考化学试题安徽省亳州市第二中学2021-2022学年高二下学期期末考试化学试题广东省广州市荔湾区2021-2022学年高二下学期期末考试化学试题(已下线)专题13 原子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)云南省普洱市第一中学2021-2022学年高二下学期3月份考试化学试题云南省蒙自一中2021-2022学年高二下学期3月份考试化学试题新疆乌苏市第一中学2021-2022学年高二下学期3月月考化学试题(加强班)新疆乌苏市第一中学2021-2022学年高二下学期3月月考化学试题(平行班)浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题湖南省长沙市明达中学2021-2022学年高二上学期期末考试化学试题福建省三明市宁化第六中学2021-2022学年高二下学期第一次月考化学试题海南省儋州川绵中学2021-2022学年高二下学期第一次月考化学试题陕西省西安市阎良区关山中学2021-2022学年高二下学期期末质量检测化学试题安徽省滁州市定远县育才学校2021-2022学年高二分层班下学期期中考试化学试题上海市建平中学2022-2023学年上学期高二10月月考化学(B卷)试题河北省石家庄市第二中学2022-2023学年高二上学期10月月考化学试题(已下线)第36讲 原子结构与性质(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第36讲 原子结构与性质(讲)-2023年高考化学一轮复习讲练测(全国通用)海南省琼海市嘉积中学2022-2023学年高二上学期第二次月考(期中)化学试题河北省衡水市第二中学2022-2023学年高二上学期期中考试化学试题辽宁省锦州市黑山县黑山中学2021-2022学年高二上学期12月月考化学试题天津市南开中学2022-2023学年高三上学期第三次月考化学试题吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题天津市天津中学2022-2023学年高二上学期线上期末考试化学试题(已下线)1.2.2 元素周期律-同步学习必备知识广东省深圳外国语学校2022-2023学年高二上学期期末考试化学试题江西省九江市濂溪区第一中学2022-2023学年高二上学期期末考试化学试题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题河北省石家庄市辛集市2022-2023学年高二上学期期末教学质量监测化学试题福建省龙岩第一中学2022-2023学年高二下学期第一次月考化学试题福建省永安市第三中学高中校2022-2023学年高三下学期第一次月考(3月)化学试题贵州省贵阳清镇北大培文学校2022-2023学年高二下学期3月月考化学试题江西省抚州市第一中学2022-2023学年高二下学期第一次月考化学试题福建省莆田第十五中学2022-2023学年高二下学期第一次月考(3月)化学试题广东省台山市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)专题01 原子结构与性质(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)河南省洛阳市2022-2023学年高二下学期期中考试化学试题甘肃省高台县第一中学2022-2023学年高二下学期期中考试化学试题广东省佛山市顺德区郑裕彤中学2022-2023学年高二下学期期末模拟化学试题黑龙江省哈尔滨师范大学附属中学2022-2023学年高二下学期期中考试化学试题内蒙古赤峰二中2022-2023学年高二下学期第二次月考化学试题广东省汕尾市华大实验学校2022-2023学年高二下学期5月月考化学试题云南省云南省楚雄彝族自治州民族中学2022-2023学年高二下学期6月月考化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题四川省绵阳中学2022-2023学年高二上学期9月线上测试化学试题甘肃省庆阳第六中学2022-2023学年高二下学期期中考试化学试题海南省海口市第一中学2023-2024学年高二上学期第一次月考化学试题河南省焦作市2022-2023学年第四中学高二下学期3月月考 化学试卷贵州省黔西南布依族苗族自治州2023-2024学年高一上学期1月期末化学试题黑龙江省黑河市第一中学2023-2024学年高二下学期4月月考化学试题陕西省汉中市西乡县第一中学2023-2024学年高二下学期3月月考化学试题四川省内江市威远县威远中学校2023-2024学年高二下学期第一次月考化学试卷内蒙古赤峰新城红旗中学2023-2024学年高二下学期4月月考化学试题河北省石家庄市西山学校2023-2024学年高二上学期期末考试化学试题
6 . 某元素X的逐级电离能如图所示,下列说法正确的是
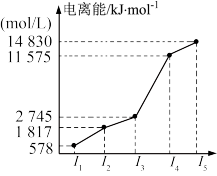

| A.X元素可能为+4价 | B.X可能为非金属 |
| C.X为第五周期元素 | D.X与氯反应时最可能生成的阳离子为X3+ |
您最近一年使用:0次
2022-03-28更新
|
290次组卷
|
26卷引用:云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题
云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题(已下线)2013-2014学年四川省成都市六校协作体高二上学期期中考试化学试卷(已下线)2014-2015学年四川邛崃市高埂中学高二上学期第一次月考化学试卷2014-2015福建省福州八中高二上学期期中化学(理)试卷2015-2016学年贵州省思南中学高二下期中化学试卷云南省曲靖市沾益二中2017-2018学年高二下学期期末考试化学试题云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题云南省彝良县民族中学2018-2019学年高二上学期12月份考试化学试题2020届高三化学二轮物质结构题型专攻——元素性质的递变规律【选择提升专练】人教化学选修3第一章第二节课时5山东省济南外国语学校2019-2020学年高二下学期3月份“空中课堂”阶段性测试化学试题天津市第二十中学2019-2020学年高二下学期阶段性检测化学试题四川省乐山沫若中学2020-2021学年高二上学期第一次月考化学试题(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)河南省汤阴县五一中学2019-2020学年高二下学期期中考试化学试题吉林省长春市实验中学2020-2021学年度高二下学期阶段考试化学试题新疆乌鲁木齐市第八中学2020-2021学年高二下学期第一阶段考试化学试题云南省通海县第一中学2021-2022学年高二下学期3月月考化学试题云南省普洱市第一中学2021-2022学年高二下学期3月份考试化学试题四川省平昌县得胜中学2021-2022学年高二上学期10月月考化学试题四川省巴中市平昌县博雅学校2021-2022学年高二上学期第二次月考化学试题云南省玉溪市华宁县第二中学2021-2022年高二下学期开学考试化学试题河北省唐山市迁西县职教中心2021-2022学年高二(普职融通二部)下学期4月月考化学试题1.3.2元素的电离能、电负性及其变化规律(课前)-鲁科版选择性必修2陕西省咸阳市实验中学2022-2023学年高二上学期第一次月考化学试题
名校
7 . 下列变化需要吸收能量的是
A.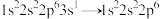 | B.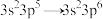 |
C.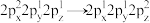 | D. |
您最近一年使用:0次
2022-01-05更新
|
51次组卷
|
3卷引用:云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题
8 . 铬铁合金作为钢的添加料生产多种具有高强度、耐高温、耐腐蚀等优良性能的特种钢,这类特种钢中含有碳、硅、氧、氮、磷、硫等元素。
(1)基态Cr原子的价电子排布式为___________ 。
(2) C、N、O、Si三种元素的第一电离能由大到小的顺序为___________ 。
(3)PO 的空间构型为
的空间构型为___________ ,中心原子的杂化方式为___________ 。
(4)SiO2晶体常伴生于各种矿石中,其晶体结构中,最小的环上有___________ 个原子;Si与C元素位于同一主族,比较SiO2与CO2的键角大小:SiO2___________ CO2(填写“大于”、“小于”或“等于”),原因是___________ 。
(5)无水CrCl3和氨分子作用能形成某种配合物,该配合物的组成相当于CrCl3·6NH3.已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构简式___________ ,配位数___________ ,1 mol该配合物中含有σ键的数目为___________ 。
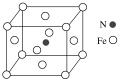
(6)铁和氮形成一种晶体,晶胞结构如图所示,则该晶体的化学式为___________ ,若该晶体的晶胞密度ρg·cm-3,用NA表示阿伏加德罗常数的值,则该晶胞的体积是___________ cm3。
(1)基态Cr原子的价电子排布式为
(2) C、N、O、Si三种元素的第一电离能由大到小的顺序为
(3)PO
 的空间构型为
的空间构型为(4)SiO2晶体常伴生于各种矿石中,其晶体结构中,最小的环上有
(5)无水CrCl3和氨分子作用能形成某种配合物,该配合物的组成相当于CrCl3·6NH3.已知:若加入AgNO3溶液,能从该配合物的水溶液中将所有的氯沉淀为AgCl;若加入NaOH溶液并加热,无刺激性气体产生。请从配合物的形式推算出它的内界和外界,写出该配合物的结构简式
(6)铁和氮形成一种晶体,晶胞结构如图所示,则该晶体的化学式为

您最近一年使用:0次
9 . 下列关于元素第一电离能的说法不正确的是
| A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 |
| B.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大 |
| C.最外层电子排布为ns2np6(当只有K层时为1s2)的原子,第一电离能较大 |
| D.对于同一元素而言,原子的电离能I1<I2<I3…… |
您最近一年使用:0次
2021-06-05更新
|
1026次组卷
|
54卷引用:云南省丽江市永胜县第二中学2019—2020学年高二上学期期末考试化学试题
云南省丽江市永胜县第二中学2019—2020学年高二上学期期末考试化学试题(已下线)2009—2010泉州七中学年度下学期高二年期中考试化学卷(已下线)2012-2013学年陕西省宝鸡中学高二下学期期中考试化学试卷2015-2016学年西藏日喀则一中高二10月月考化学试卷2015-2016学年河北邢台一中高二上学期期中测试化学试卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2016-2017学年湖北省武汉市第二中学高二下学期期中考试化学试卷湖北省武汉市第二中学2016-2017学年高二下学期期中考试化学试题福建省福州市八县(市)协作校2016-2017学年高二下学期期中考试化学试题福建省晋江市季延中学2017-2018学年高二上学期期中考试(理)化学试题四川省广安市2017-2018学年高二上学期期末考试化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第2课时【全国百强校】黑龙江省实验中学2017-2018学年高二下学期期中考试(理)化学试题山西省临猗县临晋中学2017-2018学年高二下学期期末考试化学试题云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题贵州省织金县第一中学2018-2019学年高二上学期期中考试化学试题四川省宜宾市第四中学2018-2019学年高二上学期期末模拟理科综合化学试题【全国百强校】山东省潍坊第一中学2018-2019学年高二下学期开学(2月)考试化学试题山西省沁县中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二下学期4月月考化学试题吉林省乾安县第七中学2018-2019学年高二下学期第二次质量检测化学试题(已下线)专题11.3 晶体结构与性质(练)-《2020年高考一轮复习讲练测》人教化学选修3第一章第二节课时6第3节 原子结构与元素性质——A学习区 夯实基础(鲁科版选修3)海南省海口市海南枫叶国际学校2019-2020学年高二下学期期中考试化学试题(已下线)第十一单元 物质的结构与性质测试题-2021年高考化学一轮复习名师精讲练(已下线)山东省邹城市2018-2019学年高二上学期12月月考化学试卷宁夏回族自治区银川市宁夏大学附属中学2020-2021学年高二上学期第一次月考化学试题(鲁科版2019)选择性必修2 第1章 原子结构与元素性质 第3节 元素性质及其变化规律(人教版2019)选择性必修2 第一章 原子结构与性质 第二节 原子结构与元素的性质 易错颖难集训(二)高二选择性必修2(人教版2019)第一章 原子结构与性质 第二节综合训练鲁科版2019选择性必修2第1章 原子结构与元素性质 第1章学科素养提升(人教版2019)选择性必修2第一章 原子结构与性质 学科素养提升(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版选修3)2月刊 (同步课堂必刷题)(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修2)2月刊 (同步课堂必刷题)(已下线)1.3.1 电离能及其变化规律-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记山西省太原市第五十六中学校2020-2021学年高二第一次月考化学试题宁夏银川市贺兰县景博高中2020-2021学年高二下学期期中考试化学试题黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期期中考试化学试题云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题(已下线)专题14 物质结构与性质-备战2022年高考化学学霸纠错(全国通用)(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.2 原子半径 元素的电离能及其变化规律-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)陕西省咸阳市实验中学2021-2022学年高二上学期第一次月考化学试题(已下线)第38练 原子结构与元素的性质-2023年高考化学一轮复习小题多维练(全国通用)专题2 原子结构与元素性质 第二单元 元素性质的递变规律 第2课时 元素第一电离能和电负性的周期性变化第一章 本章达标检测2江苏省盐城市东台创新高级中学2021-2022学年高二2月份月检测化学试题广东省茂名市电白区2022-2023学年高二上学期期末考试化学(选择性考试)试题安徽省 淮北师范大学附属实验中学2022-2023学年高二下学期第一次月考化学试题2.2.2元素第一电离能和电负性的周期性变化 课中陕西省宝鸡市渭滨区2023-2024学年高二上学期期末考试化学试题山东省青岛一中2023-2024学年高一下学期4月月考化学试卷
名校
解题方法
10 . X、Y、Z、W为原子序数依次增大的前四周期元素,X原子为元素周期表中半径最小的原子,Z原子最外层电子数为次外层电子数的三倍,W位于第IB族,X、Y、Z、W形成的阳离子为狭长的八面体结构如图所示,下列说法不正确的是


| A.X、Y、Z元素第一电离能最大的是Z |
| B.两种配体分子中的键角:X2Z<YX3 |
| C.由图可知该阳离子中心原子的配位数为6 |
| D.加热时该离子首先失去的组分是X2Z |
您最近一年使用:0次
2021-04-29更新
|
574次组卷
|
5卷引用:云南省丽江市古城区第一中学2022-2023学年高三下学期3月月考化学试题
云南省丽江市古城区第一中学2022-2023学年高三下学期3月月考化学试题山东省德州市2021届高三第二次模拟考试化学试题(已下线)2021年高考化学押题预测卷(福建卷)(03)(含考试版、答题卡、参考答案、全解全析)(已下线)专题13 物质结构与性质基础-备战2022年高考化学真题及地市好题专项集训【山东专用】浙江金华第一中学2021-2022学年高一领军班下学期期中考试化学试题



