1 . 褪黑素是迄今发现的最强的内源性自由基清除剂。褪黑素的基本功能就是参与抗氧化系统,防止细胞产生氧化损伤,在这方面,它的功效超过了已知的所有体内物质。某研究小组以乙炔为原料,设计合成褪黑素,合成路线如下(部分反应条件已省略):

已知:无水乙酸钠在碱石灰作用下发生反应:
回答下列问题:
(1)B→C的反应类型为___________ ,C中含氧官能团的名称为___________ ,C分子是否为手性分子:___________ (填“是”或“否”)。
(2)已知: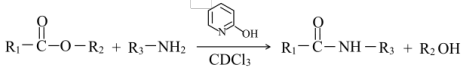 ,通常用酯基和氨基生成酰胺基,不用羧基和氨基直接反应,结合成键元素间
,通常用酯基和氨基生成酰胺基,不用羧基和氨基直接反应,结合成键元素间电负性差值大小 解释原因___________ 。
(3)E→F过程中,反应i的化学方程式为:___________ 。
(4)J的结构简式为___________ ,其中氮原子的杂化轨道类型为___________ 。
(5)写出符合下列条件的H的一种同分异构体(不考虑立体异构)的结构简式___________ 。
i.含有3个六元环,其中1个是苯环;
ii.含有 结构,不含
结构,不含 键;
键;
iii.含有4种不同化学环境的氢原子。
(6)综合上述信息并结合所学知识,在下图方框中填写合适的物质(写结构简式)。①________ ;②_________ ;③___________ 。


已知:无水乙酸钠在碱石灰作用下发生反应:

回答下列问题:
(1)B→C的反应类型为
(2)已知:
 ,通常用酯基和氨基生成酰胺基,不用羧基和氨基直接反应,结合成键元素间
,通常用酯基和氨基生成酰胺基,不用羧基和氨基直接反应,结合成键元素间| 元素 | H | C | O |
| 电负性 | 2.1 | 2.5 | 3.5 |
(3)E→F过程中,反应i的化学方程式为:
(4)J的结构简式为
(5)写出符合下列条件的H的一种同分异构体(不考虑立体异构)的结构简式
i.含有3个六元环,其中1个是苯环;
ii.含有
 结构,不含
结构,不含 键;
键;iii.含有4种不同化学环境的氢原子。
(6)综合上述信息并结合所学知识,在下图方框中填写合适的物质(写结构简式)。①

您最近一年使用:0次
解题方法
2 . 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种新型超分子,其分子结构如下图所示(Y和Y之间重复单元的W、X未全部标出),W、X、Z分别位于不同周期,Z是同周期中金属性最强的元素,下列说法正确的是


A.简单气态氢化物的沸点: |
B.第一电离能: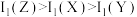 |
C. 只含有离子键 只含有离子键 |
D.原子半径: |
您最近一年使用:0次
名校
解题方法
3 . 2023年诺贝尔化学奖授予对量子点的发现有突出贡献的科研工作者。量子点是指尺寸在纳米量级(通常2~20nm)的半导体晶体,其中铜铟硫(CuInS2)量子点被广泛用于光电探测、发光二极管以及光电化学电池领域。下列说法不正确 的是
| A.制备过程中得到的CuInS2量子点溶液能够产生丁达尔效应 |
| B.可利用X射线衍射技术解析量子点的晶体结构 |
| C.已知In的原子序数为49,可推知In位于元素周期表第四周期 |
| D.基态Cu+的价层电子排布式为3d10 |
您最近一年使用:0次
2023-11-06更新
|
596次组卷
|
7卷引用:云南省大理白族自治州民族中学2023-2024学年高三上学期1月月考理综试卷
云南省大理白族自治州民族中学2023-2024学年高三上学期1月月考理综试卷北京市丰台区2023-2024学年高三上学期期中练习化学试题(已下线)选择题1-5北京市第一七一中学2023-2024学年高三上学期12月月考化学试题 (已下线)题型05 物质的性质与应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)宁夏石嘴山市平罗中学2023-2024学年高三上学期第三次月考化学试题北京汇文中学2023-2024学年高三上学期12月上旬化学测试
4 . 三价铬离子能形成多种配位化合物,[Cr(NH3)3(H2O)2Cl]2+(其结构如下图)是其中一种配位化合物的阳离子。下列说法正确的是
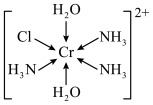

| A.该配合物的中心离子是Cr3+,配位数为5 |
| B.基态原子未成对电子数:Cr>N>O>Cl |
| C.基态原子的第一电离能:Cl>O>N>H |
| D.该配合物阳离子中存在极性键和非极性键 |
您最近一年使用:0次
5 . 氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一
Ⅰ.一定条件下,用 催化还原可消除NO污染。
催化还原可消除NO污染。
已知:
①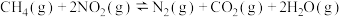
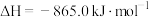
②
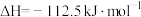
(1) 和
和 完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则
完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则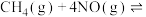
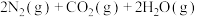

___________  ;一定温度下,往一体积不变的密闭容器中加入适量的
;一定温度下,往一体积不变的密闭容器中加入适量的 和NO,下列条件能判断该反应到达平衡状态的有
和NO,下列条件能判断该反应到达平衡状态的有___________ (填序号)。
A.混合气体的平均相对分子质量不变
B.
C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
E.混合气体的密度不变
(2)将2mol NO(g)、1mol (g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
(g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和 。平衡时,若
。平衡时,若 、
、 与
与 三者的物质的量相等,则NO转化率为
三者的物质的量相等,则NO转化率为___________ ,反应②平衡常数
___________ (用含p的代数式表示)。
Ⅱ.利用如图所示原理去除NO:
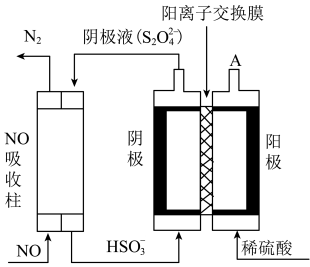
(3)基态N原子中,电子占据的最高能级为___________ 能级,该能级轨道的形状为___________ ;电解池中阴极反应式为___________ 。
(4)A口每产生224mL (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为___________ mol。
Ⅰ.一定条件下,用
 催化还原可消除NO污染。
催化还原可消除NO污染。已知:
①
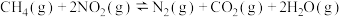
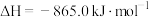
②

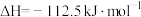
(1)
 和
和 完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则
完全反应,每生成2.24L(标准状况)NO时,吸收8.9kJ的热量,则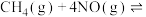
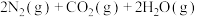

 ;一定温度下,往一体积不变的密闭容器中加入适量的
;一定温度下,往一体积不变的密闭容器中加入适量的 和NO,下列条件能判断该反应到达平衡状态的有
和NO,下列条件能判断该反应到达平衡状态的有A.混合气体的平均相对分子质量不变
B.

C.单位时间里有4n mol C—H断开同时有4n mol O—H断开
D.混合气体的压强不变
E.混合气体的密度不变
(2)将2mol NO(g)、1mol
 (g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和
(g)和2mol He(g)通入反应器,在温度T、压强p条件下进行反应②和 。平衡时,若
。平衡时,若 、
、 与
与 三者的物质的量相等,则NO转化率为
三者的物质的量相等,则NO转化率为
Ⅱ.利用如图所示原理去除NO:

(3)基态N原子中,电子占据的最高能级为
(4)A口每产生224mL
 (体积已换算成标准状况,不考虑
(体积已换算成标准状况,不考虑 的溶解),可处理NO的物质的量为
的溶解),可处理NO的物质的量为
您最近一年使用:0次
2023-09-20更新
|
325次组卷
|
2卷引用:云南大理市辖区2023-2024学年高三上学期毕业生区域性规模化统一检测理综化学试题
6 . 铜是重要的战略资源,云南是我国铜资源储量较高的省份之一,回答下列问题:
(1)铜在周期表中位于第______ 族(填族序数),属于______ 区。
(2)铜可以形成多种配合物。
① 的核外电子排布式是
的核外电子排布式是______ ,过渡金属离子与水分子形成配合物时,若d轨道全空或全满时,化合物无颜色,否则有颜色。据此判断,
______ (填“有”或“无”)颜色。
② 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是______ , 中N原子的杂化方式是
中N原子的杂化方式是______ ,空间构型是______ 。
(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是______ 。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为______ 。
(1)铜在周期表中位于第
(2)铜可以形成多种配合物。
①
 的核外电子排布式是
的核外电子排布式是
②
 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是 中N原子的杂化方式是
中N原子的杂化方式是(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近一年使用:0次
7 . 短周期主族元素X、Y、Z、Q、W原子序数依次增大,X的一种核素常用于测定文物的年代,Z的一种单质常用来消毒杀菌,Q最外层有2个电子,W和Y同族。下列说法不正确的是
| A.第一电离能:X>Y>Z | B.简单氢化物的沸点:Y>W |
| C.最高价氧化物对应水化物的酸性:Y>X | D.X、Y、Z的最简单氢化物的杂化方式均为 杂化 杂化 |
您最近一年使用:0次
解题方法
8 . 某元素基态原子价电子排布式为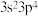 ,下列说法不正确的是
,下列说法不正确的是
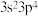 ,下列说法不正确的是
,下列说法不正确的是| A.该原子位于周期表p区 |
| B.该元素的最高正价为+4价 |
| C.该基态原子中存在两个未成对电子 |
| D.该元素最简单氢化物的空间构型是V形 |
您最近一年使用:0次
名校
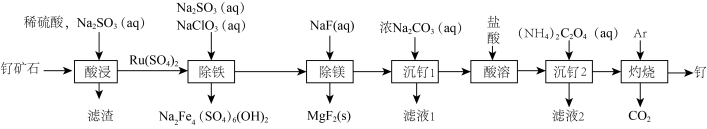
9 . 铂钉催化剂是甲醇燃料电池的阳极催化剂。一种以钉矿石[主要含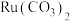 ,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钉(Ru)的流程如图。回答下列问题:
,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钉(Ru)的流程如图。回答下列问题:
(1)根据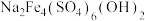 中Fe的化合价,写出该离子的价层电子排布式为
中Fe的化合价,写出该离子的价层电子排布式为___________ 。
(2)“酸浸”时,Na2SO3的作用是___________ 。“滤渣”的主要成分有SiO2和___________ (填化学式)。
(3)“除铁”的离子方程式为___________ 。(提示:1molNaClO3参与反应,转移6mol电子)
(4)从“滤液2”中可提取一种化肥,该物质的阳离子的空间构型为___________ 。
(5)“灼烧”时Ar的作用是___________ 。
(6)某工厂用10t钉矿石[含 、
、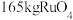 ],最终制得3636kgRu,则Ru的产率为
],最终制得3636kgRu,则Ru的产率为___________ (保留三位有效数字)。
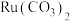 ,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钉(Ru)的流程如图。回答下列问题:
,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钉(Ru)的流程如图。回答下列问题:
(1)根据
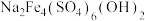 中Fe的化合价,写出该离子的价层电子排布式为
中Fe的化合价,写出该离子的价层电子排布式为(2)“酸浸”时,Na2SO3的作用是
(3)“除铁”的离子方程式为
(4)从“滤液2”中可提取一种化肥,该物质的阳离子的空间构型为
(5)“灼烧”时Ar的作用是
(6)某工厂用10t钉矿石[含
 、
、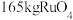 ],最终制得3636kgRu,则Ru的产率为
],最终制得3636kgRu,则Ru的产率为
您最近一年使用:0次
名校
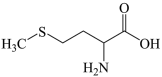
10 . 甲硫氨酸是构成人体的必需氨基酸之一,结构简式如图所示。下列有关说法正确的是

| A.CH4、CS2、SO2都是由极性键构成的极性分子 |
| B.基态氧原子的电子有8种空间运动状态 |
| C.甲硫氨酸分子中碳原子的杂化类型有sp2和sp3 |
| D.甲硫氨酸分子间不能形成氢键 |
您最近一年使用:0次



