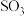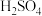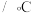名校
1 . 中国古代文献中记载了大量古代化学的研究成果,《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,反应原理为:S+2KNO3+3C===K2S+N2↑+3CO2↑。
(1)氮原子的价层电子排布图为___________ ,烟花燃放过程中,钾元素中的电子跃迁的方式是___________ ,K、S、N、O四种元素第一电离能由大到小的顺序为___________ 。上述反应涉及的元素中电负性最大的是___________ (填元素符号)。
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为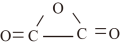 )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。
①C2O3中碳原子的杂化轨道类型为___________ ,CO2分子的立体构型为___________ 。
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是______________________ 。
③CO分子中π键与σ键个数比为___________ 。
(3)超氧化钾的晶胞结构图如下:

则与K+等距离且最近的K+个数为___________ ,若晶胞参数为dpm,则该超氧化物的密度为___________ g·cm-3(用含d、NA的代数式表示,设NA表示阿伏伽德罗常数的值)。
(1)氮原子的价层电子排布图为
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为
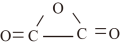 )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。①C2O3中碳原子的杂化轨道类型为
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是
③CO分子中π键与σ键个数比为
(3)超氧化钾的晶胞结构图如下:

则与K+等距离且最近的K+个数为
您最近一年使用:0次
2019-04-03更新
|
526次组卷
|
5卷引用:云南省大理州祥云四中2020届高三下学期3月线上模拟考试理综化学试题
2 . 碳、氧、硅、锗、氟、氯、溴、镍元素在化学中占有极其重要的地位。
(1)第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是________ 。
(2)从电负性角度分析,碳、氧和硅元素的非金属性由强至弱的顺序为____________________ 。
(3)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为__________________ 。
(4)基态锗(Ge)原子的电子排布式是____________ ,Ge的最高价氯化物分子式是________ 。该元素可能的性质或应用有________ (填字母)。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.锗的第一电离能高于碳而电负性低于碳
(5)溴与氯能以________ 键结合形成BrCl,BrCl分子中,________ 显正电性。BrCl与水发生反应的化学方程式为______________________________________________ 。
(1)第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
(2)从电负性角度分析,碳、氧和硅元素的非金属性由强至弱的顺序为
(3)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(4)基态锗(Ge)原子的电子排布式是
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.锗的第一电离能高于碳而电负性低于碳
(5)溴与氯能以
您最近一年使用:0次
2019-01-11更新
|
710次组卷
|
7卷引用:云南省剑川县第一中学2019-2020学年高二上学期期末考试化学试题
名校
3 . 若以E(nl)表示某能级的能量,以下各式中正确的是( )
| A.E(3s)>E(2s)>E(1s) | B.E(3s)>E(3p)>E(3d) |
| C.E(4f)>E(4s)>E(3d) | D.E(5s)>E(4s)>E(4f) |
您最近一年使用:0次
2019-01-02更新
|
475次组卷
|
4卷引用:云南省云龙县第二中学2019-2020学年高二上学期期末考试化学试题
名校
4 . 下面是第二周期部分元素基态原子的电子排布图,据此下列说法错误的是( )
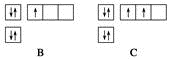



| A.每个原子轨道里最多只能容纳2个电子 |
| B.电子排在同一能级时,总是优先单独占据一个轨道 |
| C.每个能层所具有的能级数等于能层的序数(n) |
| D.若原子轨道里有2个电子,则其自旋状态相反 |
您最近一年使用:0次
2018-11-27更新
|
179次组卷
|
3卷引用:云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题
名校
5 . X、Y两元素可形成X2Y3型化合物,则X、Y原子最外层的电子排布可能是( )
| A.X:3s23p1 Y:3s23p5 | B.X:2s22p2 Y:2s22p4 |
| C.X:3s23p1 Y:3s23p4 | D.X:3s2 Y:2s22p3 |
您最近一年使用:0次
2018-09-28更新
|
196次组卷
|
6卷引用:云南省云龙县第二中学2019-2020学年高二上学期期末考试化学试题
解题方法
6 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____________________________ ,基态S原子电子占据最高能级的电子云轮廓图为________ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________________ 。
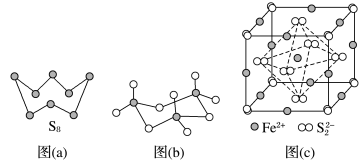
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为________ 形,其中共价键的类型有________ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为______________________________ g·cm-3;晶胞中Fe2+位于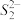 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为________ nm。
|
|
|
|
|
| |
熔点 | -85.5 | 115.2 |
(分解) | -75.5 | 16.8 | 10.3 |
沸点 | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为
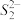 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
2018-09-23更新
|
263次组卷
|
7卷引用:云南省漾濞二中2020届高三上学期开学考试化学试题
7 . 下列有关电离能的说法,正确的是( )
| A.第一电离能越大的原子失电子的能力越强 |
| B.第一电离能是元素的原子失去核外第一个电子需要的能量 |
| C.同一周期中,主族元素原子第一电离能从左到右越来越大 |
| D.可通过一种元素各级电离能的数值,判断元素可能的化合价 |
您最近一年使用:0次
2018-08-02更新
|
282次组卷
|
7卷引用:云南省剑川县第一中学2019-2020学年高二上学期期末考试化学试题
8 . 在多电子原子中,轨道能量是由以下哪些因素决定( )
①能层 ②能级 ③电子云的伸展方向 ④电子自旋状态
①能层 ②能级 ③电子云的伸展方向 ④电子自旋状态
| A.①② | B.①④ | C.②③ | D.③④ |
您最近一年使用:0次
2018-04-06更新
|
459次组卷
|
11卷引用:云南省云龙县第二中学2019-2020学年高二上学期期末考试化学试题
云南省云龙县第二中学2019-2020学年高二上学期期末考试化学试题(已下线)2013-2014浙江省台州中学下学期第二次统练高二化学试卷2015-2016学年安徽省六安一中高二上学期期末化学试卷河南省安阳市林虑中学2017-2018学年高二4月份调研考试化学试题【全国百强校】内蒙古北方重工业集团有限公司第三中学2017-2018学年高二下学期期末考试化学试题上海市民星中学2018—2019学年高三上学期期中考试化学试题贵州省岑巩县第二中学2019-2020学年高二上学期期末考试化学试题云南省通海县第一中学2021-2022学年高二下学期3月月考化学试题云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题云南省瑞丽市第一民族中学2021-2022学年高二下学期3月月考化学试题陕西省西安市阎良区关山中学2021-2022学年高二下学期期末质量检测化学试题
名校
9 . 甲、乙两元素原子的L层电子数都是其他层电子总数的2倍。下列推断正确的是( )
| A.甲与乙位于同一周期 |
| B.甲与乙位于同一主族 |
| C.甲与乙都位于元素周期表的p区 |
| D.甲与乙的原子序数之和为偶数 |
您最近一年使用:0次
2018-02-12更新
|
503次组卷
|
10卷引用:云南省永平县第二中学2019-2020学年高二上学期期末考试化学试题
云南省永平县第二中学2019-2020学年高二上学期期末考试化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:第一章 综合检测1云南省曲靖市沾益二中2017-2018学年高二下学期期末考试化学试题吉林省白山市第七中学2018-2019学年高二下学期期中考试化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)四川省达州市第一中学校2022-2023学年高二上学期10月月考化学试题湖北省十堰市普通高中协作体2022-2023学年高二下学期3月月考化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题
名校
10 . 以下电子排布式是基态原子的电子排布的是( )
①1s12s1 ②1s22s12p1 ③1s22s22p63s2 ④1s22s22p63s23p1
①1s12s1 ②1s22s12p1 ③1s22s22p63s2 ④1s22s22p63s23p1
| A.①② | B.①③ | C.②③ | D.③④ |
您最近一年使用:0次
2018-02-11更新
|
1146次组卷
|
11卷引用:云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题
云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题宁夏吴忠市2017-2018学年高二人教版选修3化学同步练习:第1章 原子结构与性质综合练习1人教版2017-2018学年高二化学选修三同步训练:1.1 原子结构(第2课时)云南省泸水五中2018-2019学年高二上学期期中考试化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二下学期第一次调研化学试题云南省金平县第一中学2019-2020学年高二上学期期末考试化学试题山西省运城市永济涑北中学2019-2020学年高二下学期3月月考化学试题陕西省咸阳百灵学校2019-2020学年高二下学期第二次月考化学试题(人教版2019)选择性必修2 第一章 原子结构与性质 第一节 原子结构云南省玉溪市江川区第一中学2021-2022学年高二下学期3月月考化学试题云南省西双版纳傣族自治州第一中学2022-2023学年高二下学期期末考试化学试题