解题方法
1 . 胆矾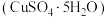 可写为
可写为 ,其结构示意图如图所示:
,其结构示意图如图所示:
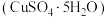 可写为
可写为 ,其结构示意图如图所示:
,其结构示意图如图所示: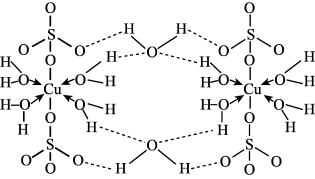
A.胆矾晶体中存在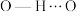 氢键 氢键 | B.胆矾晶体中 的配位数是4 的配位数是4 |
C.基态 的价层电子排布式为 的价层电子排布式为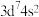 | D.五水硫酸铜晶体是一种含水混合物 |
您最近一年使用:0次
解题方法
2 . 离子液体有独特的优良性能。某离子液体 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是
 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是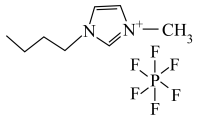
A.第一电离能: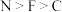 | B. 原子的杂化轨道类型均为 原子的杂化轨道类型均为 |
C. 中所含 中所含 键的数目为 键的数目为 | D.最简单氢化物的沸点: |
您最近一年使用:0次
2024·云南昆明·三模
3 . W、X、Y、Z是原子序数依次增大的四种短周期主族元素。W的原子半径最小,基态X原子的最外层有3个未成对电子,Y与Z同族,由这四种元素与Ce元素组成的化合物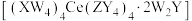 是分析化学常用的滴定剂。下列说法错误的是
是分析化学常用的滴定剂。下列说法错误的是
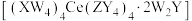 是分析化学常用的滴定剂。下列说法错误的是
是分析化学常用的滴定剂。下列说法错误的是| A.第一电离能:X>Y>Z |
| B.与W形成的最简单化合物的沸点:Y>Z |
C.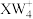 、 、 的空间构型均为正四面体形 的空间构型均为正四面体形 |
D.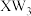 、 、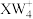 中心原子杂化方式和键角均相同 中心原子杂化方式和键角均相同 |
您最近一年使用:0次
名校
解题方法
4 . LiDFOB是一种新型的电解质锂盐,被广泛用于目前的锂电池中。LiDFOB的结构如图所示,其中元素M、X、Y、Z位于同一短周期且原子序数依次增大,X原子核外的s轨道与p轨道上的电子数之比为2:1,下列叙述正确的是
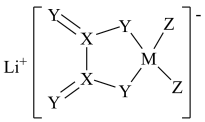
| A.基态Z原子核外有5种能量不同的电子 |
| B.该化合物中有极性键、非极性键、配位键和离子键 |
| C.第一电离能:Z>X>Y>M |
| D.M、X、Y、Z中,Z的最高价氧化物对应的水化物酸性最强 |
您最近一年使用:0次
2024-05-12更新
|
101次组卷
|
2卷引用:云南省昆明市云南师范大学附属中学2023-2024学年高三下学期适应性月考(九)理综试卷-高中化学
名校
解题方法
5 . 长周期元素M的一种配合物对某些有机反应具有优良的催化性能,其结构可用下图表示,其中W、X、Y、Z为原子序数依次增加的短周期元素,M和Z的简单离子的电子层结构相同,下列叙述错误的是
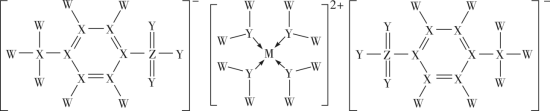
| A.简单离子半径:Z>M |
| B.电负性:Y>X>W>M |
| C.W、X、Y、Z均为元素周期表中p区元素 |
D.该配合物中X原子的轨道杂化类型为 、 、 |
您最近一年使用:0次
6 . 废弃电脑的CPU中含有贵重金属Cu、Ag、Au,可回收利用,部分流程如下:

(1)铜元素在周期表中位于______ ,基态铜原子的核外电子排布式为______ 。
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
(3)用Zn粉还原 的化学反应方程式为
的化学反应方程式为______ ;
(4)试剂1为______ (填名称,下同),试剂2为______ ;
(5)加入过其铁粉的原因是______ ;
(6)滤渣2溶于试剂2的原因是______ ;(用离子反应方程式表示)
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为______  (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

(1)铜元素在周期表中位于
(2)电脑CPU在使用时会涂抹一层散热硅脂(一种液体橡胶,主要成分为聚二甲基硅氧烷和聚甲基硅氧烷),可用______洗去;
| A.NaOH溶液 | B.纯碱溶液 | C.稀硫酸 | D.酒精 |
(3)用Zn粉还原
 的化学反应方程式为
的化学反应方程式为(4)试剂1为
(5)加入过其铁粉的原因是
(6)滤渣2溶于试剂2的原因是
(7)金属铜的晶胞结构如图所示,铜原子之间的最小距离为apm,则铜晶胞的密度为
 (
( 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近一年使用:0次
名校
7 . 黑火药的主要成分为木炭(C)、硫黄(S)和火硝(KNO3).请回答下列问题。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为___________ 形。
(2)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为___________ 。
(3)C、N、O、K四种元素的第一电离能由大到小的顺序为___________ 。
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为___________ ;
②H2Se的中心原子杂化类型是:___________ , SeO32-的立体构型是___________ ;
③比较H2S与H2O沸点高低,并说明原因:___________ 。
(1)基态碳原子的电子占据最高能级的电子云轮廓图为
(2)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态N原子的电子自旋磁量子数的代数和为(3)C、N、O、K四种元素的第一电离能由大到小的顺序为
(4)O、S、Se、Te同主族元素,Te位于第五周期
①基态Te原子价电子排布式为
②H2Se的中心原子杂化类型是:
③比较H2S与H2O沸点高低,并说明原因:
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语或图示表达正确的是
| A.基态25Mn的价电子3d44s2 |
| B.PCl3分子的空间结构模型:正四面体 |
C.2pz的电子云轮廓图: |
D.基态氧原子的轨道表示式: 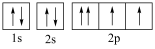 |
您最近一年使用:0次
解题方法
9 . 尿素 可与正烷烃形成超分子,原理如图所示。下列说法错误的是
可与正烷烃形成超分子,原理如图所示。下列说法错误的是
 可与正烷烃形成超分子,原理如图所示。下列说法错误的是
可与正烷烃形成超分子,原理如图所示。下列说法错误的是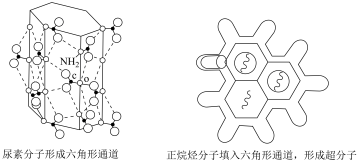
| A.尿素分子中各元素的电负性:O>N>C>H |
| B.尿素分子通过分子间氢键形成六角形通道结构 |
| C.依据分子直径的大小差异可分离同碳数正烷烃和支链烷烃 |
| D.该超分子能稳定存在的原因是尿素分子和正烷烃分子通过共价键结合使能量降低、熵减小 |
您最近一年使用:0次
2024-04-18更新
|
152次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
名校
解题方法
10 . 现有A、B、C、D、E、F六种元素,均为前4周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)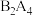 的电子式为
的电子式为___________ (用元素符号表示,下同)。
(2)C元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)某同学推断D元素基态原子的轨道表示式为: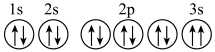 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了___________ (填序号)。
a.泡利不相容原理 b.洪特规则
(4)C、D、E三种元素的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(5)其中五种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈狭长的八面体结构(如下图所示)。阳离子中存在的化学键类型有___________ (填序号)。
该化合物加热时阳离子首先失去的组分是___________ (填化学式),判断理由是___________ 。
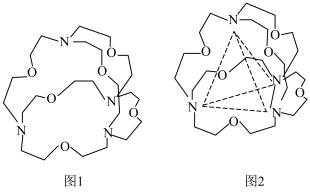
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________ (填标号)。 b.
b. c.
c. d.
d.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素基态原子的核外p电子数比s电子数少1 |
| C元素基态原子的核外p轨道中有两个未成对电子 |
D元素的气态基态原子的第一至第四电离能分别是: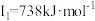 , ,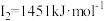 , ,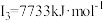 , ,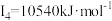 |
| E元素的主族序数比周期数大3 |
| F元素位于元素周期表中的第11列 |
(1)
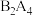 的电子式为
的电子式为(2)C元素的原子核外共有
(3)某同学推断D元素基态原子的轨道表示式为:
 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了a.泡利不相容原理 b.洪特规则
(4)C、D、E三种元素的简单离子半径由大到小的顺序是
(5)其中五种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,阳离子呈狭长的八面体结构(如下图所示)。阳离子中存在的化学键类型有

该化合物加热时阳离子首先失去的组分是
(6)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
 b.
b. c.
c. d.
d.
您最近一年使用:0次



