名校
解题方法
1 . 碲具有独特的理化性质,被广泛应用于军工、航天、石油化工、冶金等领域。从碲铜渣[主要成分为 ,含Bi(Ⅲ)、Sb(Ⅲ)、Pb(Ⅱ)、Se等杂质]中分离提纯碲的一种流程如下图所示。
,含Bi(Ⅲ)、Sb(Ⅲ)、Pb(Ⅱ)、Se等杂质]中分离提纯碲的一种流程如下图所示。
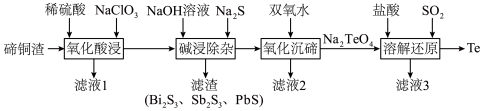
回答下列问题:
(1)“氧化酸浸”时,
 发生反应生成难溶的
发生反应生成难溶的 ,该反应的化学方程式为
,该反应的化学方程式为(2)已知“碱浸除杂”所得浸出液中硒和碲的化合价相同,“氧化沉碲”的目的是利用钠盐的溶解性差异分离硒和碲,推测滤液2中硒的存在形式是
 表面吸附的杂质,将其置于氢氧化钠溶液中进行常温漂洗,漂洗液与滤液2合并,经煮沸后可返回上述流程中的
表面吸附的杂质,将其置于氢氧化钠溶液中进行常温漂洗,漂洗液与滤液2合并,经煮沸后可返回上述流程中的(3)
 在“溶解还原”工序中生成单质Te的总反应的离子方程式为
在“溶解还原”工序中生成单质Te的总反应的离子方程式为(4)滤液1、2、3中,含铜量较高,可用于回收铜的是
(5)碲是第五周期氧族元素,其基态原子的价层电子排布式为
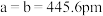 、
、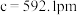 ,
, ,
,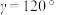 ,碲晶体的密度为
,碲晶体的密度为 (列出计算式即可)。
(列出计算式即可)。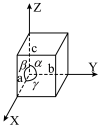
您最近一年使用:0次
名校
2 . 一种性能优越的高分子材料的结构如图所示。其中,W、X、Y、Z为原子序数依次增大的短周期元素,基态Y、Z原子核外电子运动的空间状态均有5个。下列说法正确的是

| A.X、Y、Z分别与W形成的简单化合物中,X的最稳定 |
| B.四种元素中Y的第一电离能最大,Z的电负性最大 |
| C.仅由上述四种元素不可能形成离子化合物 |
| D.该高分子中不存在大π键 |
您最近一年使用:0次
名校
3 . 按要求完成下列小题。
(1)Cu2+基态核外电子排布式为_______ 。
(2)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Mn原子未成对的电子数为_______ 。
②第三电离能I3(Fe)<I3(Mn),原因是_______ 。
(3)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为_______
②H2O分子的空间结构分别是_______ ,键角H2O_______ NH3。(填>、<或=)
(1)Cu2+基态核外电子排布式为
(2)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Mn原子未成对的电子数为
②第三电离能I3(Fe)<I3(Mn),原因是
(3)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为
②H2O分子的空间结构分别是
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语表达错误的是
| A.N原子核外电子有7种空间运动状态 |
B. 的结构式: 的结构式: |
C. 的结构示意图: 的结构示意图: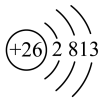 |
D.基态Cr原子的价层电子轨道表示式: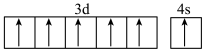 |
您最近一年使用:0次
2024-03-22更新
|
336次组卷
|
3卷引用:云南省开远市第一中学校2023-2024学年高二下学期3月月考化学试题
解题方法
5 . 有A、B、C、D、E五种元素。其相关信息如下:
回答下列问题:
(1)E元素原子基态时的外围电子排布式为_____ 。
(2)C元素的第一电离能比氧元素的第一电离能_____ (填“大”或“小”),原因是_____ 。
(3)C2A4分子中C原子的杂化轨道类型是_____ 。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_____ (填序号)。
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_____ (填字母)。
a.平面正方形 b.正四面体 c.三角锥形 d.V形
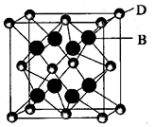
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为_____ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能与氧形成砖红色E2O和黑色的EO两种氧化物 |
(1)E元素原子基态时的外围电子排布式为
(2)C元素的第一电离能比氧元素的第一电离能
(3)C2A4分子中C原子的杂化轨道类型是
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键
[E(CA3)4]2+具有对称的空间构型,若[E(CA3)4]2+中的两个CA3被两个其他基团取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为

您最近一年使用:0次
名校
解题方法
6 . 下列有关化学用语表示错误的是
A.氯气的共价键电子云轮廓图: |
B.二氧化硅的分子式为 |
C. 的电子式: 的电子式: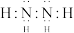 |
D.氯碱工业原理: |
您最近一年使用:0次
7 . 下列有关说法正确的是
A.元素的电负性: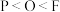 |
B.因为二氧化硅的相对分子质量比二氧化碳大,所以沸点: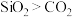 |
C. 、 、 、 、 三种离子晶体的熔点: 三种离子晶体的熔点: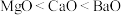 |
D.稳定性: ,是因为水分子间存在氢键的缘故 ,是因为水分子间存在氢键的缘故 |
您最近一年使用:0次
名校
解题方法
8 . W、X、Y、Z是原子序数依次增大的短周期主族元素,W原子的核外电子只有一种运动状态,X基态原子最外层电子数是内层电子数的三倍,Y的氧化物常用作耐火材料,且基态原子s能级的电子总数等于p能级的电子总数,Z的最高价氧化物对应的水化物是酸性最强的含氧酸,是同周期电负性最大的元素。下列说法错误的是
A.W与X形成的简单氢化物中X原子是 杂化 杂化 |
| B.Y的第一电离能高于同周期相邻两种元素 |
C.简单离子的半径 |
| D.Z元素核外电子的空间运动状态有9种 |
您最近一年使用:0次
9 . 下列化学用语或图示表达正确的是
A.Cr的简化电子排布式: | B.Al原子的最高能级原子轨道形状: |
C.乙烯的结构简式: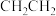 | D.基态N原子的轨道表示式: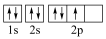 |
您最近一年使用:0次
10 . 完成下列问题。
(1)基态氧原子的电子排布式为_______ 。
(2)基态 原子中,电子占据的最高能层符号为
原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为______ ,电子数为_____ 。
(3) 的价电子排布图为
的价电子排布图为______ 。
(1)基态氧原子的电子排布式为
(2)基态
 原子中,电子占据的最高能层符号为
原子中,电子占据的最高能层符号为(3)
 的价电子排布图为
的价电子排布图为
您最近一年使用:0次



