名校
解题方法
1 . X、Y、Z三种元素基态原子的价电子排布式分别为 、
、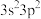 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是
 、
、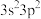 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是A. | B.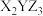 | C.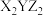 | D. |
您最近一年使用:0次
2024-04-04更新
|
145次组卷
|
10卷引用:云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题
云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题湖南省汨罗市楚雄中学2021-2022学年高二12月月考化学试题2014-2015河南省实验中学高二下学期期中考试化学试卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题四川省广元中学2021-2022学年高二下学期第一次段考化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题甘肃省武山县第一高级中学2023-2024学年高二下学期第一次月考化学试卷
2 . 金属铜、铁在日常生活中应用广泛,根据下列说法回答下列问题。
(1) 的制备反应为
的制备反应为 。
。
上述氧化过程中, (II)
(II)_____ (答简化电子排布式)变为 III)
III)_____ (答外围电子排布图),基态 (III)电子占据
(III)电子占据_____ 个不同轨道。
(2)对上述反应式中的短周期元素按照电负性由小到大排序为_____
(3)配合物 的配位数为6,其配体
的配位数为6,其配体 中的
中的 的杂化方式为
的杂化方式为_____ 杂化。
(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。
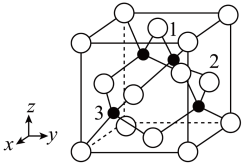
①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于_____ (填“离子”或“共价”)化合物。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为( ,
, ,1),则原子2和3的坐标分别为
,1),则原子2和3的坐标分别为_____ 、_____ 。
③已知该晶体的密度为 ,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为_____ pm(只写计算式)。
(1)
 的制备反应为
的制备反应为 。
。上述氧化过程中,
 (II)
(II) III)
III) (III)电子占据
(III)电子占据(2)对上述反应式中的短周期元素按照电负性由小到大排序为
(3)配合物
 的配位数为6,其配体
的配位数为6,其配体 中的
中的 的杂化方式为
的杂化方式为(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。

①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为(
 ,
, ,1),则原子2和3的坐标分别为
,1),则原子2和3的坐标分别为③已知该晶体的密度为
 ,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为
您最近一年使用:0次
3 . 钛(Ti)及其化合物的应用研究是目前前沿科学之一,请回答下列问题:
(1)基态钛原子的电子排布式为_______ 。
(2) 作光催化剂可将甲醛、苯等有害气体转化为
作光催化剂可将甲醛、苯等有害气体转化为 和
和 。上述含碳原子的分子中,碳原子的杂化方式为
。上述含碳原子的分子中,碳原子的杂化方式为 的是
的是_______ (填名称)。
(3)作为过渡元素的Fe、Cu容易形成配位化合物,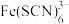 中C、N两种元素的电负性大小关系为
中C、N两种元素的电负性大小关系为_______ 。硫酸铜稀溶液中微粒间不存在的作用力有_______ (填序号)。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(4)已知Ba、Mo的氯化物沸点信息如下表所示。二者沸点差异的原因是_______ 。
(5) 分子中H-N-H的键角为107°,在
分子中H-N-H的键角为107°,在 中,H-N-H键角近似109.5°,键角变大的原因是
中,H-N-H键角近似109.5°,键角变大的原因是_______ 。
(6)贵金属磷化物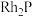 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为_______ ,晶体的密度为_______  。(列出计算式即可)。
。(列出计算式即可)。

(1)基态钛原子的电子排布式为
(2)
 作光催化剂可将甲醛、苯等有害气体转化为
作光催化剂可将甲醛、苯等有害气体转化为 和
和 。上述含碳原子的分子中,碳原子的杂化方式为
。上述含碳原子的分子中,碳原子的杂化方式为 的是
的是(3)作为过渡元素的Fe、Cu容易形成配位化合物,
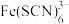 中C、N两种元素的电负性大小关系为
中C、N两种元素的电负性大小关系为A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(4)已知Ba、Mo的氯化物沸点信息如下表所示。二者沸点差异的原因是
| 氯化物 | 沸点 |
 | 1560℃ |
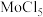 | 268℃ |
(5)
 分子中H-N-H的键角为107°,在
分子中H-N-H的键角为107°,在 中,H-N-H键角近似109.5°,键角变大的原因是
中,H-N-H键角近似109.5°,键角变大的原因是(6)贵金属磷化物
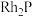 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为 。(列出计算式即可)。
。(列出计算式即可)。
您最近一年使用:0次
4 . 当镁原子由1s22s22p63s2跃迁到1s22s22p63p2时,以下认识正确的是
| A.镁原子由基态转化成激发态,这一过程中吸收热量 |
| B.镁原子由基态转化成激发态,这一过程中释放热量 |
| C.转化后位于p能级上的两个电子的能量没有发生任何变化 |
| D.转化后镁原子与硅原子电子层结构相同,化学性质相似 |
您最近一年使用:0次
2022-04-12更新
|
27次组卷
|
2卷引用:云南省玉溪市通海县第二中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
5 . 已知A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大。A原子、C原子的L能层中都有两个未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)D的最高价氧化物的空间构型为_________ 。
(2)E2+的价层电子排布图是___________ ,F原子的电子排布式是___________ 。
(3)A的最高价氧化物对应的水化物分子结构式为_______ ,其中心原子采取的轨道杂化方式为_________ ,B的简单气态氢化物的空间构型经过分析为三角锥形,判断依据是_________ 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,含DAB-的水溶液可以用于实验室中E3+的定性检验,检验E3+的离子方程式为________ 。
(1)D的最高价氧化物的空间构型为
(2)E2+的价层电子排布图是
(3)A的最高价氧化物对应的水化物分子结构式为
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,含DAB-的水溶液可以用于实验室中E3+的定性检验,检验E3+的离子方程式为
您最近一年使用:0次
6 . 填空。
(1)基态X原子的第二电子层上只有一个空轨道,则X是___________ ,其电子排布图为___________ ;Y原子的核电荷数为33,其价层电子排布式是___________ ,其在元素周期表中的位置属于___________ 区的元素。
(2)德国和美国科学家首次研制出了由20个碳原子构成的空心笼状分子C20,该笼状结构是由多个正五边形构成的(如图所示)。请回答:
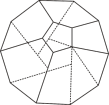
①C20分子中共有_______ 个正五边形,共有_______ 条棱。C20晶体属于________ (填晶体类型)。
②固体C60与C20相比较,熔点较高的应为_______ ,理由是________ 。
(3)在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空院中,晶胞如图所示。

①该晶体的化学式为___________ 。
②若取碳原子为晶胞顶点,则镍原子位于晶胞的_________ 位置。
(4)白磷分子中P—P键易断开,若一个白磷分子( )中的每个P—P键均断开插入一个氧原子,则一共可结合
)中的每个P—P键均断开插入一个氧原子,则一共可结合________ 个氧原子,这样得到磷的一种氧化物,其分子式为_________ 。由C、H、N三种元素组成的某化合物CxHyNz,其分子内含4个氮原子排成的内空的正四面体(同白磷),每两个氮原子间都有一个碳原子,且分子内无C—C键和C=C键,则化合物的分子式为________ 。
(1)基态X原子的第二电子层上只有一个空轨道,则X是
(2)德国和美国科学家首次研制出了由20个碳原子构成的空心笼状分子C20,该笼状结构是由多个正五边形构成的(如图所示)。请回答:

①C20分子中共有
②固体C60与C20相比较,熔点较高的应为
(3)在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空院中,晶胞如图所示。

①该晶体的化学式为
②若取碳原子为晶胞顶点,则镍原子位于晶胞的
(4)白磷分子中P—P键易断开,若一个白磷分子(
 )中的每个P—P键均断开插入一个氧原子,则一共可结合
)中的每个P—P键均断开插入一个氧原子,则一共可结合
您最近一年使用:0次
名校
7 . 13Al、12Mg、16S、17Cl是周期表中的短周期主族元素。下列有关说法正确的是
A.第一电离能: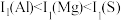 |
| B.H2S中S的杂化轨道类型为sp2 |
| C.元素S在周期表中位于第3周期IVA族 |
| D.最高价氧化物的水化物的碱性:Mg(OH)2<Al(OH)3 |
您最近一年使用:0次
名校
解题方法
8 . 下列有关化学用语正确的是
A.Cr原子的价电子排布图: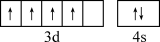 |
B.NaH的电子式: |
| C.Ca2+基态电子排布式:1s22s22p63s23p6 |
D.F原子的结构示意图: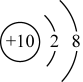 |
您最近一年使用:0次
名校
解题方法
9 . 已知X、Y为同周期非金属元素,且电负性Y>X,下列说法正确的是
| A.化学键的极性:H—Y大于H—X |
| B.第一电离能Y一定大于X |
| C.含氧酸的酸性:Y对应的酸的酸性强于X对应的酸的酸性 |
| D.X和Y形成化合物时,X显负价,Y显正价 |
您最近一年使用:0次
解题方法
10 . 2020年9月,中国向联合国大会宣布“30.60目标”,即二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。目前我国正在大力发展新能源车。磷酸铁锂电池主要成分为LiFePO4,可采用二价铁盐或三价铁盐、H3PO4、NH3∙H2O等作为原料制备。
(1)H3PO4中PO 空间构型为
空间构型为___________
(2)Fe2+的电子排布式为___________ 。Fe3+比Fe2+更稳定的原因是___________ 。
(3)NH3和PH3结构相似,但NH3易溶于水,PH3难溶于水,原因是___________
(4)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
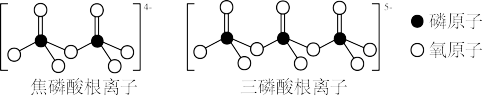
这类磷酸根离子的化学式可用通式表示为___________ (用n代表P原子数)。
(5)石墨可用作锂离子电池的负极材料,Li+嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物。某石墨嵌入化合物的平面结构如图甲所示,则x=___________ ;若每个六元环都对应一个Li+,则化学式为___________ 。
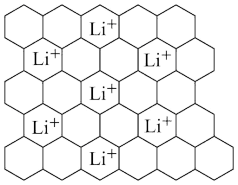
甲
(6)某金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,阴离子是由12个硼原子和12个氢原子所构成的离子团。阴离子在晶胞中的位置如图乙所示,其堆积方式为___________ ,Li+占据阴离子组成的所有正四面体空隙中心,该化合物的化学式为___________ (用最简整数比表示)。假设晶胞边长为a nm,则该晶胞的密度为___________ g/cm-3(用含a、NA的代数式表示)。
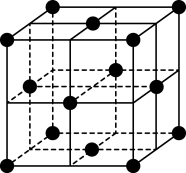
乙
(1)H3PO4中PO
 空间构型为
空间构型为(2)Fe2+的电子排布式为
(3)NH3和PH3结构相似,但NH3易溶于水,PH3难溶于水,原因是
(4)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:

这类磷酸根离子的化学式可用通式表示为
(5)石墨可用作锂离子电池的负极材料,Li+嵌入石墨的两层间,导致石墨的层堆积方式发生改变,形成化学式为LixC6的嵌入化合物。某石墨嵌入化合物的平面结构如图甲所示,则x=

甲
(6)某金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,阴离子是由12个硼原子和12个氢原子所构成的离子团。阴离子在晶胞中的位置如图乙所示,其堆积方式为

乙
您最近一年使用:0次



