1 . 一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是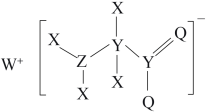
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近一年使用:0次
2024-04-08更新
|
63次组卷
|
2卷引用:云南省大理州实验中学2021-2022学年高二下学期化学期中考试题
名校
解题方法
2 . X、Y、Z三种元素基态原子的价电子排布式分别为 、
、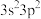 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是
 、
、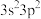 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是A. | B.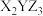 | C.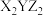 | D. |
您最近一年使用:0次
2024-04-04更新
|
145次组卷
|
10卷引用:云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题
云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题2014-2015河南省实验中学高二下学期期中考试化学试卷云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题湖南省汨罗市楚雄中学2021-2022学年高二12月月考化学试题四川省广元中学2021-2022学年高二下学期第一次段考化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题甘肃省武山县第一高级中学2023-2024学年高二下学期第一次月考化学试卷
解题方法
3 . 短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法正确的是
| 元素 |  |  |  |  |
| 最高价氧化物的水化物 | 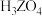 | |||
 溶液对应的pH(25℃) 溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
| A.X、W最简单氢化物的键角:X>W |
| B.简单离子半径:W<Y |
| C.元素电负性、第一电离能:Z<W |
| D.简单氢化物的沸点:X<Z |
您最近一年使用:0次
2024-02-02更新
|
76次组卷
|
4卷引用:云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷
云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省浏阳市2023-2024学年高二上学期期末质量监测考试化学试题江西省上饶市广丰一中2023-2024学年高三上学期12月考试化学试卷
4 . 铜和三氧化二铁在工农业生产中用途广泛。用黄铜矿(主要成分为 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
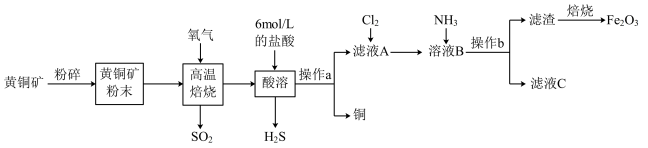
回答下列问题:
(1)铜的价电子排布式____________ 。
(2)高温焙烧时发生的反应是 ,1mol
,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子____________ mol。
(3)向滤液A中通入 的目的是
的目的是________________________________________________ 。
(4)向溶液B中通入 后发生反应的离子方程式为
后发生反应的离子方程式为_____________________________________________ 。
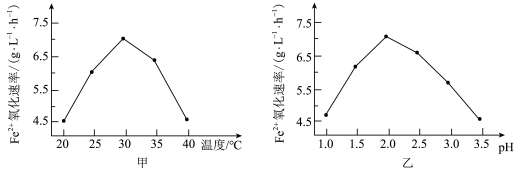
(5)工业上用生物法处理 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)
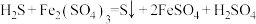
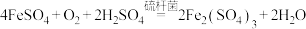
由图甲和图乙判断使用硫杆菌的最佳条件为___________________ 。若反应温度过高,反应速率下降,其原因是_______________________________________________ 。
 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
回答下列问题:
(1)铜的价电子排布式
(2)高温焙烧时发生的反应是
 ,1mol
,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子(3)向滤液A中通入
 的目的是
的目的是(4)向溶液B中通入
 后发生反应的离子方程式为
后发生反应的离子方程式为(5)工业上用生物法处理
 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)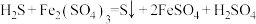
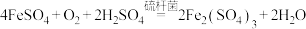
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
解题方法
5 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1) 的价电子排布图为:
的价电子排布图为:_________________________ ,基态磷原子的所有电子中有________ 种空间运动状态。
(2)Li、O、P三种元素的电负性由大到小的顺序是:________________________ 。
(3)无水硫酸铜为白色粉末溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有___________ 。
A.配位键 B.金属键 C.离子键 D.共价键
E.氢键 F.范德华力
(4)N和P是同主族元素,但是 分子中的键角大子
分子中的键角大子 分子中的键角,原因是:
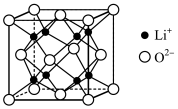
分子中的键角,原因是:___________________________________________ 。 为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为
为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为____________  (列出计算式即可),
(列出计算式即可), 和
和 的最短距离等于
的最短距离等于____________ nm(用含b的代数式表示)。
(1)
 的价电子排布图为:
的价电子排布图为:(2)Li、O、P三种元素的电负性由大到小的顺序是:
(3)无水硫酸铜为白色粉末溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有
A.配位键 B.金属键 C.离子键 D.共价键
E.氢键 F.范德华力
(4)N和P是同主族元素,但是
 分子中的键角大子
分子中的键角大子 分子中的键角,原因是:
分子中的键角,原因是: 为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为
为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为 (列出计算式即可),
(列出计算式即可), 和
和 的最短距离等于
的最短距离等于
您最近一年使用:0次
6 . 下列关于原子核外电子排布与元素在周期表中位置关系的表述正确的是
A.原子的价电子排布式为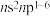 的元素一定是主族元素 的元素一定是主族元素 |
B.氯化钠晶体中,每个 周围与它距离相等且最近的 周围与它距离相等且最近的 有6个 有6个 |
| C.因同周期主族元素的原子半径从左到右逐渐减小,故其第一电离能逐渐增大 |
D. 是一种非常稳定的化合物,是由于水分子间形成氢键所致 是一种非常稳定的化合物,是由于水分子间形成氢键所致 |
您最近一年使用:0次
7 . X、Y、Z、W为原子序数依次增大的前四周期主族元素,四种元素中仅X、Y在同一周期,它们形成的一种物质的结构如图所示,其中所有原子均形成了8电子稳定结构。下列推断中正确的是
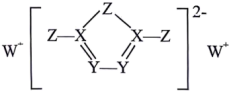
| A.X的氢化物常温下一定是气体 | B.1mol上述物质中,含有的 数目为7 数目为7 |
| C.Y的含氧酸的酸性一定比Z的含氧酸弱 | D.元素的第一电离能:X<Y<W |
您最近一年使用:0次
2023-12-21更新
|
307次组卷
|
2卷引用:云南省昭通市云天化中学教研联盟2023-2024学年高二上学期期中考试化学试题
解题方法
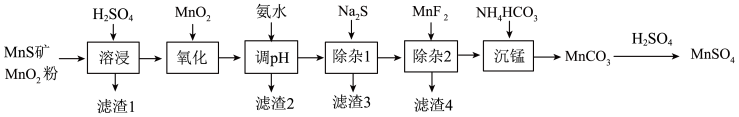
8 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
(1)Fe2+的价电子排布式为_______ ,在元素周期表中Zn处于_______ 区。
(2)“滤渣1”含有S和_______ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______ 。
(3)“氧化”中添加适量的MnO2的作用是_______ 。
(4)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(5)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是_______ 。
(6)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_______ 。
(7)写出“沉锰”的离子方程式_______ 。
(8)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y= 时,z=
时,z=_______ 。

相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)Fe2+的价电子排布式为
(2)“滤渣1”含有S和
(3)“氧化”中添加适量的MnO2的作用是
(4)“调pH”除铁和铝,溶液的pH范围应调节为
(5)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(6)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(7)写出“沉锰”的离子方程式
(8)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=
 时,z=
时,z=
您最近一年使用:0次
2023-12-15更新
|
280次组卷
|
4卷引用:云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷
云南省腾冲市2022-2023学年高三上学期期中教育教学质量监测理科综合试卷江西省上饶市清源学校2023-2024学年高三上学期12月考试化学试题(已下线)T15-工业流程题(已下线)T15-工业流程题
9 . 氮掺杂碳层包覆纳米金催化剂(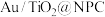 )催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
)催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
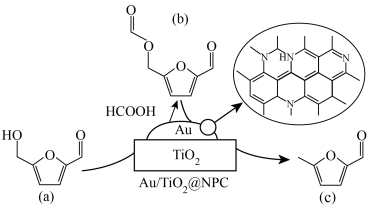
下列说法正确的是
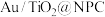 )催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
)催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
下列说法正确的是
A.第一电离能: |
B.图示反应过程中有 键的断裂和形成 键的断裂和形成 |
C.基态 原子的价层电子排布式为 原子的价层电子排布式为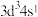 |
D.若 换成 换成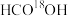 ,则(b)为 ,则(b)为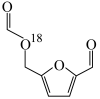 |
您最近一年使用:0次
10 . NCM是三元锂电池最重要的前驱体材料,一种以镍钴杂料(主要成分为 、
、 、
、 ,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
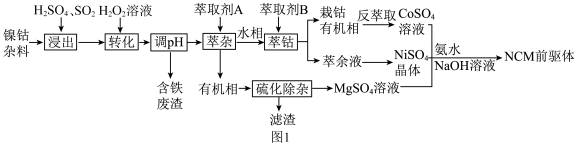
回答下列问题:
(1)基态钴原子核外未成对电子数与基态锰原子核外未成对电子数之比为___________ 。
(2)为提高“浸出”效率,可采取的措施有___________ (写出一条即可);“浸出”过程中 的作用是
的作用是___________ (用离子方程式表示)。
(3)常温下,若“转化”后的溶液中 浓度为
浓度为 ,在“调
,在“调 ”过程中,当
”过程中,当 调节到2.2时,开始出现
调节到2.2时,开始出现 沉淀,若要使
沉淀,若要使 完全沉淀,则调节溶液
完全沉淀,则调节溶液 最小为
最小为___________ [已知:当c(Fe3+)≤1×10-5mol/L时,认为 沉淀完全]
沉淀完全]
(4)有机萃取剂P204和P507对金属离子的萃取率与pH的关系如图2、图3所示。
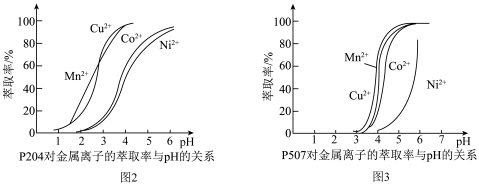
①萃取剂A是___________ (填“P204”或“P507”,下同),萃取剂B是___________ 。
②进行“萃钴”操作前,需对水相调pH至___________ (填标号),以达到最佳萃取 的效果。
的效果。
a.2.5 b.3.5 c.4.5 d.5.5
③萃取剂萃取 的原理为2HR(有机相)
的原理为2HR(有机相)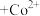 (水相)
(水相)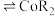 (有机相)
(有机相) (水相),则反萃取操作中可向载钴有机相中加入
(水相),则反萃取操作中可向载钴有机相中加入___________ (填试剂名称)得到含 的溶液;一定条件下,萃取平衡时,溶液中
的溶液;一定条件下,萃取平衡时,溶液中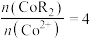 ,则
,则 的萃取率为
的萃取率为___________ 。
(5)一种NiAs晶体结构如图4所示。
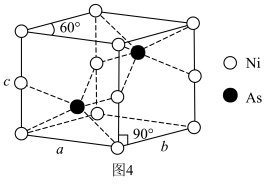
通过X射线光谱测算出该晶胞参数为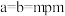 ,
,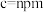 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶体密度为
,则该晶体密度为___________ (填含m、n和 的表达式)
的表达式) 。
。
 、
、 、
、 ,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
回答下列问题:
(1)基态钴原子核外未成对电子数与基态锰原子核外未成对电子数之比为
(2)为提高“浸出”效率,可采取的措施有
 的作用是
的作用是(3)常温下,若“转化”后的溶液中
 浓度为
浓度为 ,在“调
,在“调 ”过程中,当
”过程中,当 调节到2.2时,开始出现
调节到2.2时,开始出现 沉淀,若要使
沉淀,若要使 完全沉淀,则调节溶液
完全沉淀,则调节溶液 最小为
最小为 沉淀完全]
沉淀完全](4)有机萃取剂P204和P507对金属离子的萃取率与pH的关系如图2、图3所示。

①萃取剂A是
②进行“萃钴”操作前,需对水相调pH至
 的效果。
的效果。a.2.5 b.3.5 c.4.5 d.5.5
③萃取剂萃取
 的原理为2HR(有机相)
的原理为2HR(有机相)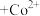 (水相)
(水相)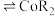 (有机相)
(有机相) (水相),则反萃取操作中可向载钴有机相中加入
(水相),则反萃取操作中可向载钴有机相中加入 的溶液;一定条件下,萃取平衡时,溶液中
的溶液;一定条件下,萃取平衡时,溶液中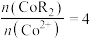 ,则
,则 的萃取率为
的萃取率为(5)一种NiAs晶体结构如图4所示。

通过X射线光谱测算出该晶胞参数为
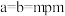 ,
,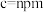 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶体密度为
,则该晶体密度为 的表达式)
的表达式) 。
。
您最近一年使用:0次



