1 . 元素周期表被认为是“科学共同的语言”,它的发现使化学学习和研究变得有规律可循。其简洁有序的背后,是众多科学家艰苦奋斗的结果。下图是元素周期表的一部分,请按要求回答下列问题:

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为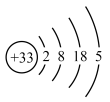 ,砷在周期表中的位置是
,砷在周期表中的位置是___________ 。我国“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。原子半径:Ga___________ As(填“>”或“<”)。
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途___________ 。
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为___________ (填化学式)。
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是___________ 。
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
(6)小赵同学在研究元素周期表时发现,碳元素有“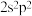 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是___________ 。

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为
 ,砷在周期表中的位置是
,砷在周期表中的位置是(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
| A.“类钫”在化合物中显+1价 |
| B.“类钫”单质具有强氧化性 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 |
| D.“类钫”单质能与冷水剧烈反应 |
(6)小赵同学在研究元素周期表时发现,碳元素有“
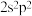 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是
您最近一年使用:0次
名校
2 . 硅材料在生活中占有重要地位。Si(NH2)4(结构如图所示)受热分解可生成Si3N4和NH3。Si3N4是一种优良的耐高温结构陶瓷。下列有关说法错误的是
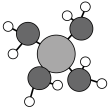

| A.电负性N>Si |
| B.Si3N4属于分子晶体 |
| C.基态Si和N原子的未成对电子数之比为2:3 |
| D.Si(NH2)4中的Si、N原子轨道的杂化类型相同 |
您最近一年使用:0次
2024-01-11更新
|
217次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高三上学期高考适应性月考卷(六)理科综合试卷
名校
3 . W、X、Y、Z为短周期主族元素,原子序数依次增大,由它们形成的一种物质的结构简式如图所示。下列说法正确的是
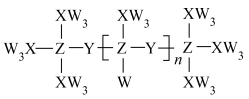
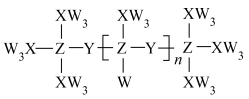
| A.四种元素中W的电负性最大,且为4.0 |
| B.由VSEPR模型可推断Z-Y-Z的键角为180° |
| C.Y的最高正化合价与其主族序数相等 |
D.基态X、Z原子的价层电子排布分别为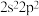 、 、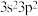 |
您最近一年使用:0次
名校
解题方法
4 . 铜盐中毒可用青霉胺解毒,解毒原理如下: 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
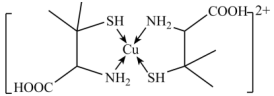
 能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
能与青霉胺形成环状络合物,其结构如图所示。该环状络合物无毒、易溶于水,可经尿液排出。下列说法错误的是
A.比较硫化氢与氨气键角的大小: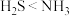 |
| B.第二周期主族元素中,第一电离能大于N的元素有1种 |
| C.该环状络合物易溶于水的主要原因是其与水可形成分子间氢键 |
| D.该环状络合物中,VSEPR模型为四面体或正四面体的非金属原子共有13个 |
您最近一年使用:0次
5 . 以下对核外电子运动状况的描述正确的是
A.同一原子中, 能级的轨道依次增多 能级的轨道依次增多 |
| B.电子云图中的一个小黑点表示一个自由运动的电子 |
C. 电子能量较高,总是在比 电子能量较高,总是在比 电子离核更远的地方运动 电子离核更远的地方运动 |
| D.在同一能级上运动的电子,其运动状态不可能相同 |
您最近一年使用:0次
2024-01-09更新
|
243次组卷
|
2卷引用:云南省昭通市第一中学2023-2024学年高二下学期开学考试化学试题
名校
6 . 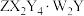 是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,
是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,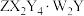 热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是
热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是

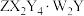 是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,
是一种白色晶体,不溶于水,用于陶瓷上釉等。W、X、Y、Z为前20号元素,原子序数依次增加且加和为35,已知X原子最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,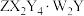 热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是
热分解可制备ZY,该化合物的热重曲线如图所示,下列叙述错误的是
| A.第一电离能:Y>X>Z |
B.键角: |
C.Z、X可以组成含有共价键的离子化合物 |
D.600℃热分解后生成固体化合物 |
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W是短周期主族元素,工业上通过液化空气再分离获得X元素的单质 ;Y元素基态原子最外电子层的s、p能级上电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
;Y元素基态原子最外电子层的s、p能级上电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
 ;Y元素基态原子最外电子层的s、p能级上电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是
;Y元素基态原子最外电子层的s、p能级上电子数相等;Z元素的+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列有关这些元素性质的说法一定正确的是| A.X元素的最简单氢化物分子的空间结构为三角锥形 |
| B.Y元素最高价氧化物的晶体类型为共价晶体 |
| C.Z元素的单质在一定条件下能与X元素的单质反应 |
| D.Z元素的第一电离能一定比W大 |
您最近一年使用:0次
2024-01-02更新
|
116次组卷
|
2卷引用:云南省三校2023-2024学年高三上学期高考备考实用性联考(四)理科综合试题
8 . 下列电子层中,含有3个能级的是
| A.K电子层 | B.L电子层 | C.M电子层 | D.N电子层 |
您最近一年使用:0次
解题方法
9 . 已知某基态原子的电子排布式为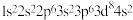 ,该元素在周期表中的位置和区分别是
,该元素在周期表中的位置和区分别是
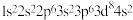 ,该元素在周期表中的位置和区分别是
,该元素在周期表中的位置和区分别是| A.第四周期ⅡB族;s区 | B.第四周期ⅦB族;d区 |
| C.第四周期Ⅶ族;d区 | D.第四周期Ⅷ族;d区 |
您最近一年使用:0次
解题方法
10 . 原子结构与元素周期表存在着内在联系,根据已学知识,请你回答下列问题:
(1)指出31号元素镓Ga)在元素周期表中的位置:_______ 。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为_______ 。
(3)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为 ,该元素的符号是
,该元素的符号是_______ 。
(5)P和S是同一周期的两种元素,P的第一电离能比S大,原因是_______ 。
(1)指出31号元素镓Ga)在元素周期表中的位置:
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为
 ,该元素的符号是
,该元素的符号是(5)P和S是同一周期的两种元素,P的第一电离能比S大,原因是
您最近一年使用:0次



