名校
1 . 2023年的诺贝尔化学奖授予了“发现和合成量子点”的三位科学家。下图是一种量子点的结构,下列说法不正确的是

A.基态原子第一电离能: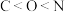 |
B.基态Se原子的价层电子排布式为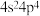 |
| C.该结构中C和N原子轨道的杂化类型相同 |
D.该结构中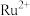 提供空轨道,N原子提供孤电子对 提供空轨道,N原子提供孤电子对 |
您最近一年使用:0次
2024-02-25更新
|
188次组卷
|
2卷引用:云南省保山市2023-2024学年高三上学期期末质量监测理综化学试题
名校
2 . 锌焙砂是锌精矿经焙烧后所得的产物,是褐色微颗粒状固体,其主要成分为 ,还含有
,还含有 、
、 和少量
和少量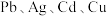 ,以锌焙砂为原料制备
,以锌焙砂为原料制备 和黄铁矾的工艺流程如下:
和黄铁矾的工艺流程如下:
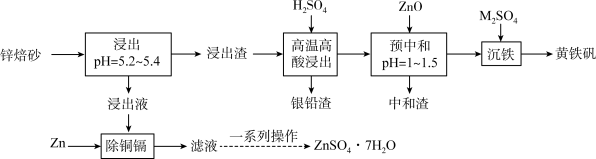
已知:① 可以看成
可以看成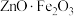 ,在高温高酸环境下才会溶解;
,在高温高酸环境下才会溶解;
② 下,
下, 和
和 开始沉淀和沉淀完全(
开始沉淀和沉淀完全(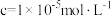 )时的
)时的 如下表:
如下表:
回答下列问题:
(1)基态 原子的简化电子排布式为
原子的简化电子排布式为_______ ,基态 原子价层电子轨道表示式为
原子价层电子轨道表示式为_______ ,基态 原子未成对电子数目为
原子未成对电子数目为_______ ,铜元素的焰色为绿色,该光谱属于_______ (填“发射”或“吸收”)光谱。
(2)欲提高 在5.2~5.4时的“浸出”速率,可采用的方法是
在5.2~5.4时的“浸出”速率,可采用的方法是_______ (写两种)。
(3)在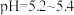 “浸出”时,锌焙砂中的铜转化为
“浸出”时,锌焙砂中的铜转化为 反应的离子方程式为
反应的离子方程式为_______ 。
(4) 时,浸出液中
时,浸出液中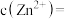
_______  。
。
(5)当有 、
、 或
或 存在时,调节含
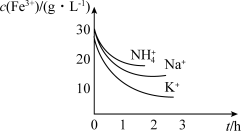
存在时,调节含 溶液的
溶液的 ,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中,
,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中,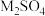 最好选用
最好选用_______ (填化学式)。
(6)获得 的一系列操作是
的一系列操作是_______ 、_______ 过滤、洗涤、干燥。
 ,还含有
,还含有 、
、 和少量
和少量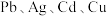 ,以锌焙砂为原料制备
,以锌焙砂为原料制备 和黄铁矾的工艺流程如下:
和黄铁矾的工艺流程如下:
已知:①
 可以看成
可以看成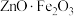 ,在高温高酸环境下才会溶解;
,在高温高酸环境下才会溶解;②
 下,
下, 和
和 开始沉淀和沉淀完全(
开始沉淀和沉淀完全(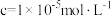 )时的
)时的 如下表:
如下表:| 金属离子 |  | |
| 开始沉淀 | 沉淀完全 | |
 | 6.2 | 8.2 |
 | 1.5 | 3.2 |
(1)基态
 原子的简化电子排布式为
原子的简化电子排布式为 原子价层电子轨道表示式为
原子价层电子轨道表示式为 原子未成对电子数目为
原子未成对电子数目为(2)欲提高
 在5.2~5.4时的“浸出”速率,可采用的方法是
在5.2~5.4时的“浸出”速率,可采用的方法是(3)在
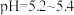 “浸出”时,锌焙砂中的铜转化为
“浸出”时,锌焙砂中的铜转化为 反应的离子方程式为
反应的离子方程式为(4)
 时,浸出液中
时,浸出液中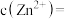
 。
。(5)当有
 、
、 或
或 存在时,调节含
存在时,调节含 溶液的
溶液的 ,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中,
,即可生成黄铁矾。不同种类的阳离子“沉铁”效果如图,则工艺流程中, 最好选用
最好选用
(6)获得
 的一系列操作是
的一系列操作是
您最近一年使用:0次
2024-02-14更新
|
195次组卷
|
2卷引用:云南省昆明市云南师范大学实验中学2023-2024学年高二下学期3月月考化学试题
3 . 下列化学用语或图示表达不正确的是
A.基态 原子的价层电子排布图: 原子的价层电子排布图: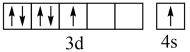 |
B.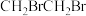 的名称:1,2-二溴乙烷 的名称:1,2-二溴乙烷 |
C. 的电子式: 的电子式: |
D.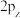 的电子云轮廓图: 的电子云轮廓图: |
您最近一年使用:0次
解题方法
4 . 皓矾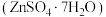 主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为
主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为 ,还含有少量
,还含有少量 以及
以及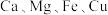 等的化合物)制备,制备流程图如图所示:
等的化合物)制备,制备流程图如图所示:

已知:常温下,金属离子开始沉淀和完全沉淀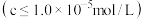 时的
时的 如下表所示:
如下表所示:
回答下列问题:
(1)写出基态铜原子的价层电子排布式_______ 。
(2)滤渣①的主要成分为_______ ;“浸取”工序中,能加快浸取效率的措施有_______ (任写一种作答)。
(3)“氧化”时该步骤离子方程式为_______ 。
(4)若“调 过滤”工序中,调节溶液
过滤”工序中,调节溶液 ,所得“滤渣②的主要成分为
,所得“滤渣②的主要成分为_______ ,氢氧化铁的溶度积常数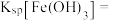
_______ 。
(5)“转化过滤”中加入锌粉的目的是_______ 。
(6)从滤液④获得皓矾晶体的具体操作为_______ 、_______ 、过滤、洗涤、干燥。
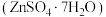 主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为
主要用作制取颜料和其他含锌材料,在防腐、电镀、医学、畜牧业和农业上也有诸多应用。皓矾可由菱锌矿(主要成分为 ,还含有少量
,还含有少量 以及
以及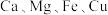 等的化合物)制备,制备流程图如图所示:
等的化合物)制备,制备流程图如图所示:
已知:常温下,金属离子开始沉淀和完全沉淀
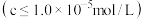 时的
时的 如下表所示:
如下表所示:| 金属离子 |  |  |  |  |  |
开始沉淀时 | 1.9 | 6.4 | 4.7 | 7.0 | 9.1 |
沉淀完全时 | 3.4 | 8.4 | 6.7 | 9.0 | 11.1 |
(1)写出基态铜原子的价层电子排布式
(2)滤渣①的主要成分为
(3)“氧化”时该步骤离子方程式为
(4)若“调
 过滤”工序中,调节溶液
过滤”工序中,调节溶液 ,所得“滤渣②的主要成分为
,所得“滤渣②的主要成分为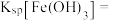
(5)“转化过滤”中加入锌粉的目的是
(6)从滤液④获得皓矾晶体的具体操作为
您最近一年使用:0次
5 .  为原子序数依次增大的短周期主族元素,
为原子序数依次增大的短周期主族元素, 的简单氢化物能与它的最高价氧化物的水化物反应生成盐,
的简单氢化物能与它的最高价氧化物的水化物反应生成盐, 原子核外
原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,
能级上的电子总数相等, 原子核外没有未成对电子,
原子核外没有未成对电子, 与
与 位于同一主族。下列说法正确的是
位于同一主族。下列说法正确的是
 为原子序数依次增大的短周期主族元素,
为原子序数依次增大的短周期主族元素, 的简单氢化物能与它的最高价氧化物的水化物反应生成盐,
的简单氢化物能与它的最高价氧化物的水化物反应生成盐, 原子核外
原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,
能级上的电子总数相等, 原子核外没有未成对电子,
原子核外没有未成对电子, 与
与 位于同一主族。下列说法正确的是
位于同一主族。下列说法正确的是A.简单离子半径: | B. 的第一电离能比 的第一电离能比 第一电离能小 第一电离能小 |
C.用电解 的氧化物制备 的氧化物制备 单质 单质 | D. 的简单氢化物比 的简单氢化物比 的简单氢化物稳定 的简单氢化物稳定 |
您最近一年使用:0次
解题方法
6 . a、b、c、d、e、f是原子序数依次增大的非0族元素,位于元素周期表的前四周期。a的一种核素无中子,b的s能级电子数与p能级的电子数之比为4:3,c与e同主族,未成对电子数为2,d在同周期元素中的原子半径最大,f在同周期元素中的未成对电子数最多。请回答下列问题:
(1)上述元素中,位于元素周期表p区的元素有________ (填元素符号),其中基态c原子中电子占据的最高能级的原子轨道形状是________ 。
(2)基态e原子的核外电子排布式为_______ ,其核外有____ 种不同空间运动状态的电子。
(3)b、c、d、e简单离子半径由大到小的顺序为_____ (用离子符号表示)。
(4)基态f原子的未成对电子数与成对电子数之比为______ 。
(1)上述元素中,位于元素周期表p区的元素有
(2)基态e原子的核外电子排布式为
(3)b、c、d、e简单离子半径由大到小的顺序为
(4)基态f原子的未成对电子数与成对电子数之比为
您最近一年使用:0次
名校
7 . 氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如下图(~代表糖苷键)。下列说法错误的是


| A.所涉及的四种元素电负性大小关系:H<C<O<N |
B.鸟嘌呤分子中2号N原子的杂化类型为 |
| C.基态氧原子核外的电子有5种不同的空间运动状态 |
| D.氢键的强度较小,在DNA解旋和复制时容易断裂和形成 |
您最近一年使用:0次
8 . 碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1) 的基态原子的电子排布式为
的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是___________ ;氧化后的原料还需粉碎、过筛,目的是___________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式___________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成___________ (填化学式)。
(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为___________ 。若Te的原子半径为rpm,碲化锌晶胞中面心与顶点的碲原子相切,晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________  (列出计算式)。
(列出计算式)。
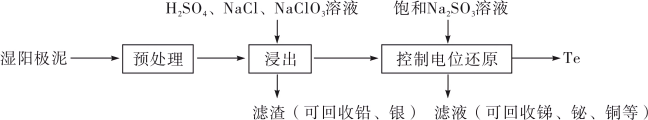
| 物质 | 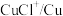 | 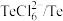 | 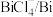 | 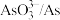 | 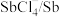 |
| 氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)
 的基态原子的电子排布式为
的基态原子的电子排布式为(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为
 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数
 (列出计算式)。
(列出计算式)。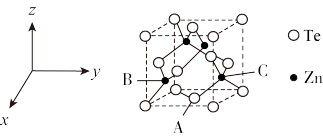
您最近一年使用:0次
名校
解题方法
9 . 长周期元素M的一种配合物对某些有机反应具有优良的催化性能,其结构可用下图表示,其中W、X、Y、Z为原子序数依次增加的短周期元素,M和Z的简单离子的电子层结构相同,下列叙述错误的是
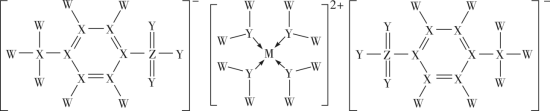
| A.简单离子半径:Z>M |
| B.电负性:Y>X>W>M |
| C.W、X、Y、Z均为元素周期表中p区元素 |
D.该配合物中X原子的轨道杂化类型为 、 、 |
您最近一年使用:0次
10 . 实验室以含钴废料(主要成分是CoO、Co2O3,含少量Fe2O3、Al2O3等杂质)为原料制备CoCO3的流程如图所示。
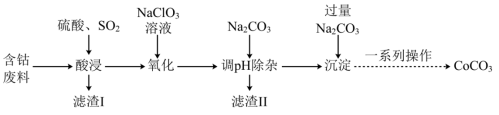
已知:①“酸浸”后过滤得到的滤液中含有Co2+、Fe2+、Al3+等。
②有关沉淀数据如表(完全沉淀时金属离子浓度≤1×10-5mol/L):
回答下列问题:
(1)基态钴原子的价层电子排布式为_______ ,在“酸浸”之前,先要对含钴废料进行粉碎处理,其目的是_______ 。
(2)“酸浸”时需通入SO2,其中SO2作______ (填“氧化剂”或“还原剂”),由于“酸浸”时,溶液中会产生Fe3+,写出SO2与Fe3+反应的离子方程式:______ 。
(3)“氧化”流程中,氧化剂与还原剂的物质的量之比为______ 。
(4)常温下,若浸取液中c(Co2+)=0.1mol/L,则“调pH除杂”时需调节溶液pH的范围为______ 至______ 。(加入NaClO3和Na2CO3时,溶液的体积变化忽略)
(5)“滤渣II”的主要成分为______ 。
(6)“一系列操作”为过滤、洗涤、干燥,其中过滤所需要的硅酸盐材质的仪器有_______ 。
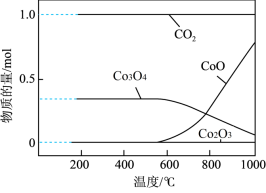
(7)将得到的CoCO3固体在空气中加热,反应温度对反应产物的影响如图所示,则500~1000℃时,发生主要反应的化学方程式为_______ 。

已知:①“酸浸”后过滤得到的滤液中含有Co2+、Fe2+、Al3+等。
②有关沉淀数据如表(完全沉淀时金属离子浓度≤1×10-5mol/L):
| 沉淀 | Al(OH)3 | Fe(OH)3 | Co(OH)2 |
| 恰好完全沉淀时的pH | 5.2 | 2.8 | 9.4 |
(1)基态钴原子的价层电子排布式为
(2)“酸浸”时需通入SO2,其中SO2作
(3)“氧化”流程中,氧化剂与还原剂的物质的量之比为
(4)常温下,若浸取液中c(Co2+)=0.1mol/L,则“调pH除杂”时需调节溶液pH的范围为
(5)“滤渣II”的主要成分为
(6)“一系列操作”为过滤、洗涤、干燥,其中过滤所需要的硅酸盐材质的仪器有
(7)将得到的CoCO3固体在空气中加热,反应温度对反应产物的影响如图所示,则500~1000℃时,发生主要反应的化学方程式为

您最近一年使用:0次



