解题方法
1 . 原子结构与元素周期表存在着内在联系,根据已学知识,请你回答下列问题:
(1)指出31号元素镓Ga)在元素周期表中的位置:_______ 。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为_______ 。
(3)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为 ,该元素的符号是
,该元素的符号是_______ 。
(5)P和S是同一周期的两种元素,P的第一电离能比S大,原因是_______ 。
(1)指出31号元素镓Ga)在元素周期表中的位置:
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为
 ,该元素的符号是
,该元素的符号是(5)P和S是同一周期的两种元素,P的第一电离能比S大,原因是
您最近一年使用:0次
名校
解题方法
2 . 我国科学家构建了新型催化剂“纳米片” ,该“纳米片”可用于氧化
,该“纳米片”可用于氧化 和吸附
和吸附 。回答下列问题:
。回答下列问题:
(1)基态Co原子的价层电子排布式为_______ ,N、C、Co中第一电离能最大的是_______ (填元素符号)。
(2)在空气中 会被氧化成
会被氧化成 ,
, 中S原子采用
中S原子采用_______ 杂化。已知氧族元素氢化物的熔沸点高低顺序为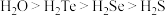 ,其原因是
,其原因是_______ 。
(3)氰 称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则
称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则 分子中σ键、π键个数之比为
分子中σ键、π键个数之比为_______ 。
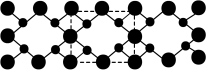
(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示,它的化学式为_______ 。
 ,该“纳米片”可用于氧化
,该“纳米片”可用于氧化 和吸附
和吸附 。回答下列问题:
。回答下列问题:(1)基态Co原子的价层电子排布式为
(2)在空气中
 会被氧化成
会被氧化成 ,
, 中S原子采用
中S原子采用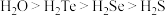 ,其原因是
,其原因是(3)氰
 称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则
称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则 分子中σ键、π键个数之比为
分子中σ键、π键个数之比为(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示,它的化学式为

您最近一年使用:0次
2024-01-01更新
|
188次组卷
|
3卷引用:云南省昭通市等4地2023-2024学年高二上学期12月月考化学试题
3 . 铜和三氧化二铁在工农业生产中用途广泛。用黄铜矿(主要成分为 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
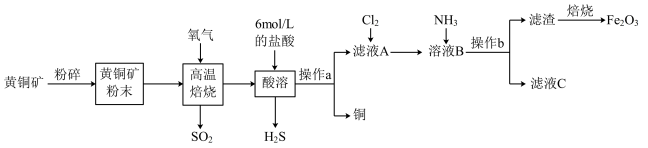
回答下列问题:
(1)铜的价电子排布式____________ 。
(2)高温焙烧时发生的反应是 ,1mol
,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子____________ mol。
(3)向滤液A中通入 的目的是
的目的是________________________________________________ 。
(4)向溶液B中通入 后发生反应的离子方程式为
后发生反应的离子方程式为_____________________________________________ 。
(5)工业上用生物法处理 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)
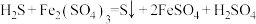
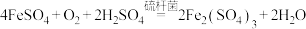
由图甲和图乙判断使用硫杆菌的最佳条件为___________________ 。若反应温度过高,反应速率下降,其原因是_______________________________________________ 。
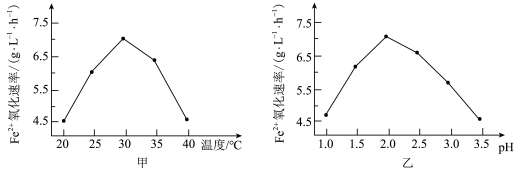
 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
回答下列问题:
(1)铜的价电子排布式
(2)高温焙烧时发生的反应是
 ,1mol
,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子(3)向滤液A中通入
 的目的是
的目的是(4)向溶液B中通入
 后发生反应的离子方程式为
后发生反应的离子方程式为(5)工业上用生物法处理
 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)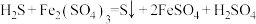
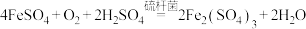
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
4 . 下列关于原子核外电子排布与元素在周期表中位置关系的表述正确的是
A.原子的价电子排布式为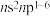 的元素一定是主族元素 的元素一定是主族元素 |
B.氯化钠晶体中,每个 周围与它距离相等且最近的 周围与它距离相等且最近的 有6个 有6个 |
| C.因同周期主族元素的原子半径从左到右逐渐减小,故其第一电离能逐渐增大 |
D. 是一种非常稳定的化合物,是由于水分子间形成氢键所致 是一种非常稳定的化合物,是由于水分子间形成氢键所致 |
您最近一年使用:0次
解题方法
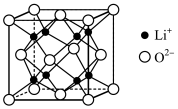
5 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1) 的价电子排布图为:
的价电子排布图为:_________________________ ,基态磷原子的所有电子中有________ 种空间运动状态。
(2)Li、O、P三种元素的电负性由大到小的顺序是:________________________ 。
(3)无水硫酸铜为白色粉末溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有___________ 。
A.配位键 B.金属键 C.离子键 D.共价键
E.氢键 F.范德华力
(4)N和P是同主族元素,但是 分子中的键角大子
分子中的键角大子 分子中的键角,原因是:
分子中的键角,原因是:___________________________________________ 。 为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为
为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为____________  (列出计算式即可),
(列出计算式即可), 和
和 的最短距离等于
的最短距离等于____________ nm(用含b的代数式表示)。
(1)
 的价电子排布图为:
的价电子排布图为:(2)Li、O、P三种元素的电负性由大到小的顺序是:
(3)无水硫酸铜为白色粉末溶于水形成蓝色溶液,则硫酸铜稀溶液中不存在的微粒间作用力有
A.配位键 B.金属键 C.离子键 D.共价键
E.氢键 F.范德华力
(4)N和P是同主族元素,但是
 分子中的键角大子
分子中的键角大子 分子中的键角,原因是:
分子中的键角,原因是: 为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为
为离子晶体,具有反萤石结构,晶胞如图所示。若晶胞参数为b nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为 (列出计算式即可),
(列出计算式即可), 和
和 的最短距离等于
的最短距离等于
您最近一年使用:0次
6 . X、Y、Z、W为原子序数依次增大的前四周期主族元素,四种元素中仅X、Y在同一周期,它们形成的一种物质的结构如图所示,其中所有原子均形成了8电子稳定结构。下列推断中正确的是
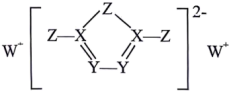
| A.X的氢化物常温下一定是气体 | B.1mol上述物质中,含有的 数目为7 数目为7 |
| C.Y的含氧酸的酸性一定比Z的含氧酸弱 | D.元素的第一电离能:X<Y<W |
您最近一年使用:0次
2023-12-21更新
|
312次组卷
|
2卷引用:云南省昭通市云天化中学教研联盟2023-2024学年高二上学期期中考试化学试题
7 . 氮掺杂碳层包覆纳米金催化剂(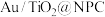 )催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
)催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
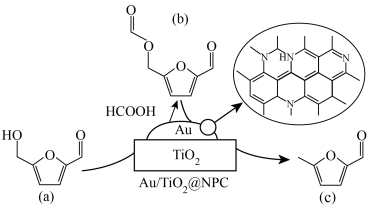
下列说法正确的是
 )催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
)催化5-羟甲基糠醛非邻氢转化制5-甲基糠醛的反应过程如图所示。
下列说法正确的是
A.第一电离能: |
B.图示反应过程中有 键的断裂和形成 键的断裂和形成 |
C.基态 原子的价层电子排布式为 原子的价层电子排布式为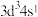 |
D.若 换成 换成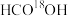 ,则(b)为 ,则(b)为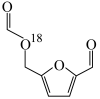 |
您最近一年使用:0次
8 . NCM是三元锂电池最重要的前驱体材料,一种以镍钴杂料(主要成分为 、
、 、
、 ,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
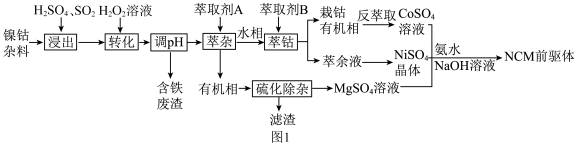
回答下列问题:
(1)基态钴原子核外未成对电子数与基态锰原子核外未成对电子数之比为___________ 。
(2)为提高“浸出”效率,可采取的措施有___________ (写出一条即可);“浸出”过程中 的作用是
的作用是___________ (用离子方程式表示)。
(3)常温下,若“转化”后的溶液中 浓度为
浓度为 ,在“调
,在“调 ”过程中,当
”过程中,当 调节到2.2时,开始出现
调节到2.2时,开始出现 沉淀,若要使
沉淀,若要使 完全沉淀,则调节溶液
完全沉淀,则调节溶液 最小为
最小为___________ [已知:当c(Fe3+)≤1×10-5mol/L时,认为 沉淀完全]
沉淀完全]
(4)有机萃取剂P204和P507对金属离子的萃取率与pH的关系如图2、图3所示。
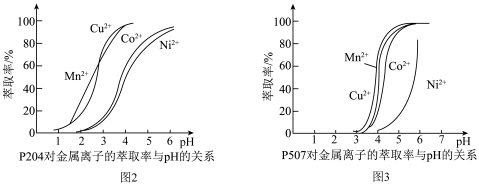
①萃取剂A是___________ (填“P204”或“P507”,下同),萃取剂B是___________ 。
②进行“萃钴”操作前,需对水相调pH至___________ (填标号),以达到最佳萃取 的效果。
的效果。
a.2.5 b.3.5 c.4.5 d.5.5
③萃取剂萃取 的原理为2HR(有机相)
的原理为2HR(有机相)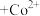 (水相)
(水相)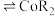 (有机相)
(有机相) (水相),则反萃取操作中可向载钴有机相中加入
(水相),则反萃取操作中可向载钴有机相中加入___________ (填试剂名称)得到含 的溶液;一定条件下,萃取平衡时,溶液中
的溶液;一定条件下,萃取平衡时,溶液中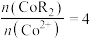 ,则
,则 的萃取率为
的萃取率为___________ 。
(5)一种NiAs晶体结构如图4所示。
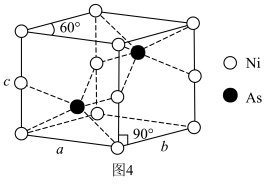
通过X射线光谱测算出该晶胞参数为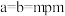 ,
,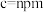 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶体密度为
,则该晶体密度为___________ (填含m、n和 的表达式)
的表达式) 。
。
 、
、 、
、 ,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
,还含有少量铁和铜的氧化物)为原料制备NCM前驱体的工艺流程如图1所示。
回答下列问题:
(1)基态钴原子核外未成对电子数与基态锰原子核外未成对电子数之比为
(2)为提高“浸出”效率,可采取的措施有
 的作用是
的作用是(3)常温下,若“转化”后的溶液中
 浓度为
浓度为 ,在“调
,在“调 ”过程中,当
”过程中,当 调节到2.2时,开始出现
调节到2.2时,开始出现 沉淀,若要使
沉淀,若要使 完全沉淀,则调节溶液
完全沉淀,则调节溶液 最小为
最小为 沉淀完全]
沉淀完全](4)有机萃取剂P204和P507对金属离子的萃取率与pH的关系如图2、图3所示。

①萃取剂A是
②进行“萃钴”操作前,需对水相调pH至
 的效果。
的效果。a.2.5 b.3.5 c.4.5 d.5.5
③萃取剂萃取
 的原理为2HR(有机相)
的原理为2HR(有机相)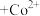 (水相)
(水相)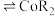 (有机相)
(有机相) (水相),则反萃取操作中可向载钴有机相中加入
(水相),则反萃取操作中可向载钴有机相中加入 的溶液;一定条件下,萃取平衡时,溶液中
的溶液;一定条件下,萃取平衡时,溶液中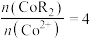 ,则
,则 的萃取率为
的萃取率为(5)一种NiAs晶体结构如图4所示。

通过X射线光谱测算出该晶胞参数为
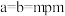 ,
,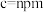 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶体密度为
,则该晶体密度为 的表达式)
的表达式) 。
。
您最近一年使用:0次
名校
解题方法
9 . 2023年诺贝尔化学奖授予对量子点的发现有突出贡献的科研工作者。量子点是指尺寸在纳米量级(通常2~20nm)的半导体晶体,其中铜铟硫(CuInS2)量子点被广泛用于光电探测、发光二极管以及光电化学电池领域。下列说法不正确 的是
| A.制备过程中得到的CuInS2量子点溶液能够产生丁达尔效应 |
| B.可利用X射线衍射技术解析量子点的晶体结构 |
| C.已知In的原子序数为49,可推知In位于元素周期表第四周期 |
| D.基态Cu+的价层电子排布式为3d10 |
您最近一年使用:0次
2023-11-06更新
|
605次组卷
|
7卷引用:云南省大理白族自治州民族中学2023-2024学年高三上学期1月月考理综试卷
云南省大理白族自治州民族中学2023-2024学年高三上学期1月月考理综试卷北京市丰台区2023-2024学年高三上学期期中练习化学试题(已下线)选择题1-5北京市第一七一中学2023-2024学年高三上学期12月月考化学试题 (已下线)题型05 物质的性质与应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)宁夏石嘴山市平罗中学2023-2024学年高三上学期第三次月考化学试题北京汇文中学2023-2024学年高三上学期12月上旬化学测试
10 . 三价铬离子能形成多种配位化合物,[Cr(NH3)3(H2O)2Cl]2+(其结构如下图)是其中一种配位化合物的阳离子。下列说法正确的是
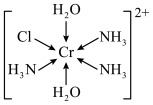

| A.该配合物的中心离子是Cr3+,配位数为5 |
| B.基态原子未成对电子数:Cr>N>O>Cl |
| C.基态原子的第一电离能:Cl>O>N>H |
| D.该配合物阳离子中存在极性键和非极性键 |
您最近一年使用:0次



