名校
解题方法
1 . 氮化钛是一种导电材料,也是一种催化剂。氮化钛晶胞如图所示,A的原子坐标为 ,C的原子坐标为
,C的原子坐标为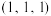 。已知:它的晶胞参数为
。已知:它的晶胞参数为 ,氮原子半径为
,氮原子半径为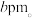 下列叙述错误的是
下列叙述错误的是
 ,C的原子坐标为
,C的原子坐标为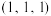 。已知:它的晶胞参数为
。已知:它的晶胞参数为 ,氮原子半径为
,氮原子半径为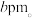 下列叙述错误的是
下列叙述错误的是
| A.基态钛原子有2个未成对电子 | B.B的原子坐标为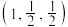 |
C.钛原子半径为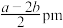 | D.氮原子的配位数为12 |
您最近一年使用:0次
名校
2 . 卤素单质及其化合物在工农业生产中有着广泛的应用。回答下列问题:
(1)类卤素 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):
①硫氰酸和异硫氰酸分子中 键和
键和 键个数之比
键个数之比___________ (填“相等”或“不相等”)。
②异硫氰酸中N的杂化轨道类型是___________ 。
③硫氰酸的电子式为___________ 。
(2) 的VSEPR模型是
的VSEPR模型是___________ , 的中心原子的价层电子对数是
的中心原子的价层电子对数是___________ 。
(3)键角:
___________ (填“>”“<”或“=”) ,判断的理由为
,判断的理由为___________ 。
(4)酸性:三氟乙酸( )
)___________ (填“>”或“<”) ,判断的理由为
,判断的理由为___________ 。
(5) 与水反应的化学方程式为
与水反应的化学方程式为___________ (该反应为非氧化还原反应)。
(1)类卤素
 对应的酸有两种,硫氰酸(
对应的酸有两种,硫氰酸( )和异硫氰酸(
)和异硫氰酸( ):
):①硫氰酸和异硫氰酸分子中
 键和
键和 键个数之比
键个数之比②异硫氰酸中N的杂化轨道类型是
③硫氰酸的电子式为
(2)
 的VSEPR模型是
的VSEPR模型是 的中心原子的价层电子对数是
的中心原子的价层电子对数是(3)键角:

 ,判断的理由为
,判断的理由为(4)酸性:三氟乙酸(
 )
) ,判断的理由为
,判断的理由为(5)
 与水反应的化学方程式为
与水反应的化学方程式为
您最近一年使用:0次
2024-04-26更新
|
209次组卷
|
2卷引用:广西壮族自治区桂林市联考2023-2024学年高二下学期3月月考化学试题
3 . Mn是元素周期表中第25号元素,它的氧化物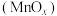 可用于催化醇的氧化氰化,反应如下:
可用于催化醇的氧化氰化,反应如下:
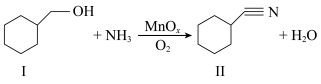
回答下列问题:
(1)组成物质Ⅰ的元素中,电负性最大是_____ (填元素符号)。
(2)物质Ⅱ中C原子的杂化轨道类型有_____ ; 该分子中含有
该分子中含有 键
键_____ mol。
(3) 的VSEPR模型为
的VSEPR模型为_____ ;已知 ,但该反应不及Na与
,但该反应不及Na与 的反应剧烈,从共价键的角度分析,可能的原因是
的反应剧烈,从共价键的角度分析,可能的原因是_____ 。
(4)Mn元素在周期表中的位置是_____ ;基态Mn原子的核外电子有_____ 种空间运动状态。
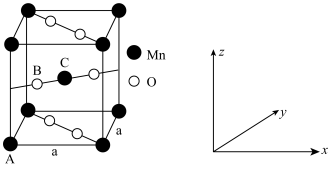
(5)某种 晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
晶体的晶胞如下图所示,该晶体中Mn元素的化合价为_____ 。已知该晶胞底面是边长为 的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为
的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为 、
、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为_____ cm(用含a、m、n的代数式表示)。
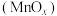 可用于催化醇的氧化氰化,反应如下:
可用于催化醇的氧化氰化,反应如下:
回答下列问题:
(1)组成物质Ⅰ的元素中,电负性最大是
(2)物质Ⅱ中C原子的杂化轨道类型有
 该分子中含有
该分子中含有 键
键(3)
 的VSEPR模型为
的VSEPR模型为 ,但该反应不及Na与
,但该反应不及Na与 的反应剧烈,从共价键的角度分析,可能的原因是
的反应剧烈,从共价键的角度分析,可能的原因是(4)Mn元素在周期表中的位置是
(5)某种
 晶体的晶胞如下图所示,该晶体中Mn元素的化合价为
晶体的晶胞如下图所示,该晶体中Mn元素的化合价为 的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为
的正方形,以晶胞参数为单位长度建立坐标系,A、B、C处的原子坐标参数分别为 、
、 、
、 ,则Mn与O形成化学键的键长为
,则Mn与O形成化学键的键长为
您最近一年使用:0次
名校
解题方法
4 . 下列关于各晶体模型示意图的分析正确的是
| 名称 |  的晶胞 的晶胞 |  的晶胞 的晶胞 | 晶体碘的晶胞 | 石墨晶体的结构 |
| 模型 示意图 | 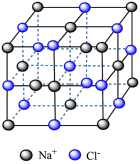 |  |  | 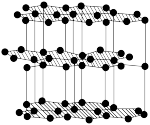 |
| 分析 | 1个 晶胞内含有6个 晶胞内含有6个 和6个 和6个 | B.Si原子的配位数为2 | C. 在晶胞中的排列有2种取向 在晶胞中的排列有2种取向 | D.石墨层与层间的主要作用力是共价键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-15更新
|
415次组卷
|
3卷引用:广西桂林市2022-2023学年高二下学期期末考试化学试题
名校
5 . 2020年8月19日发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》中指出,氯喹类药物可用于治疗新冠肺炎,其中羟基氯喹结构如图所示。
(1)羟基氯喹分子中含氧官能团的名称为_____ 。
(2)羟基氯喹分子中基态Cl原子核外电子有_____ 种空间运动状态。
(3)羟基氯喹分子中C、N、O三种元素的电负性由小到大的顺序为_____ (用元素符号表示),第一电离能由小到大的顺序为_____ (用元素符号表示)。
(4)N原子的VSEPR模型为_____ 。
(5)请在答题卡中,用*标出羟基氯喹分子中的手性碳原子_____ 。
(6)下列现代分析手段中,可用于检测羟基氯的晶体结构是_____ 。

(1)羟基氯喹分子中含氧官能团的名称为
(2)羟基氯喹分子中基态Cl原子核外电子有
(3)羟基氯喹分子中C、N、O三种元素的电负性由小到大的顺序为
(4)N原子的VSEPR模型为
(5)请在答题卡中,用*标出羟基氯喹分子中的手性碳原子
(6)下列现代分析手段中,可用于检测羟基氯的晶体结构是
| A.X射线衍射 | B.原子光谱 | C.元素分析 | D.红外光谱 |
您最近一年使用:0次
2023-04-24更新
|
667次组卷
|
3卷引用:广西大学附属中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
6 . 乙二胺四乙酸铁钠可用于感光材料冲洗药品及漂白剂,化学式为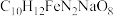 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下:
(1)基态氯原子的价层电子排布图为___________ 。
(2)下列氮原子能量最高的是___________(填标号)。
(3)EDTA的组成元素中C、N、O的第一电离能由大到小顺序为___________ (填元素符号)。碳原子的杂化轨道类型为___________ 。
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为___________ 。
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为___________ 。___________ 区(填“s”“p”“d”或“ds”)。铁的某种晶胞沿面对角线的位置切下之后可以得到如图2所示的截面。假设铁的原子半径为a nm,则该铁晶体的密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
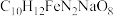 ;工业上可用EDTA与
;工业上可用EDTA与 、NaOH溶液发生反应进行制备,合成路线如下:
、NaOH溶液发生反应进行制备,合成路线如下: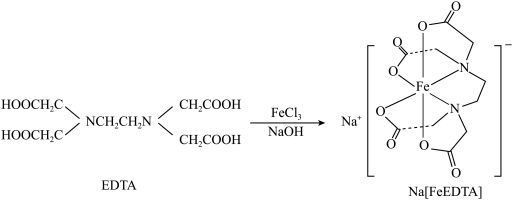
(1)基态氯原子的价层电子排布图为
(2)下列氮原子能量最高的是___________(填标号)。
A.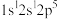 | B. | C. | D.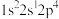 |
(4)NH3中N—H键的键角小于CH4中C—H键的键角,其原因为
(5)某种Fe、N组成的磁性化合物的结构如图1所示,N随机排列在Fe构成的正八面体的空隙中。该磁性化合物的化学式为
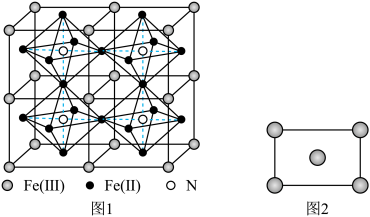
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2023-04-23更新
|
865次组卷
|
8卷引用:广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题
广西壮族自治区南宁市第二中学2023届高三下学期收网考理科综合化学试题2023届广西钦州市灵山县那隆中学高三下学期5月考前冲刺保温卷理综试卷-高中化学福建省百校联盟2023届高三第三次模拟考试化学试题福建省百校联盟2023届高三下学期第三次模拟考试化学试题(已下线)押题密卷 02-【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)专题16 物质结构与性质综合题-2023年高考化学真题题源解密(全国通用)北京市第二中学2022-2023学年高二下学期期末考试化学试题北京市首都师范大学附属中学2023-2024学年高三下学期3月月考化学试题
7 . 黑火药的爆炸反应原理为2KNO3+3C+S K2S+N2↑+3CO2↑。请回答下列问题:
K2S+N2↑+3CO2↑。请回答下列问题:
(1)基态O原子的核外电子排布式为___________ ;基态18O原子核外有___________ 种空间运动状态的电子。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用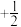 表示,与之相反的用
表示,与之相反的用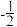 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为___________ 。
(3)K位于周期表的___________ 区;基态钾离子的电子占据的最高能层符号是___________ 。
(4)K+与S2-具有相同的电子构型,r(K+)小于r(S2-),原因是___________ 。
(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是___________ 。
a.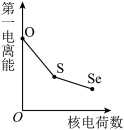 b.
b.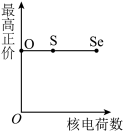 c.
c. d.
d.
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能(E1)。MgO的Born-Haber循环如图所示。

由图可知,Mg原子的第二电离能为___________ kJ/mol;O=O键的键能为___________ kJ/mol;氧原子的第一电子亲和能为___________ kJ/mol。
 K2S+N2↑+3CO2↑。请回答下列问题:
K2S+N2↑+3CO2↑。请回答下列问题:(1)基态O原子的核外电子排布式为
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
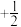 表示,与之相反的用
表示,与之相反的用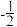 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数的代数和为(3)K位于周期表的
(4)K+与S2-具有相同的电子构型,r(K+)小于r(S2-),原因是
(5)下列曲线表示氧族元素性质随核电荷数的变化趋势,正确的是
a.
 b.
b. c.
c. d.
d.
(6)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能(E1)。MgO的Born-Haber循环如图所示。

由图可知,Mg原子的第二电离能为
您最近一年使用:0次
2023-03-10更新
|
392次组卷
|
2卷引用:广西南宁市2022-2023学年高二上学期期末教学质量调研化学试题
8 . 氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将乙炔催化还原成乙烯。
①基态Fe3+的核外电子排布式为_______ 。
②C、N、O三种元素第一电离能从大到小的顺序是_______ 。
③下列说法正确的有_______ (不定项选择)。
A.C2H2、C2H4都是非极性分子 B.碳负离子CH 呈三角锥形
呈三角锥形
C.NO+电子式为 D.NH3沸点比N2高,主要是因为前者是极性分子
D.NH3沸点比N2高,主要是因为前者是极性分子
(2)NaN3可用于汽车安全气囊。写出两种与N 互为等电子体的分子或离子
互为等电子体的分子或离子_______ 。
(3)烟酰胺是一种含氮有机物,结构简式如图所示,烟酰胺分子中氮原子的杂化轨道类型有_______ ,1 mol该分子中含σ键的数目为_______ 。

(4)CaF2的晶胞如图所示,若该晶体的密度为ρ g/cm3,阿伏加德罗常数的值为NA,则晶胞边长为_______ pm(用含ρ、NA的代数式表示)。
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将乙炔催化还原成乙烯。
①基态Fe3+的核外电子排布式为
②C、N、O三种元素第一电离能从大到小的顺序是
③下列说法正确的有
A.C2H2、C2H4都是非极性分子 B.碳负离子CH
 呈三角锥形
呈三角锥形C.NO+电子式为
 D.NH3沸点比N2高,主要是因为前者是极性分子
D.NH3沸点比N2高,主要是因为前者是极性分子(2)NaN3可用于汽车安全气囊。写出两种与N
 互为等电子体的分子或离子
互为等电子体的分子或离子(3)烟酰胺是一种含氮有机物,结构简式如图所示,烟酰胺分子中氮原子的杂化轨道类型有

(4)CaF2的晶胞如图所示,若该晶体的密度为ρ g/cm3,阿伏加德罗常数的值为NA,则晶胞边长为

您最近一年使用:0次
解题方法
9 . 钛、铜、锌及其化合物在生产生活中有着广泛的应用,回答下列问题:
(1)基态铜原子的价电子排布式_______ ;元素铜和锌的第二电离能: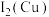
_______  (填“>”、“>”或“=”)
(填“>”、“>”或“=”)
(2)硫酸铜溶于氨水可形成 络合物。
络合物。 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为_______ ,阴离子的立体构型为_______ ;1mol 中含有
中含有 键的数目为
键的数目为_______ 。
(3)钛与卤素形成的化合物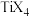 熔点如表,则
熔点如表,则 的熔点比
的熔点比 高的原因可能是
高的原因可能是_______ 。
(4)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如图所示:则组成R的元素中,除Ti之外元素的电负性从大到小的顺序是_______ (填元素符号)。

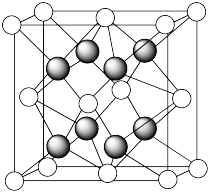
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_______ ;若该晶胞边长为a pm,NA代表阿伏加德罗常数的值,则晶胞密度为_______  。
。

(1)基态铜原子的价电子排布式
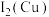
 (填“>”、“>”或“=”)
(填“>”、“>”或“=”)(2)硫酸铜溶于氨水可形成
 络合物。
络合物。 中N原子的杂化轨道类型为
中N原子的杂化轨道类型为 中含有
中含有 键的数目为
键的数目为(3)钛与卤素形成的化合物
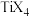 熔点如表,则
熔点如表,则 的熔点比
的熔点比 高的原因可能是
高的原因可能是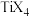 |  |  |  |  |
| 熔点℃ | 377 | ―24 | 38.3 | 153 |
(4)某含钛半夹心结构催化剂R能催化乙烯、丙烯等的聚合,其结构如图所示:则组成R的元素中,除Ti之外元素的电负性从大到小的顺序是

(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
 。
。
您最近一年使用:0次
解题方法
10 .  是制作超细铜粉的原料,回答下列问题:
是制作超细铜粉的原料,回答下列问题:
(1) 中Cu显+1价,其价电子排布图为
中Cu显+1价,其价电子排布图为_______ ,核外电子有_______ 种空间运动状态。
(2)N、O、S第一电离能由大到小的顺序是_______ (用元素符号表示)。研究发现,它们简单氢化物的沸点按 、
、 、
、 依次降低,出现这一现象的原因是
依次降低,出现这一现象的原因是_______ 。
(3) 的空间构型为
的空间构型为_______ (写名称),写出一种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(4)超细铜粉与钙可形成储氢合金 ,晶胞结构如图所示。已知储氢后氢进入晶胞空隙,晶胞体积不变,形成合金
,晶胞结构如图所示。已知储氢后氢进入晶胞空隙,晶胞体积不变,形成合金 。则
。则 中n=
中n=_______ (填数值);储氢后合金的密度增加了_______ %(填数值)。

 是制作超细铜粉的原料,回答下列问题:
是制作超细铜粉的原料,回答下列问题:(1)
 中Cu显+1价,其价电子排布图为
中Cu显+1价,其价电子排布图为(2)N、O、S第一电离能由大到小的顺序是
 、
、 、
、 依次降低,出现这一现象的原因是
依次降低,出现这一现象的原因是(3)
 的空间构型为
的空间构型为 互为等电子体的分子的化学式
互为等电子体的分子的化学式(4)超细铜粉与钙可形成储氢合金
 ,晶胞结构如图所示。已知储氢后氢进入晶胞空隙,晶胞体积不变,形成合金
,晶胞结构如图所示。已知储氢后氢进入晶胞空隙,晶胞体积不变,形成合金 。则
。则 中n=
中n=
您最近一年使用:0次



