1 . 门捷列夫认为氮、碳、氧、氢是“四大天王”元素,它们与宇宙和生命的形成都有密切联系,可以相互结合成很多化合物。
(1)四种元素中,核外未成对电子数目相同的元素有___________ (填写元素符号,下同);四种元素的原子半径由大到小的顺序为___________ 。
(2)HCN是生命演化过程中的基础物质之一。已知HCN中C、N都满足8电子稳定结构,则HCN的电子式为___________ ;其中C、N之间的共用电子对偏向的元素是___________ ,从原子结构角度解释其原因___________ 。
(3)N2O是医学上的一-种麻醉剂,可以通过反应NH3+O2→N2O+H2O制得,配平该反应的化学方程式___________ ,若生成1.8g水,转移的电子数目为___________ 个(结构保留两位有效数字)。
(1)四种元素中,核外未成对电子数目相同的元素有
(2)HCN是生命演化过程中的基础物质之一。已知HCN中C、N都满足8电子稳定结构,则HCN的电子式为
(3)N2O是医学上的一-种麻醉剂,可以通过反应NH3+O2→N2O+H2O制得,配平该反应的化学方程式
您最近一年使用:0次
名校
解题方法
2 . 自然界中许多固态物质都是晶体,它们们有规则的几何外形,如晶莹的雪花、玲珑剔透的石英、棱角分明的食盐固体和许多矿石。我们的生活因此而多美丽。
(1)区分晶体和非晶体最科学的方法是_________ (填选项序号,下同)
A.比较硬度 B.对固体进行X射线衍射 C.看是否有规则的几何外形
(2)下列各组物质的晶体中,化学键类型、晶体类型都相同的是
(3)下列物质性质的变化规律,与化学键的强弱无关的是
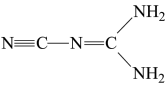
(4)某物质(结构简式如图所示)可溶于水、乙醇,熔点为209.5 ℃。下列说法不正确的是 。
(5)随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N 等已被发现。下列有关说法中,正确的是 。
等已被发现。下列有关说法中,正确的是 。
(1)区分晶体和非晶体最科学的方法是
A.比较硬度 B.对固体进行X射线衍射 C.看是否有规则的几何外形
(2)下列各组物质的晶体中,化学键类型、晶体类型都相同的是
| A.CO2和SO2 | B.NaCl和HCl | C.H2S和H2O | D.CF2Cl2和CH3COONa |
(3)下列物质性质的变化规律,与化学键的强弱无关的是
| A.金刚石的硬度、熔点、沸点都高于晶体硅 |
| B.Li、Na、K、Rb的熔点、沸点逐渐降低 |
| C.NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D.F2、Cl2、Br2、I2的熔点、沸点逐渐升高 |
(4)某物质(结构简式如图所示)可溶于水、乙醇,熔点为209.5 ℃。下列说法不正确的是 。

| A.该物质为共价晶体 |
| B.该物质分子中含有极性共价键 |
| C.该物质分子中σ键和π键的个数比为3∶1 |
| D.该物质分子中每个原子最外层均达到8电子稳定结构 |
(5)随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N
 等已被发现。下列有关说法中,正确的是 。
等已被发现。下列有关说法中,正确的是 。| A.H2 与 H3 中存在氢键 | B.O2 与 O4 互为同位素 |
| C.C60 分子中有范德华力 | D.N 中含有 24 个价电子 中含有 24 个价电子 |
您最近一年使用:0次
名校
解题方法
3 . ⅤA族元素(N、P、As、Sb、Bi等)在生活中占有重要地位。请回答:
(1)叠氮酸根离子 的空间结构名称为
的空间结构名称为___________ ;中心氮原子的杂化轨道类型是___________ ;叠氮化钠 用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和
用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和 ,
, 不稳定而分解的原因是
不稳定而分解的原因是___________ 。
(2)实验室测得分子式为 的化合物有两种不同的熔点和沸点:
的化合物有两种不同的熔点和沸点:
B的结构式为___________ 。
(3)已知P可以与Cl形成多种化合物,如: 、
、 、
、 等,下列说法
等,下列说法不正确 的是___________。
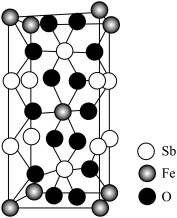
(4)Fe、Sb与O形成的某化合物晶体的晶胞如图。该化合物的化学式为___________ 。
(1)叠氮酸根离子
 的空间结构名称为
的空间结构名称为 用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和
用于汽车的安全气囊中,当汽车发生剧烈碰撞时,可分解生成Na和 ,
, 不稳定而分解的原因是
不稳定而分解的原因是(2)实验室测得分子式为
 的化合物有两种不同的熔点和沸点:
的化合物有两种不同的熔点和沸点:| 熔点/℃ | 沸点/℃ | |
| A |  | 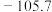 |
| B |  | 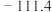 |
(3)已知P可以与Cl形成多种化合物,如:
 、
、 、
、 等,下列说法
等,下列说法A.微粒半径: |
| B.同周期中第一电离能小于P的元素有4种 |
C.根据电负性差异, 的水解产物为 的水解产物为 和 和 |
D.已知 以 以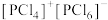 的形式存在,熔融时不导电,可推测熔融时 的形式存在,熔融时不导电,可推测熔融时 可能转化为 可能转化为 |

您最近一年使用:0次
2023-08-08更新
|
557次组卷
|
3卷引用:浙江省杭州市强基联盟2023届高三下学期2月统测化学试题
名校
解题方法
4 . 我国力争在2030年前实现“碳达峰”。2060年前实现“碳中和”的目标,因此二氧化碳的固定及转化成了重要的研究课题。
Ⅰ.在 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;
Ⅱ.新型 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。
请回答下列问题:
(1)基态Cu原子的外围电子排布式为___________ ,基态O原子核外有___________ 种不同运动状态的电子。
(2)Ⅰ中涉及的 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是___________ (填化学式)。
(3) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子中含有的 键和
键和 键数目之比为
键数目之比为___________ 。
(4) 反应中,
反应中, 的立体构型为
的立体构型为___________ , 的沸点高于
的沸点高于 的原因是
的原因是___________ 。
(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。
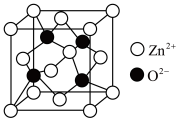
① 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为___________ 。
②设晶胞边长为anm, 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  。
。
Ⅰ.在
 催化作用下
催化作用下 和
和 反应生成甲醇:
反应生成甲醇: ;
;Ⅱ.新型
 水介质电池放电时,温室气体
水介质电池放电时,温室气体 被转化为储能物质
被转化为储能物质 。
。请回答下列问题:
(1)基态Cu原子的外围电子排布式为
(2)Ⅰ中涉及的
 、
、 、
、 、
、 ,属于非极性分子的是
,属于非极性分子的是(3)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为 键和
键和 键数目之比为
键数目之比为(4)
 反应中,
反应中, 的立体构型为
的立体构型为 的沸点高于
的沸点高于 的原因是
的原因是(5)氧化锌(ZnO),俗称锌白,是一种常用的化学添加剂,广泛地应用于塑料、硅酸盐制品、合成橡胶等产品的制作中。一种ZnO的立方晶胞如图所示。

①
 周围距离最近且等距的
周围距离最近且等距的 数目为
数目为②设晶胞边长为anm,
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 。
。
您最近一年使用:0次
2023-07-30更新
|
933次组卷
|
4卷引用:内蒙古名校联盟2022-2023学年高二下学期期末考试化学试题
解题方法
5 . 填空。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下,则该元素是___________ (填写元素符号)。
(2)请解释 的热稳定性高于
的热稳定性高于 的原因
的原因___________ 。
(3)基态氮原子核外电子的空间运动状态有___________ 种, 的键角约为107°,推测
的键角约为107°,推测 的键角
的键角___________ 107°(填“>,<或=”)。
(4)基态硅原子价层电子轨道表示式为___________ ; 与N-甲基咪唑(分子式为:
与N-甲基咪唑(分子式为: ,结构为
,结构为 )反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是
)反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是___________ ,1个N-甲基咪唑分子中含有___________ 个 键。
键。
(5)已知周期表中存在对角相似规则,如Be与Al在周期表中处于对角线位置则化学性质相似,Be的氧化物、氢氧化物也有两性,写出Be的氢氧化物与氢氧化钠反应的化学方程式___________ 。
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下,则该元素是
| 电离能 |  |  |  |  | …… |
 | 578 | 1817 | 2745 | 11575 | …… |
 的热稳定性高于
的热稳定性高于 的原因
的原因(3)基态氮原子核外电子的空间运动状态有
 的键角约为107°,推测
的键角约为107°,推测 的键角
的键角(4)基态硅原子价层电子轨道表示式为
 与N-甲基咪唑(分子式为:
与N-甲基咪唑(分子式为: ,结构为
,结构为 )反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是
)反应可以得到一种功能性螯合物。则:C、N、H三种非金属元素的电负性由大到小的顺序是 键。
键。(5)已知周期表中存在对角相似规则,如Be与Al在周期表中处于对角线位置则化学性质相似,Be的氧化物、氢氧化物也有两性,写出Be的氢氧化物与氢氧化钠反应的化学方程式
您最近一年使用:0次
2023-03-28更新
|
693次组卷
|
3卷引用:浙江省绍兴市上虞区2022-2023学年高二上学期期末教学质量调测化学试题
名校
6 . C、O、S、 、
、 、
、 等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
(1) 元素在元素周期表的位置是
元素在元素周期表的位置是_______ ,基态 原子能量最高的电子占据的原子轨道的形状是
原子能量最高的电子占据的原子轨道的形状是_______ ,基态 原子的简化电子排布式为
原子的简化电子排布式为_______ 。
(2)基态S原子的价层电子轨道表示式为_______ , 属于
属于_______ 分子(填“极性”或“非极性”)。
(3) 的键角
的键角_______  的键角(填“>”、“<”或“=”),理由是
的键角(填“>”、“<”或“=”),理由是_______
(4)琥珀酸亚铁片是预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。 比
比 的离子半径小,原因是
的离子半径小,原因是_______ 。
 、
、 、
、 等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:(1)
 元素在元素周期表的位置是
元素在元素周期表的位置是 原子能量最高的电子占据的原子轨道的形状是
原子能量最高的电子占据的原子轨道的形状是 原子的简化电子排布式为
原子的简化电子排布式为(2)基态S原子的价层电子轨道表示式为
 属于
属于(3)
 的键角
的键角 的键角(填“>”、“<”或“=”),理由是
的键角(填“>”、“<”或“=”),理由是(4)琥珀酸亚铁片是预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是 比
比 的离子半径小,原因是
的离子半径小,原因是
您最近一年使用:0次
2023-03-05更新
|
385次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期期末考试化学试题
名校
7 . 方钴矿化合物是典型的热电材料,在环境污染和能源危机日益严重的今天,进行新型热电材料的研究具有很强的现实意义。
(1)Brian Sales等研究了一类新型热电材料,叫作填隙方钴矿锑化物,在钴和锑形成的晶体空隙中填充入稀土原子La(如图所示),该化合物的化学式为_______ 。

(2)Co和Fe的逐级电离能数据如表,Fe的 大于Co的原因是
大于Co的原因是_______ 。
(3)已知 的熔点73℃,沸点223.5℃,
的熔点73℃,沸点223.5℃, 的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是
的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是_______ 。预测 的空间构型为
的空间构型为_______ 。
(4)为更好地理解超酸的强酸性,实验小组查阅相关资料了解得:混合超强酸 显强酸性的原因是氟化氢提供
显强酸性的原因是氟化氢提供 和离子
和离子 ,氟离子通过强配位键与
,氟离子通过强配位键与 生成稳定结构的四氟化硼阴离子,于是
生成稳定结构的四氟化硼阴离子,于是 就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸(
就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸( )是最早发现的超强酸,其中Sb采取
)是最早发现的超强酸,其中Sb采取_______ 杂化方式,S采取_______ 杂化方式。
(1)Brian Sales等研究了一类新型热电材料,叫作填隙方钴矿锑化物,在钴和锑形成的晶体空隙中填充入稀土原子La(如图所示),该化合物的化学式为

(2)Co和Fe的逐级电离能数据如表,Fe的
 大于Co的原因是
大于Co的原因是| 元素 |  |  |  |  | 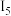 | …… |
| Fe | 462.5 | 1561.9 | 2957 | 5290 | 7240 | |
 | 760.4 | 1648 | 3232 | 4950 | 7670 |
 的熔点73℃,沸点223.5℃,
的熔点73℃,沸点223.5℃, 的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是
的熔点是735℃,沸点是1049℃。两者的熔沸点差异较大的原因是 的空间构型为
的空间构型为(4)为更好地理解超酸的强酸性,实验小组查阅相关资料了解得:混合超强酸
 显强酸性的原因是氟化氢提供
显强酸性的原因是氟化氢提供 和离子
和离子 ,氟离子通过强配位键与
,氟离子通过强配位键与 生成稳定结构的四氟化硼阴离子,于是
生成稳定结构的四氟化硼阴离子,于是 就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸(
就成为了“自由质子”,从而导致整合体系具有非常强的酸性。以此类推,魔酸( )是最早发现的超强酸,其中Sb采取
)是最早发现的超强酸,其中Sb采取
您最近一年使用:0次
2022-11-10更新
|
165次组卷
|
2卷引用:山东省菏泽市2022-2023学年高三上学期期中联考化学(A卷)试题
名校
解题方法
8 . C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式_______ ,C、O、Si三种元素的电负性由大到小的顺序为_______ 。
(2)干冰是分子晶体,其密度比冰大的原因是_______ 。SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为_______ 。
(3)氧化物XO的电子总数与SiC的相等,则X为_______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是_______ 。
(4)向盛有硫酸铜水溶液的试管中加氨水,先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解的原因是:_______ 。
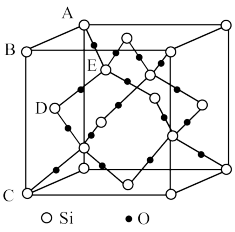
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含_______ 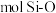 键。如果该立方体的边长为
键。如果该立方体的边长为 ,用
,用 表示阿伏加德罗常数,则SiO2晶体的密度表达式为
表示阿伏加德罗常数,则SiO2晶体的密度表达式为_______  。
。
(1)写出Si的基态原子核外最外层电子排布式
(2)干冰是分子晶体,其密度比冰大的原因是
(3)氧化物XO的电子总数与SiC的相等,则X为
(4)向盛有硫酸铜水溶液的试管中加氨水,先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解的原因是:
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含
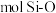 键。如果该立方体的边长为
键。如果该立方体的边长为 ,用
,用 表示阿伏加德罗常数,则SiO2晶体的密度表达式为
表示阿伏加德罗常数,则SiO2晶体的密度表达式为 。
。
您最近一年使用:0次
2022-10-30更新
|
1740次组卷
|
3卷引用:宁夏银川市第六中学2022-2023学年高三上学期第二次月考化学试题
22-23高二上·浙江·期末
9 . 回答下列问题
(1)接近水的沸点的水蒸气的相对分子质量测定值比按化学式H2O计算出来的相对分子质量大一些,主要原因是_______ 。
(2)N2、O2、 F2 跟H2的反应能力依次增强,其原因是_______ 。
(3)H3O+中H-O-H的键角比H2O的_______ (填 “大”或“小”),原因为_______ 。
(4)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
GaF3熔点比GaCl3熔点高很多的原因是_______ 。
(5)已知CoCl2溶液中存在平衡: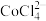 (蓝色)+6H2O
(蓝色)+6H2O 
 (粉红色)+ 4Cl-,将CoCl2溶于一定浓度盐酸后得到紫色溶液,再加水稀释可得到粉红色溶液,用平衡移动理论解释加水稀释后的现象
(粉红色)+ 4Cl-,将CoCl2溶于一定浓度盐酸后得到紫色溶液,再加水稀释可得到粉红色溶液,用平衡移动理论解释加水稀释后的现象_______ 。
(1)接近水的沸点的水蒸气的相对分子质量测定值比按化学式H2O计算出来的相对分子质量大一些,主要原因是
(2)N2、O2、 F2 跟H2的反应能力依次增强,其原因是
(3)H3O+中H-O-H的键角比H2O的
(4)金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
| GaF3 | GaCl3 | GaBr3 | |
| 熔点/°C | > 1000 | 77.75 | 122.3 |
(5)已知CoCl2溶液中存在平衡:
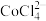 (蓝色)+6H2O
(蓝色)+6H2O 
 (粉红色)+ 4Cl-,将CoCl2溶于一定浓度盐酸后得到紫色溶液,再加水稀释可得到粉红色溶液,用平衡移动理论解释加水稀释后的现象
(粉红色)+ 4Cl-,将CoCl2溶于一定浓度盐酸后得到紫色溶液,再加水稀释可得到粉红色溶液,用平衡移动理论解释加水稀释后的现象
您最近一年使用:0次
名校
10 . 1828年,德国化学家维勒在制备无机盐氰酸铵(NH4OCN)时得到尿素[CO(NH2)2]。尿素的人工合成,揭开了人工合成有机物的序幕。完成下列填空:
(1)将上述元素按原子半径由小到大的顺序排列_______ 。(用元素符号表示)
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式_______ ,其中N元素的化合价为_______ 。
(3)N2H4性质与NH3相似,也可与硫酸反应生成N2H6SO4,则N2H6SO4中存在的作用力为_______ ,N2H6SO4与强碱溶液反应的离子方程式为_______ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2)。
①写出反应的化学方程式,并标出电子转移方向与数目_______ 。
②被氧化的元素是_______ ,还原产物是_______ ,若反应中有3NA个电子发生转移,参与反应的氨的质量为_______ g。
(1)将上述元素按原子半径由小到大的顺序排列
(2)已知氰酸分子内含有叁键,且所有原子最外层均已达到稳定结构,试写出其结构式
(3)N2H4性质与NH3相似,也可与硫酸反应生成N2H6SO4,则N2H6SO4中存在的作用力为
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2)。
①写出反应的化学方程式,并标出电子转移方向与数目
②被氧化的元素是
您最近一年使用:0次
2022-10-13更新
|
172次组卷
|
2卷引用:华东师范大学第一附属中学2022-2023学年高二上学期10月适应性调研化学试题



