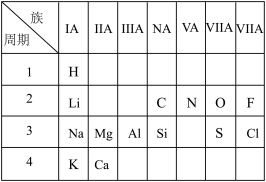
1 . 某研究小组对下列元素周期表(部分)进行研究,回答下列问题。___________ 周期___________ 族。
(2)原子半径最小的元素是___________ 。非金属性最强的元素是___________ 。
(3)钠、镁、铝三种单质中,与冷水反应最剧烈的是___________ 。
(4)KOH和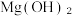 中,碱性较弱的是
中,碱性较弱的是___________ 。
(5)原子核外电子排布中,最外层电子数是内层电子数3倍的元素是___________ 。
(6)能证明Cl元素比S元素非金属性更强的化学反应,其化学方程式为___________ 。
(2)原子半径最小的元素是
(3)钠、镁、铝三种单质中,与冷水反应最剧烈的是
(4)KOH和
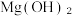 中,碱性较弱的是
中,碱性较弱的是(5)原子核外电子排布中,最外层电子数是内层电子数3倍的元素是
(6)能证明Cl元素比S元素非金属性更强的化学反应,其化学方程式为
您最近一年使用:0次
解题方法
2 . 二硫化硒(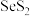 )具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。该物质中存在的化学键为
)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。该物质中存在的化学键为___________ ,已知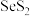 中硫元素的化合价为负价,请从原子结构角度解释原因:
中硫元素的化合价为负价,请从原子结构角度解释原因:___________ 。
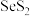 )具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。该物质中存在的化学键为
)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。该物质中存在的化学键为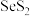 中硫元素的化合价为负价,请从原子结构角度解释原因:
中硫元素的化合价为负价,请从原子结构角度解释原因:
您最近一年使用:0次
3 . 下表显示了元素周期表中短周期的一部分,①~⑥代表6种短周期元素。已知③与氢元素能组成生活中最常见的化合物X。请填写下列空白。
(1)④是___________ (写出元素符号)。
(2)⑥的单质与X反应的化学方程式为___________ 。
(3)①、②、③分别与氢元素组成含10个电子的分子的化学式分别为___________ 、___________ 、___________ 。
| ① | ② | ③ | ||||
| ④ | ⑤ | ⑥ |
(2)⑥的单质与X反应的化学方程式为
(3)①、②、③分别与氢元素组成含10个电子的分子的化学式分别为
您最近一年使用:0次
解题方法
4 . 如表为元素周期表的一部分,参照元素①~⑩在表中的位置,回答下列问题:
(1)写出元素锗(Ge,原子序数32)在元素周期表中的位置___________ 。
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为___________ 。
(3)写出②的单质在足量④的单质中燃烧产物的电子式___________ 。用电子式表示⑤和⑩组成简单化合物的形成过程___________ 。
(4)④和⑨的单质均能与 反应生成的
反应生成的 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性___________ >___________ (填化学式),从原子结构角度解释原因___________ 。
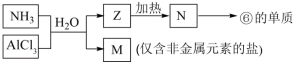
(5)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:___________ (填字母)。
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.Z→N的化学方程式___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(2)第三周期中非金属性最强的元素的原子形成简单离子的结构示意图为
(3)写出②的单质在足量④的单质中燃烧产物的电子式
(4)④和⑨的单质均能与
 反应生成的
反应生成的 型化合物,请判断这两种
型化合物,请判断这两种 型化合物的热稳定性
型化合物的热稳定性(5)由表中①、③、④、⑥、⑩元素形成的常见物质Z、M、N可发生以下反应:
a.离子键 b.极性共价键 c.非极性共价键
ⅱ.Z→N的化学方程式
您最近一年使用:0次
5 . 硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。河南焦作的山药富含硒(Se),有抗癌、抗衰老等重要功能。请回答下列问题。
(1)34Se在周期表中的位置为___________ 。
(2)氧、硫、硒位于同一主族,下列说法正确的是___________(填标号)。
(3)SO2通入SeO2的水溶液中会生成不溶于水的Se,该反应的化学方程式为___________ ;Se能与浓硫酸反应生成SO2和SeO2,则浓硫酸、SO2和SeO2三者中,氧化性最弱的为___________ 。
(4)某混合物中硒主要以Se和CuSe的形式存在,从该混合物中提取硒主要步骤如下:
ⅰ.将该混合物与浓硫酸混合焙烧,产生SO2、SeO2的烟气
ⅱ.用水吸收ⅰ中烟气,可得Se固体
①若用NaOH溶液吸收烟气中的SeO2,则生成一种盐,该盐的化学式为___________ 。
②焙烧时,CuSe与浓H2SO4反应的化学方程式为___________ ,理论上该反应每转移1mol电子,得到的SeO2的质量为___________ g。
(1)34Se在周期表中的位置为
(2)氧、硫、硒位于同一主族,下列说法正确的是___________(填标号)。
| A.还原性:S2->Se2- |
| B.浓硒酸可能具有强氧化性、吸水性 |
| C.稳定性:H2Se>H2S>H2O |
| D.氧化性:O2>Se |
(4)某混合物中硒主要以Se和CuSe的形式存在,从该混合物中提取硒主要步骤如下:
ⅰ.将该混合物与浓硫酸混合焙烧,产生SO2、SeO2的烟气
ⅱ.用水吸收ⅰ中烟气,可得Se固体
①若用NaOH溶液吸收烟气中的SeO2,则生成一种盐,该盐的化学式为
②焙烧时,CuSe与浓H2SO4反应的化学方程式为
您最近一年使用:0次
6 . 1869年,门捷列夫制出了第一张 元素周期表,它的出现是化学发展史上的重要里程碑之一、
(1)元素周期表共有___________ 个周期。其中N元素在周期表中的位置是:___________ 。
(2)在放电或高温下,空气中的 会转化为
会转化为 ,过程如图:
,过程如图:___________ (选填图中编号);写出③的化学反应方程式___________ 。
(3)对“N”“P”元素及其化合物相关性质进行比较,下列说法错误的是___________。
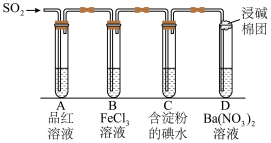
某兴趣小组探究二氧化硫的部分性质,如图所示:
(4)当足量的 进入装置A中后,品红溶液将
进入装置A中后,品红溶液将___________ (填“褪色”或“不褪色”),说明 具有
具有___________ (填“氧化性”或“漂白性”)。
(5)当 进入装置D中后,溶液中产生白色沉淀,其化学式为
进入装置D中后,溶液中产生白色沉淀,其化学式为___________ ,反应的离子方程式表示为___________ 。
(1)元素周期表共有
(2)在放电或高温下,空气中的
 会转化为
会转化为 ,过程如图:
,过程如图: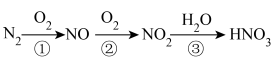
(3)对“N”“P”元素及其化合物相关性质进行比较,下列说法错误的是___________。
A.原子半径大小: |
B.原子得电子的能力: |
C.气态氢化物的热稳定性: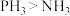 |
D.最高价氧化物对应水化物的酸性: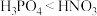 |
某兴趣小组探究二氧化硫的部分性质,如图所示:
(4)当足量的
 进入装置A中后,品红溶液将
进入装置A中后,品红溶液将 具有
具有(5)当
 进入装置D中后,溶液中产生白色沉淀,其化学式为
进入装置D中后,溶液中产生白色沉淀,其化学式为
您最近一年使用:0次
名校
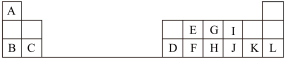
7 . 如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题。(除特别注明外,其他一律用化学式表示)___ 。
(2)元素E的最高价氧化物的电子式是____ 。
(3)某三原子分子有18个电子,该分子的空间构型为____ 。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序为____ 。
(5)H、J、K的最高价氧化物对应的水化物的酸性由强到弱的顺序为____ 。
(6)元素B的最高氧化物的水化物的电子式是___ ,其中含有的化学键为____ 。
(7)把C和D两元素的单质插入氢氧化钠溶液中形成原电池,则正极为____ (填元素名称),该原电池的负极电极反应式____ 。
(2)元素E的最高价氧化物的电子式是
(3)某三原子分子有18个电子,该分子的空间构型为
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序为
(5)H、J、K的最高价氧化物对应的水化物的酸性由强到弱的顺序为
(6)元素B的最高氧化物的水化物的电子式是
(7)把C和D两元素的单质插入氢氧化钠溶液中形成原电池,则正极为
您最近一年使用:0次
名校
解题方法
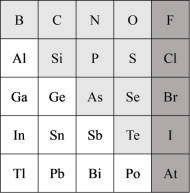
8 . 元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。 在元素周期表中的位置为:
在元素周期表中的位置为:_____ (写出周期和族)。
(2) 的最高正价为
的最高正价为_____ , 的气态氢化物的化学式为
的气态氢化物的化学式为_____ 。
(3)根据元素周期律推断,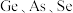 三种元素的原子半径
三种元素的原子半径由小到大 的顺序是____ (填元素符号);阴影部分元素的氢化物最稳定的是_____ (填化学式); 和
和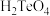 的酸性强弱:
的酸性强弱:
_____ (填“>”“<”或“=”)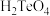 。
。
(4)可在图中分界线(明暗交界处)附近寻找_____(填字母)。
(5)硒( )化铟(
)化铟( )是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。
)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。
(6)工业上提取纳米硒的第一步是向浆化的电冶铜的阳极泥中通入氯气, 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为____ 。
 在元素周期表中的位置为:
在元素周期表中的位置为:(2)
 的最高正价为
的最高正价为 的气态氢化物的化学式为
的气态氢化物的化学式为(3)根据元素周期律推断,
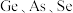 三种元素的原子半径
三种元素的原子半径 和
和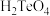 的酸性强弱:
的酸性强弱:
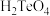 。
。(4)可在图中分界线(明暗交界处)附近寻找_____(填字母)。
| A.农药 | B.合金材料 | C.半导体材料 | D.优良的催化剂 |
 )化铟(
)化铟( )是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。
)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是_____(填字母)。A.原子半径: | B. 的金属性比 的金属性比 强 强 |
C. 的金属性比 的金属性比 弱 弱 | D.硒化铟的化学式为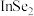 |
 被溶液中的
被溶液中的 氧化为
氧化为 及
及 ,反应中
,反应中 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解题方法
9 . 1869年,俄国化学家门捷列夫编制了一份元素周期表,是化学发展史上的一个里程碑。元素周期表的意思远远超出了化学领域本身,他体现了科学规律的本质。如图是元素周期表的一部分,回答下列问题:
(1)元素周期表中位于金属和非金属的交界处,容易找到的元素是___________。
(2)已知核内有48个中子的硒元素的同位素,下列表示该核素的符号正确的是___________。
(3)硒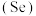 被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。
被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。
(4)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用 清除人体内的活性氧,此时
清除人体内的活性氧,此时 表现出
表现出___________ 性。(填“氧化”或“还原”)
| B | C |  |  |
 |  |  |  |
 |  | 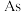 |  |
 |  |  |  |
 |  |  | 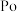 |
| A.制备农药的元素 | B.用于制作半导体材料的元素 |
| C.耐高温的合金元素 | D.制备催化剂的元素 |
A.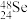 | B. | C.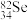 | D.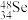 |
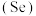 被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。
被誉为“生命的奇效元素”,下列关于硒的描述不正确的是___________。| A.富硒大米中的“硒”指硒元素 | B.最高价氧化物是 |
| C.单质常温下呈固态 | D.硒原子最外层核外电子数为6 |
 清除人体内的活性氧,此时
清除人体内的活性氧,此时 表现出
表现出
您最近一年使用:0次
解题方法
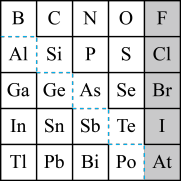
10 . 下图是元素周期表的-部分,请结合该表回答下列问题。_______ ,As的气态氢化物化学式为_______ 。
(2)在完整的周期表中,第三周期半径最大的主族元素是Na,其最高价氧化物对应水化物所含有的化学键是____ 。该元素单质与氧气在常温下反应,得到产物R,用电子式表示R的形成过程___ 。
(3)Al、S、Cl对应的简单离子半径由大到小的顺序是(填离子符号)_______ 。
(4)Cl与S的非金属性何者更强?请用一个化学方程式来证明这个结论:_______ 。
(5)根据元素周期律,推断:
①上图最右一列元素气态氢化物热稳定性最高的是_______ (填对应化学式)。
②可在图中虚线附近寻找_______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(6)硒(Se)化铟(In)是一种新型半导体材料。下列说法正确的是_______(填序号)。
(2)在完整的周期表中,第三周期半径最大的主族元素是Na,其最高价氧化物对应水化物所含有的化学键是
(3)Al、S、Cl对应的简单离子半径由大到小的顺序是(填离子符号)
(4)Cl与S的非金属性何者更强?请用一个化学方程式来证明这个结论:
(5)根据元素周期律,推断:
①上图最右一列元素气态氢化物热稳定性最高的是
②可在图中虚线附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(6)硒(Se)化铟(In)是一种新型半导体材料。下列说法正确的是_______(填序号)。
| A.原子半径:In>Se | B.In比Se易失去电子 |
| C.In的金属性比Al弱 | D.硒化铟的化学式为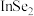 |
您最近一年使用:0次



