名校
解题方法
1 . 下表列出了A~R9种元素在周期表中的位置。请回答下列问题。
(1)在这9种元素中,最外层电子数为1的元素为_____ (填元素符号),化学性质最不活泼的是_____ (填元素符号)。
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(3)F、A、D三种元素的离子半径由大到小的顺序排列为_____ (填离子符号)。
(4)用电子式表示由C和H组成的化合物的形成过程:_____ 。
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为_____ 。
(6)由E和G所形成的化合物中所含有的化学键为_____ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是
(3)F、A、D三种元素的离子半径由大到小的顺序排列为
(4)用电子式表示由C和H组成的化合物的形成过程:
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为
(6)由E和G所形成的化合物中所含有的化学键为
您最近一年使用:0次
2023-12-24更新
|
440次组卷
|
2卷引用:湖南省长郡中学2023-2024学年高一上学期选科适应性调研检测化学试题
名校
2 . 我国的“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。
(1)镓的原子结构示意图为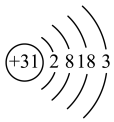 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是___________ 。
(2)GaAs的熔点为1238℃且熔融状态不导电,据此判断它是___________ (填“共价”或“离子”)化合物。
(3)镓与氨气在1100℃下反应生成氮化镓和氢气,该可逆反应每生成1 mol 放出10.3 kJ热量。该反应的热化学方程式是
放出10.3 kJ热量。该反应的热化学方程式是___________ 。(已知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
(4)下列说法错误的是___________ 。
a.氢氧化镓可能具有两性 b.砷化镓具有半导体性质
c.As与 在低温时可剧烈化合为
在低温时可剧烈化合为 d.酸性:
d.酸性:
(1)镓的原子结构示意图为
 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是(2)GaAs的熔点为1238℃且熔融状态不导电,据此判断它是
(3)镓与氨气在1100℃下反应生成氮化镓和氢气,该可逆反应每生成1 mol
 放出10.3 kJ热量。该反应的热化学方程式是
放出10.3 kJ热量。该反应的热化学方程式是(4)下列说法错误的是
a.氢氧化镓可能具有两性 b.砷化镓具有半导体性质
c.As与
 在低温时可剧烈化合为
在低温时可剧烈化合为 d.酸性:
d.酸性:
您最近一年使用:0次
3 . 请根据构造原理,按要求写出下列电子排布式或原子结构示意图:
(1)16S的电子排布式___________ 。
(2)29Cu的简化电子排布式___________ 。
(3)某元素原子的电子排布式为[Ar]3d104s24p3,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第___________ 周期。
②该元素处于元素周期表的第___________ 族。
③试推测该元素处于元素周期表的___________ 区。
(1)16S的电子排布式
(2)29Cu的简化电子排布式
(3)某元素原子的电子排布式为[Ar]3d104s24p3,根据原子核外电子排布与元素在元素周期表中的位置关系,完成下列各题:
①该元素处于元素周期表的第
②该元素处于元素周期表的第
③试推测该元素处于元素周期表的
您最近一年使用:0次
4 . 人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
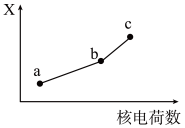
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2023-12-05更新
|
264次组卷
|
3卷引用:湖北省宜城市第一中学等六校2023-2024学年高二上学期期中考试化学试题
名校
5 . 下图是某牙膏成分表的一部分,回答下列问题:
(1)牙膏属于___________ (填“混合物”或“纯净物”)。
(2)含氟牙膏能预防龋齿,这里的“氟”指的是___________ (填“分子”“原子”或“元素”)。
(3)二氧化硅(SiO2)中硅元素的化合价为___________ 。
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈___________ (填“酸性”“碱性”或“中性”)。
| XX牙膏 成分:二氧化硅、水、 纤维素胶、碳酸钠、 香精、单氟磷酸钠、 碳酸氢钠… |
(2)含氟牙膏能预防龋齿,这里的“氟”指的是
(3)二氧化硅(SiO2)中硅元素的化合价为
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈
您最近一年使用:0次
名校
6 . 下图是氮单质及其化合物的“价类二维图”。
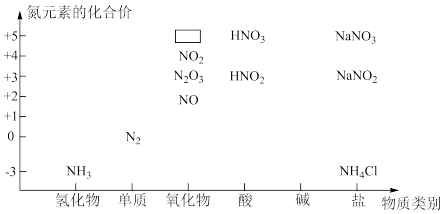
(1)写出氮元素在元素周期表中的位置:_____ 。
(2)图中方框中的化学式为_____ ,氨分子的电子式为_____ ,一水合氨电离可使溶液显碱性,写出一水合氨的电离方程式:_____ 。
(3)向盛有少量NH4Cl溶液的试管中加入NaOH溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是_____ 。
(4)氮的最高价氧化物的水化物为_____ (填写化学式),由于其见光易分解,故常保存在棕色瓶中,其分解的化学方程式为:_____ 。若有4mol该分子发生分解,则过程中转移的电子数目为_____ 。

(1)写出氮元素在元素周期表中的位置:
(2)图中方框中的化学式为
(3)向盛有少量NH4Cl溶液的试管中加入NaOH溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是
(4)氮的最高价氧化物的水化物为
您最近一年使用:0次
名校
7 . 回答下列问题
Ⅰ.有下列物质:① 固体;②熔融的
固体;②熔融的 ;③NH4HCO3晶体;④稀硫酸;⑤
;③NH4HCO3晶体;④稀硫酸;⑤ 胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
(1)上述状态下的物质可导电的是______ (填序号,下同),属于电解质的是_______ 。
(2)a个⑥原子的总质量为b g,则⑥的摩尔质量表示为_______ ,13.6g的②中阴阳离子总数为_______ 。
(3)在小烧杯中加入 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,
溶液,_______ ,即制得物质⑤ 胶体。
胶体。
(4)写出向①的水溶液中加入等物质的量的③的离子方程式:_______ 。
(5)向①溶液中通入少量⑨可产生白色沉淀,继续通入⑨可观察到白色沉淀消失,白色沉淀消失的原因为:_______ (离子方程式表示)
Ⅱ.元素周期表对学生学习化学有着重要的作用。其中过渡元素位于周期表中部,请补充以下元素的符号:
(6)原子序数21-25:_______ 、Ti、_______ 、Cr、Mn
元素周期表中同一纵列元素具有相似的化学性质,请补充以下元素的符号:
(7)第IVA族:C、Si、_______ 、_______ 、_______ 、Fl
Ⅰ.有下列物质:①
 固体;②熔融的
固体;②熔融的 ;③NH4HCO3晶体;④稀硫酸;⑤
;③NH4HCO3晶体;④稀硫酸;⑤ 胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸(1)上述状态下的物质可导电的是
(2)a个⑥原子的总质量为b g,则⑥的摩尔质量表示为
(3)在小烧杯中加入
 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,
溶液, 胶体。
胶体。(4)写出向①的水溶液中加入等物质的量的③的离子方程式:
(5)向①溶液中通入少量⑨可产生白色沉淀,继续通入⑨可观察到白色沉淀消失,白色沉淀消失的原因为:
Ⅱ.元素周期表对学生学习化学有着重要的作用。其中过渡元素位于周期表中部,请补充以下元素的符号:
(6)原子序数21-25:
元素周期表中同一纵列元素具有相似的化学性质,请补充以下元素的符号:
(7)第IVA族:C、Si、
您最近一年使用:0次
名校
8 . 在一百多种化学元素中,非金属占了23种。80%的非金属元素在社会中占重要位置。如C、N、Si、Cl等。
(1)氯元素最外电子层上有___________ 种能量不同的电子,该元素的简单阴离子核外电子排布式是___________ 。
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于___________ 晶体,请写出该化合物的化学式___________ 。
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有___________ (选填编号)。
a.Cl原子最外层电子数比氧多 b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为-2价 d.沸点:H2O>HCl
(1)氯元素最外电子层上有
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有
a.Cl原子最外层电子数比氧多 b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为-2价 d.沸点:H2O>HCl
您最近一年使用:0次
名校
解题方法
9 . 中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ ;乘务员使用的无线通话机的芯片材料所含元素在元素周期中的位置___________ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式___________ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式___________ 。
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石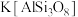 和钠长石
和钠长石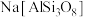 等,
等,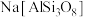 用氧化物形式表示为
用氧化物形式表示为___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石
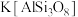 和钠长石
和钠长石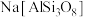 等,
等,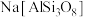 用氧化物形式表示为
用氧化物形式表示为
您最近一年使用:0次
名校
10 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素②、③、⑥的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)②和④组成的物质中含有___________ 键,可以证明该化合物含有此类型化学键的实验事实为___________ 。
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质___________ (填“能”或“不能”)与A反应,说明推测的理由___________ 。
| 周期 | IA | 0 | |||||||
| 1 | IIA | … | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||
(2)②和④组成的物质中含有
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质
您最近一年使用:0次



