名校
1 . 某种牛奶的营养成分表如下所示(NRV%是指每100g食品中营养素的含量占该营养素每日摄入量的比例)。
回答下列问题。
(1)成分表中含有的元素有Na、Ca、H、C、N、O,其中位于同周期的元素是___________ (填元素名称)。
(2)Na在元素周期表中的位置是___________ ,它与氧元素形成的常见化合物中含有非极性共价键,其电子式为___________ 。
(3)比较下列物质的性质,用“>”或“<”填空。
①半径:r(Na+)___________ r(O2-);②沸点:NH3___________ CH4
(4)设计实验证明Ca、Mg都能与水反应,且比较它们与水反应的难易程度。
(限选试剂与仪器:烧杯、小试管、胶头滴管、酚酞、蒸馏水、钙、镁条、砂纸)
| 营养成分表 | ||
| 项目 | 每100g | NRV% |
| 能量 | 309kJ | 4% |
| 蛋白质 | 3.6g | 4% |
| 脂肪 | 4.4g | 7% |
| 碳水化合物 | 5.0g | 2% |
| 钠 | 65mg | 3% |
| 钙 | 120mg | 15% |
(1)成分表中含有的元素有Na、Ca、H、C、N、O,其中位于同周期的元素是
(2)Na在元素周期表中的位置是
(3)比较下列物质的性质,用“>”或“<”填空。
①半径:r(Na+)
(4)设计实验证明Ca、Mg都能与水反应,且比较它们与水反应的难易程度。
(限选试剂与仪器:烧杯、小试管、胶头滴管、酚酞、蒸馏水、钙、镁条、砂纸)
| Ca | Mg | |
| 操作 | 取绿豆大小的一块钙投入盛有水的 | 将打磨后的镁条投入盛有冷水的试管中。 |
| 现象 | 钙先沉入水中,表面产生大量气体,一段时间后上浮,溶液变浑浊。 | 一段时间后,镁条表面有细小气泡产生。 |
| 描述或推测 | ①钙密度比水大; ②溶液中产生的沉淀主要是 | 由细小气泡猜测Mg可能与水发生反应,还需要补充的实验操作及现象是 |
| 结论 | 钙能与水反应生成沉淀和氢气,且反应剧烈。 | 镁能与水缓慢反应,化学方程式为 |
您最近一年使用:0次
2023-07-07更新
|
148次组卷
|
2卷引用:四川省成都市2022-2023学年高二下学期期末零诊测试化学试卷
名校
解题方法
2 . 单质硅是制造太阳能电池板的主要原料,制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为___________ ,下列钴原子的价层电子轨道表示式中,不符合洪特规则的是___________ (填选项字母)。
A.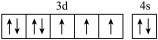 B.
B.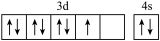
C.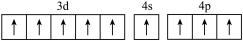 D.
D.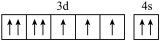
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)钛元素位于元素周期表___________ 区;基态钛原子中,最外层电子的电子云轮廓图为___________ 。
请回答下列问题:
(1)基态硼原子的电子排布式为
A.
 B.
B.
C.
 D.
D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为
(3)钛元素位于元素周期表
您最近一年使用:0次
3 . 元素周期律是对元素性质的规律性总结,元素周期表是这种规律的呈现形式。利用元素周期律可以推测一些未知元素可能的性质。根据你所学的周期律,回答下列问题:
(1)元素周期表有几个周期,几个主族。正确选项是
(2)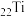 被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
(3)元素周期表中,第三电子层有一个未成对电子的元素有___________种(填序号)。
(1)元素周期表有几个周期,几个主族。正确选项是
| A.6,7 | B.7,7 | C.7,18 | D.7,14 |
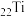 被誉为21世纪明星金属,其最外层电子数为___________(填序号)。
被誉为21世纪明星金属,其最外层电子数为___________(填序号)。| A.1个 | B.2个 | C.3个 | D.5个 |
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
名校
4 . 金属钛被誉为“二十一世纪金属”。回答下列问题:
(1)钛在周期表中的位置___________ ,位于元素周期表中___________ 区,钛原子核外有___________ 种空间运动状态不同的电子,Ti2+电子占据的最高能层的电子排布式为___________ 。
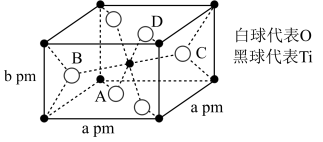
(2)TiO2的晶胞如图所示,则该晶体的密度为___________ g⋅cm-3 (设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛在周期表中的位置
(2)TiO2的晶胞如图所示,则该晶体的密度为

您最近一年使用:0次
名校
5 . 下表是元素周期表的一部分,回答相关问题。
(1)元素①和⑦形成的化合物的化学式为___________ 。
(2)元素⑥的过氧化物的电子式___________ ,其最高价氧化物对应的水化物中含有的化学键类型为___________ 。
(3)元素⑥、⑦、⑧、⑨的简单离子半径由大到小的顺序为___________ (用离子符号表示);元素④、⑤、⑧、⑨的最简单氢化物中稳定性最强的是___________ (填化学式)。
(4)最近,德国科学家实现了铷原子气体超流体态与绝缘体态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。关于铷的下列说法不正确的是___________ (填序号)。
a.与水反应比钠反应更剧烈
b.单质具有很强的氧化性
c.Rb2O在空气中不会吸收水和二氧化碳
d.Rb2O2能与水剧烈反应并释放氧气
e.RbOH的碱性比同浓度的NaOH溶液弱
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)元素⑥的过氧化物的电子式
(3)元素⑥、⑦、⑧、⑨的简单离子半径由大到小的顺序为
(4)最近,德国科学家实现了铷原子气体超流体态与绝缘体态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。关于铷的下列说法不正确的是
a.与水反应比钠反应更剧烈
b.单质具有很强的氧化性
c.Rb2O在空气中不会吸收水和二氧化碳
d.Rb2O2能与水剧烈反应并释放氧气
e.RbOH的碱性比同浓度的NaOH溶液弱
您最近一年使用:0次
2023-06-15更新
|
122次组卷
|
2卷引用:湖南省湘潭县一中2022-2023学年高一下学期期末考试化学试题
名校
6 . 元素在周期表中的位置,反映了元素的原子结构和性质。如图是元素周期表的一部分,请按照要求回答下列问题:
(1)①的元素符号是______ ,元素②位于周期表中的第______ 周期第______ 族。
(2)②、③两种元素中,非金属性较强的是______ (填元素符号)
(3)①、②、④三种元素中,原子半径最大的是______ (填元素符号)。
(4)④、⑤两种元素中最高价氧化物对应的水化物,属于两性氢氧化物的是______ (填化学式)。
(5)常温下,将元素⑥的单质通入 溶液中可制得漂白液,其有效成分是
溶液中可制得漂白液,其有效成分是 ,请写出该反应的离子方程式
,请写出该反应的离子方程式______
| 族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | |||||
(2)②、③两种元素中,非金属性较强的是
(3)①、②、④三种元素中,原子半径最大的是
(4)④、⑤两种元素中最高价氧化物对应的水化物,属于两性氢氧化物的是
(5)常温下,将元素⑥的单质通入
 溶液中可制得漂白液,其有效成分是
溶液中可制得漂白液,其有效成分是 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
2023-06-08更新
|
180次组卷
|
2卷引用:云南省普通高中2021-2022学年高一下学期期末学业水平考试化学试题
解题方法
7 . 水泥是人类最伟大的发明之一,主要成分为硅酸三钙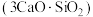 。将其与适量的水反应,形成相互交联的结构,发生的反应为
。将其与适量的水反应,形成相互交联的结构,发生的反应为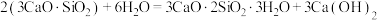 。回答下列问题:
。回答下列问题:
(1)为了加快硅酸三钙与水的反应速率,可采用的方式为_______ (填一种即可)。
(2)Si在元素周期表中的位置为_______ 。
(3) 的电子式为
的电子式为_______ , 的空间结构为
的空间结构为_______ 。
(4)元素C、O、Si、Ca的原子半径由大到小的顺序为_______ 。
(5)带有玻璃塞的磨口玻璃瓶不能用来盛装NaOH溶液的原因为_______ (用化学方程式表示)。
(6)写出 在农业上的一种用途:
在农业上的一种用途:_______ 。
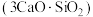 。将其与适量的水反应,形成相互交联的结构,发生的反应为
。将其与适量的水反应,形成相互交联的结构,发生的反应为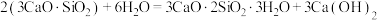 。回答下列问题:
。回答下列问题:(1)为了加快硅酸三钙与水的反应速率,可采用的方式为
(2)Si在元素周期表中的位置为
(3)
 的电子式为
的电子式为 的空间结构为
的空间结构为(4)元素C、O、Si、Ca的原子半径由大到小的顺序为
(5)带有玻璃塞的磨口玻璃瓶不能用来盛装NaOH溶液的原因为
(6)写出
 在农业上的一种用途:
在农业上的一种用途:
您最近一年使用:0次
2023-06-07更新
|
62次组卷
|
2卷引用:广东省汕头市2022-2023学年高一下学期4月期中考试化学试题
8 . 化学是一门实用性很强的科学。请根据题意填空:
(1)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有______ (填“钠”或“钾”)元素;
(2)在金属元素中,有一类金属既可单独使用,也可用于生产合金。在合金中加入该类金属,能大大改善合金的性能,因而,该类金属又被称为“冶金工业的维生素”。则该类金属是______ (填“稀土金属”或“碱土金属”);
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有______ (填“Fe2O3”或“Fe3O4”)。
(1)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有
(2)在金属元素中,有一类金属既可单独使用,也可用于生产合金。在合金中加入该类金属,能大大改善合金的性能,因而,该类金属又被称为“冶金工业的维生素”。则该类金属是
(3)中国古代最早的指南针“司南”,其具有磁性作用是因为主要含有
您最近一年使用:0次
名校
9 . 消毒剂在新冠疫情期间具有重要作用。消毒剂除了常见的有体积分数75%的医用酒精、漂白液溶液,还有高铁酸钾。
I.高铁酸钾 是一种比
是一种比 、
、 和
和 的氧化能力强的强氧化剂和消毒剂。
的氧化能力强的强氧化剂和消毒剂。
(1)下列基态原子或离子的电子排布式或排布图中,违反洪特规则的是_______ ;违反泡利原理的是_______ 。
① :
: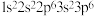
② :
: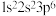
③P:
④Fe:
⑤ :
: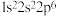
⑥C: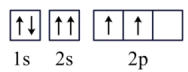
(2)高铁酸钾在水质处理中发挥着重要作用。查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:_______ 。
Ⅱ、关于原子表示时,我们也用 格式表示原子:请回答以下问题
格式表示原子:请回答以下问题
(3)中性原子的中子数N=_______ 。(用A和Z表示)
(4)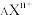 共有X个电子,则该阳离子的中子数N=
共有X个电子,则该阳离子的中子数N=_______ 。(用A、X、n表示)
Ⅲ、喷洒家用“84”消毒液是预防病毒的有效方法,某实验小组探究某品牌“84”消毒液的性质,取某品牌“84”消毒液5mL进行如表实验。
(5)写出实验室制备“84”消毒液反应的化学方程式:_______ 。
(6)查阅资料:酚酞的变色范围为8.2~10.0,且酚酞在强碱性溶液中红色会褪去。为探究操作a中溶液褪色的原因,又补充了如下实验(请将横线内容补充完整)。
获得结论:此实验小组使用的上述消毒液具有_______ 性。
I.高铁酸钾
 是一种比
是一种比 、
、 和
和 的氧化能力强的强氧化剂和消毒剂。
的氧化能力强的强氧化剂和消毒剂。(1)下列基态原子或离子的电子排布式或排布图中,违反洪特规则的是
①
 :
: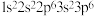
②
 :
: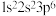
③P:

④Fe:

⑤
 :
: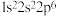
⑥C:

(2)高铁酸钾在水质处理中发挥着重要作用。查阅资料可知:干燥的高铁酸钾在常温下可以长期稳定存在,但溶于水中极易分解得到氧气和氢氧化铁胶体,写出该反应的化学方程式:
Ⅱ、关于原子表示时,我们也用
 格式表示原子:请回答以下问题
格式表示原子:请回答以下问题(3)中性原子的中子数N=
(4)
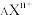 共有X个电子,则该阳离子的中子数N=
共有X个电子,则该阳离子的中子数N=Ⅲ、喷洒家用“84”消毒液是预防病毒的有效方法,某实验小组探究某品牌“84”消毒液的性质,取某品牌“84”消毒液5mL进行如表实验。
| 操作 | 现象 |
| a.测溶液pH,并向其中滴加2滴酚酞 |  ,溶液变红,5min后褪色 ,溶液变红,5min后褪色 |
| b.向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(6)查阅资料:酚酞的变色范围为8.2~10.0,且酚酞在强碱性溶液中红色会褪去。为探究操作a中溶液褪色的原因,又补充了如下实验(请将横线内容补充完整)。
| 操作 | 现象 |
| 取 | 溶液变红,30min后褪色 |
您最近一年使用:0次
名校
解题方法
10 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。Li位于周期表中_____ 区;基态Ti原子的价电子排布式为_____ ;基态Fe3+、Fe2+离子中未成对的电子数之比为_____ 。
您最近一年使用:0次



