名校
解题方法
1 . 实验室加热液体时常加入沸石,其主要成分为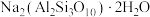 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:
(1)元素Si在周期表中的位置是_______ 。
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式);Na与同周期非金属性最强的元素形成的化合物可做调味品,用电子式表示该化合物的形成过程_______ 。
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是_______ (填化学式)。
(4)Na所在周期的主族元素中,简单离子半径最小的是_______ (填离子符号)
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
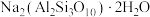 。根据其组成元素完成下列填空:
。根据其组成元素完成下列填空:(1)元素Si在周期表中的位置是
(2)沸石中的元素可形成多种化合物;Na元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
(3)与氧元素同周期的非金属元素中,简单气态氢化物最稳定的是
(4)Na所在周期的主族元素中,简单离子半径最小的是
(5)2022年我国科学家开始参与研究Uue新元素的合成。Uue与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
2 . 分析下列图表,回答问题。
(1)N、Al、Si、Ge四种元素中,某种元素的电离能数据如下:
则该元素是_______ (填写元素符号)。
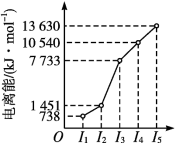
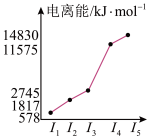
(2)短周期某主族元素M的电离能情况如图所示。则M元素位于周期表的第_______ 族。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价层电子排布式:_______ ,比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_______ 。
(1)N、Al、Si、Ge四种元素中,某种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | …… |
| In/( kJ∙mol−1) | 578 | 1 817 | 2 745 | 11 575 | …… |
(2)短周期某主族元素M的电离能情况如图所示。则M元素位于周期表的第

(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| I1 | 717 | 759 | |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
您最近一年使用:0次
2023高三·全国·专题练习
3 . 元素周期表中的特殊位置_______

(1)请在上表中画出元素周期表的轮廓,并标出周期序数和族序数。
(2)画出金属与非金属的分界线,写出分界线处金属的元素符号,并用阴影表示出过渡元素的位置。
(3)写出各周期元素的种类。
(4)写出稀有气体元素的原子序数。
(5)标出113号~118号元素的位置。
(6)根据元素原子价电子排布的特征,标出元素周期表分区情况。

(1)请在上表中画出元素周期表的轮廓,并标出周期序数和族序数。
(2)画出金属与非金属的分界线,写出分界线处金属的元素符号,并用阴影表示出过渡元素的位置。
(3)写出各周期元素的种类。
(4)写出稀有气体元素的原子序数。
(5)标出113号~118号元素的位置。
(6)根据元素原子价电子排布的特征,标出元素周期表分区情况。
您最近一年使用:0次
名校
解题方法
4 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p的原子结构示意图为___________________ 。
(2)o、p两元素的部分电离能数据如下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_________________________________________________________ 。
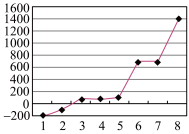
(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是___________________ (填图1中的序号)。
(4)表中所列的某主族元素的电离能情况如图所示,则该元素是___________________ (填元素符号)。
(5)基态钒原子的价电子排布图为___________________ 。
(6)写出单电子数最多的原子的电子排布式:__________________________________________ 。
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
(1)元素p的原子结构示意图为
(2)o、p两元素的部分电离能数据如下表:
元素 元素电离能/  | o | p |
| 717 | 759 |
| 1509 | 1561 |
| 3248 | 2957 |
比较两元素的
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是

(4)表中所列的某主族元素的电离能情况如图所示,则该元素是

(5)基态钒原子的价电子排布图为
(6)写出单电子数最多的原子的电子排布式:
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
A.[Ne]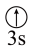 | B.[Ne]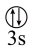 | C.[Ne]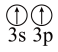 | D.[Ne] |
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
5 . 元素周期表的结构
(1)编排原则

(2)元素周期表的结构

②族的分类

③常见族的别称:第IA族(除氢外)—__________ ,VIIA—__________ ,0族—________________ ,IVA、VA、VIA族依次又叫_______________________ 。
(1)编排原则

(2)元素周期表的结构

②族的分类

③常见族的别称:第IA族(除氢外)—
您最近一年使用:0次
解题方法
6 . 目前,人们能够合成自然界中不存在的物质,人们能不能制造出自然界中不存在的元素______ ?请查阅资料说明。
您最近一年使用:0次
2022-11-25更新
|
54次组卷
|
2卷引用:苏教2020版选择性必修2专题1第三单元 物质结构研究的意义课后习题
名校
解题方法
7 . 已知元素周期表中共有18纵行。如图所示实线表示元周期表的边界,按电子排布,可把元素周期表划分为s区、p区、d区、ds等,除ds区外,其他区的名称均按构造原理最后填入电子的能级符号来命名。
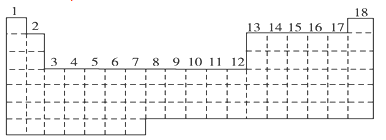
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区_____ 。
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)_____ 。
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:___________ 。
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并标记分区
(2)有的同学受这种划分的启示,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中标出4s轨道半充满的元素(用元素符号表示)
(4)请利用电子排布的相关知识解释Fe3+比Fe2+稳定的原因:
(5)随着科学技术的发展,不断有新的元素被发现。现在第七周期已经排满,则元素周期表共可以排布
您最近一年使用:0次
2022-10-20更新
|
157次组卷
|
2卷引用:河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题
解题方法
8 . 如图是元素周期表的一部分,回答下列问题:
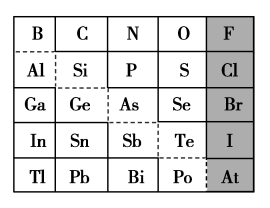
(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_______ H2SeO4(填“>”或“<”下同)。
③氢化物的还原性:H2O_______ H2S。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次
解题方法
9 . 下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是___________ ;
(2)N、O、F三种元素中,非金属性最强的是___________ (填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为___________ ;
(4)碘与氯是同主族元素。下面关于碘的推断错误的是___________ (选填字母);
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(1)钠元素在元素周期表中的位置是
(2)N、O、F三种元素中,非金属性最强的是
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为
(4)碘与氯是同主族元素。下面关于碘的推断错误的是
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为
您最近一年使用:0次





