1 . 铍在 一定条件下可形成Na2BeO2。 下列有关铍及其化合物的叙述中,正确的是
| A.氧化铍不能溶于盐酸 | B.氢氧化铍易溶于水 |
| C.铍的金属性比镁强 | D.Na2BeO2溶液呈碱性 |
您最近一年使用:0次
2 . 如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
(1)③、④、⑦的原子半径由大到小的顺序是_______ (用元素符号表示)。
(2)请写出①和⑨两种元素形成的10电子分子的电子式_______ 。
(3)下列事实能说明元素②的非金属性比元素⑥的非金属性强的是_______ (填字母)。
A.②的单质与元素⑥的简单氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mol②单质比1mol⑥单质得电子多
C.②和⑥两元素的简单氢化物受热分解,前者的分解温度高
(4)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式:_______ 。
(5)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式:_______ 。
| IA | 0 | |||||||
| 一 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 二 | ⑧ | ⑨ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)请写出①和⑨两种元素形成的10电子分子的电子式
(3)下列事实能说明元素②的非金属性比元素⑥的非金属性强的是
A.②的单质与元素⑥的简单氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mol②单质比1mol⑥单质得电子多
C.②和⑥两元素的简单氢化物受热分解,前者的分解温度高
(4)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式:
(5)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式:
您最近一年使用:0次
2021-07-07更新
|
104次组卷
|
2卷引用:四川省广安市2020-2021学年高二下学期期末考试化学联考试题
3 . 中学化学中很多“规律”都有其适用范围,下列根据“规律”推出的结论合理的是
| A.根据MgO的熔点高于CaO,推出MgCO3热分解温度比CaCO3高 |
| B.根据主族元素最高正化合价与族序数的关系,推出第VIA元素最高正价都是+6价 |
| C.根据同周期元素的电负性变化趋势,推出Ar的电负性比Cl大 |
| D.根据对角线规则,推出Be(OH)2和NaOH溶液能反应生成Na2BeO2 |
您最近一年使用:0次
4 . 下列各组元素中不符合“对角线法则”的是
| A.Li、Mg | B. P、C | C.B、Si | D.Be、Al |
您最近一年使用:0次
5 . 短周期主族元素W、X、Y、Z的原子序数依次增大,它们可组成如图所示的化合物,其中,W与Z同主族,X的核外电子数与Y的最高能层上的电子数相同。下列说法错误的是
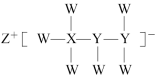
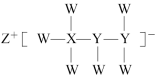
| A.ZW属于共价化合物 |
| B.YH3分子的键角大于YF3分子的键角 |
| C.与X的化学性质最相似的邻族元素是Si |
| D.XF3和YF3中X与Y的杂化方式均为sp2杂化 |
您最近一年使用:0次
20-21高二下·浙江·阶段练习
解题方法
6 . (1) HNO3失去OH-之后形成 中间体,
中间体, 中所有原子满足稳定结构,写出
中所有原子满足稳定结构,写出 的电子式
的电子式________ 。
(2)在元素周期表中,某些主族元素与其右下方的主族元素有些性质相似。写出Be(OH)2与NaOH溶液反应的离子方程式_______________________ 。
(3) AlF3的熔点(1040℃) 比AlBr3的熔点(194℃)高得多,主要原因_________________________ 。
 中间体,
中间体, 中所有原子满足稳定结构,写出
中所有原子满足稳定结构,写出 的电子式
的电子式(2)在元素周期表中,某些主族元素与其右下方的主族元素有些性质相似。写出Be(OH)2与NaOH溶液反应的离子方程式
(3) AlF3的熔点(1040℃) 比AlBr3的熔点(194℃)高得多,主要原因
您最近一年使用:0次
7 . 铍(4Be)的右下角元素是铝,根据“对角线规则”,下列描述不正确的
| A.BeO是两性氧化物 |
| B.已知AlCl3是共价化合物,则BeCl2也可能是共价化合物 |
| C.Be(OH)2既能与H2SO4溶液反应也能与NaOH溶液反应 |
| D.Be(OH)2与NaOH溶液反应后生成NaBeO2和H2O |
您最近一年使用:0次
2021-05-11更新
|
263次组卷
|
2卷引用:四川省成都市郫都区2020-2021学年高二下学期期中考试化学试题
8 . 化学学习中常用类推方法,下列类推正确的是
| A.CO2为非极性分子,SO2也为非极性分子 |
| B.固态CO2是分子晶体,固态SiO2也是分子晶体 |
| C.NH3的VSEPR模型为四面体,BF3的VSEPR模型也为四面体 |
| D.Al(OH)3能溶于NaOH溶液,Be(OH)2也能溶于NaOH溶液 |
您最近一年使用:0次
名校
9 . 氨硼烷(NH3BH3)和乙烷的结构相似,含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。下列说法错误的是
| A.H、B、N三种元素中,电负性最大的是N |
| B.根据对角线规则,B、Si最高价氧化物对应的水化物均为二元酸 |
| C.氨硼烷N采取sp3杂化,B采取sp3杂化 |
| D.NH3BH3属于分子晶体,晶体中存在的化学键有极性键和配位键 |
您最近一年使用:0次
2021-05-03更新
|
345次组卷
|
3卷引用:河南省辉县市一中2020-2021学年高二下学期第二次阶段性考试化学试题
河南省辉县市一中2020-2021学年高二下学期第二次阶段性考试化学试题辽宁省朝阳市2021届高三下学期3月普通高等学校招生全国统一模拟(一模) 化学试题(已下线)卷14 物质结构与性质选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)
名校
10 . 元素周期表中对角线原则是指某些相邻两个主族上下相差一个周期的元素之间性质相似规律,比如铍(Be)与铝的性质相似,则下列推断中,正确的是
| A.常温下BeCl2溶液pH>7 |
| B.BeCl2溶液能导电,说明BeCl2一定是离子化合物 |
| C.Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
D.Be与NaOH溶液反应的离子方程式为:2Be+2OH-+2H2O=2BeO +3H2↑ +3H2↑ |
您最近一年使用:0次
2021-04-09更新
|
183次组卷
|
2卷引用:四川省成都外国语学校2020-2021学年高二4月月考化学试题



