1 . 已知用某元素M制备化合物R的反应为3M2++2Y2O +O2+
+O2+ OH-=R+Y4O
OH-=R+Y4O +2H2O,则下列叙述中错误的是
+2H2O,则下列叙述中错误的是
 +O2+
+O2+ OH-=R+Y4O
OH-=R+Y4O +2H2O,则下列叙述中错误的是
+2H2O,则下列叙述中错误的是| A.元素M不可能为非金属元素 |
| B.元素M不可能为Ca元素 |
| C.R中M元素的化合价是+3 |
| D.反应中的M2+,被氧化与未被氧化的个数之比为2:1 |
您最近一年使用:0次
2023-09-16更新
|
61次组卷
|
2卷引用:湖北省十堰市郧阳中学2022-2023学年高一上学期10月月考化学试题
名校
解题方法
2 . 短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的价电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物的电子式为___________ 。
(2)已知:① ;△
;△
② ;
;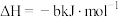
③ ;
; (“•”表示形成共价键所提供的电子)
(“•”表示形成共价键所提供的电子)
写出298 K时,A2与E2反应的热化学方程式___________ 。
(3)在某温度下、容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应: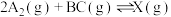 ;
;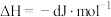 (
(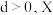 为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则该时间段内A2的平均反应速率为___________ 。
②该温度下此反应的平衡常数K的值为___________ 。
③三个容器中的反应分别达平衡时各组数据关系正确的是___________ (填序号)。
A.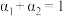 B.
B. C.
C.
D.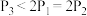 E.
E. F.
F.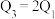
(4)近年来,我国科研人员研制出一种一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为: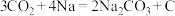 。
。
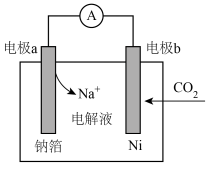
①电极a为___________ 极(填“正”或“负”)。
②电极b发生的电极反应为___________ 。
(1)A、C、D形成的化合物的电子式为
(2)已知:①
 ;△
;△
②
 ;
;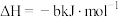
③
 ;
; (“•”表示形成共价键所提供的电子)
(“•”表示形成共价键所提供的电子)写出298 K时,A2与E2反应的热化学方程式
(3)在某温度下、容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:
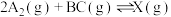 ;
;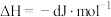 (
(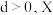 为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5 mol | n2 | n3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |  |  |  |
②该温度下此反应的平衡常数K的值为
③三个容器中的反应分别达平衡时各组数据关系正确的是
A.
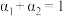 B.
B. C.
C.
D.
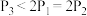 E.
E. F.
F.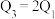
(4)近年来,我国科研人员研制出一种一种室温下“可呼吸”的Na-CO2电池装置如图所示,电池的总反应为:
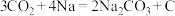 。
。
①电极a为
②电极b发生的电极反应为
您最近一年使用:0次
2023-08-11更新
|
135次组卷
|
2卷引用:湖北省十堰市等5地十堰市郧阳中学等2校2022-2023学年高二上学期10月月考化学试题
名校
解题方法
3 . 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与 剧烈化合并发生爆炸。回答下列问题:
剧烈化合并发生爆炸。回答下列问题:
(1)下列说法不正确的是_______
(2)T的最高价氧化物的水化物与氢氧化铝反应的化学方程式_______ ;
(3)画出Q的原子结构示意图_______ ;
(4)原子序数比Q大18的元素Y和元素R形成化合物 ,实验表明液态
,实验表明液态 具有一定的导电性,研究人员发现产生这一现象的可能原因在于
具有一定的导电性,研究人员发现产生这一现象的可能原因在于 的自偶电离(类似于:
的自偶电离(类似于: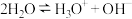 ),电离生成的+1价阳离子为
),电离生成的+1价阳离子为_______ ,-1价阴离子为_______ ; 和水反应生成两种酸,化学方程式是
和水反应生成两种酸,化学方程式是_______ 。
 剧烈化合并发生爆炸。回答下列问题:
剧烈化合并发生爆炸。回答下列问题:| R | ||
| X | T | Z |
| Q |
A.最高价氧化物对应的水化物的酸性: |
| B.R与Q的电子数相差26 |
C.气态氢化物的稳定性: |
| D.五种元素中Z的化学性质最稳定 |
(3)画出Q的原子结构示意图
(4)原子序数比Q大18的元素Y和元素R形成化合物
 ,实验表明液态
,实验表明液态 具有一定的导电性,研究人员发现产生这一现象的可能原因在于
具有一定的导电性,研究人员发现产生这一现象的可能原因在于 的自偶电离(类似于:
的自偶电离(类似于: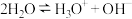 ),电离生成的+1价阳离子为
),电离生成的+1价阳离子为 和水反应生成两种酸,化学方程式是
和水反应生成两种酸,化学方程式是
您最近一年使用:0次
名校
解题方法
4 . 两种化合物的结构简式(端点、交叉点代表碳原子,氢原子已略去)如图,其中X、Y、Z、R、Q是原子序数依次增大的五种短周期主族元素,X、Y、Z、R为同周期元素,X最外层电子数为内层电子数的2倍。下列说法错误的是


| A.Q的最高价氧化物对应水化物是弱酸 |
| B.Z的某种同素异形体在大气中的含量与环境污染密切相关 |
| C.将装有YZ2气体的透明密闭容器浸入冰水中,气体颜色变深 |
| D.X、Y、Z、R、Q中,R的非金属性及简单氢化物的稳定性均最强 |
您最近一年使用:0次
2022-12-17更新
|
151次组卷
|
2卷引用:湖北省东风高中、天门中学、仙桃中学2022-2023学年高三上学期12月月考化学试题
5 . 元素X、Y、Z、W、R为原子半径依次递增的短周期元素,其中X、Z、R三元素分别位于三个不同周期。它们形成的一种重要的医药中间体的结构式如图所示。

下列说法错误的是

下列说法错误的是
| A.电负性大小:X<Z<Y |
B.1mol该医药中间体分子中含有的 键数为 键数为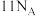 |
| C.Y形成的氢化物的沸点一定高于Z形成的氢化物的沸点 |
| D.最高价含氧酸的酸性为:W>R>Z |
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、W四种化合物均由短周期元素组成。其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
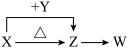
(1)W的电子式是____ 。
(2)X与Y在溶液中反应的离子方程式是____ 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用如图装置(夹持固定装置已略去)进行实验。

①若装置III中产生白色沉淀,装置V中可收集到一种无色气体。则装置I中反应的化学方程式是_____ 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体(试剂另选),则该化合物的电子式是_____ ,所需仪器装置是_____ 。(从图中选择必要装置,填写编号)
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是_____ 。
(5)城市饮用水处理新技术用NaClO2、高铁酸钠代替Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是_____ 。

(1)W的电子式是
(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用如图装置(夹持固定装置已略去)进行实验。

①若装置III中产生白色沉淀,装置V中可收集到一种无色气体。则装置I中反应的化学方程式是
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置V中气体(试剂另选),则该化合物的电子式是
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是
(5)城市饮用水处理新技术用NaClO2、高铁酸钠代替Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是
您最近一年使用:0次
名校
7 . 短周期主族元素W、X、Y、Z的原子序数依次增加。A是元素Y的单质,丙、丁、戊是由这些元素组成的二元化合物,丙是有漂白性的无色气体,戊是常用的绿色氧化剂,丁和戊含有相同的元素种类,A为常见金属且能与强碱溶液反应,甲是Z的最高价氧化物对应水化物,Z的最高价和最低价的代数和等于4。上述物质的转化关系如图所示。下列说法正确的是
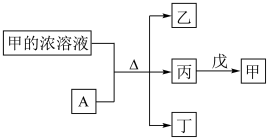

| A.气态氢化物的还原性:X>Z | B.气态氢化物的沸点:X<Z |
| C.X与Z形成的一种化合物可以作为食品添加剂 | D.简单离子半径大小:X<Y<Z |
您最近一年使用:0次
名校
8 . a、b、c、d四种元素在周期表中的位置如图所示,则下列说法正确的是
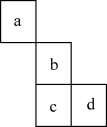

| A.a与b之间容易形成离子化合物 |
| B.若b的最高价氧化物对应水化物为H2bO4,则a的氢化物的化学式为aH3 |
| C.若b的单质与H2易化合,则c的单质与H2更易化合 |
| D.若b的单质可做半导体材料,则c的单质不可能为半导体材料 |
您最近一年使用:0次
9 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。

回答下列问题:
(1)写出物质R的电子式。_______ 。
(2)下列有关图中所示含N、S物质的叙述,正确的是_______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是_______ 。
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析, 晶体中所含化学键的类型有
晶体中所含化学键的类型有_______ ,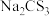 水溶液显
水溶液显_______ (填“酸性”、“碱性”或“中性”)。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: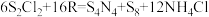 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有_______ ,该反应每生成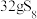 转移电子
转移电子_______  。其中被氧化的元素是
。其中被氧化的元素是_______ (填元素符号)。

回答下列问题:
(1)写出物质R的电子式。
(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与
 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将
 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析,
 晶体中所含化学键的类型有
晶体中所含化学键的类型有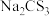 水溶液显
水溶液显(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: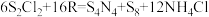 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有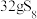 转移电子
转移电子 。其中被氧化的元素是
。其中被氧化的元素是
您最近一年使用:0次
10 . 卤化金能与亚乙基硫脲形成盐,结构如图所示。其中X代表卤素原子,W的丰度最大的一种核素原子核无中子,原子半径M>Y>Z,且M的最高正价与最低负价代数和为4,下列说法不正确 的是


| A.简单氢化物的键角:Y>Z |
| B.M最外层电子有6种空间运动状态 |
| C.该盐中Y、Z、M均达到8电子稳定结构 |
D.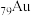 原子中电子填入的最高能级为6s 原子中电子填入的最高能级为6s |
您最近一年使用:0次
2022-11-03更新
|
168次组卷
|
2卷引用:湖北省鄂东南联盟2022-2023学年高三上学期期中联考化学试题



