名校
1 . 4种相邻的主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。回答下列问题:
(1)元素x在周期表中的位置是第____ 。其单质可采用电解熔融的___ 方法制备。用电子式表示该化合物的形成过程:___ 。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是____ ,碱性最强的是____ 。(填化学式)
(3)气体分子(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是____ 。
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是第
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是
(3)气体分子(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是
您最近一年使用:0次
10-11高三·河北衡水·阶段练习
2 . 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:
(1)画出B的离子结构示意图______ ;写出D元素最高价氧化物的水化物电子式_________
(2)盐X水溶液显____ (填“酸”“碱”“中”)性,用离子方程式解释其原因________________
(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为________
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同。Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。该燃料电池放电时,正极的电极反应式是________________________________
(5)如右图是一个电解过程示意图。
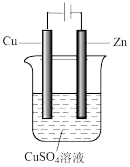
假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)_______________ L
| 元素 | 有关信息 |
| A | 元素主要化合价为—2,原子半径为0.074 n m |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102 n m,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物的水化物,能按1∶1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075 n m,最高价氧化物的水化物与其氢化物组成一种盐X |
(2)盐X水溶液显
(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同。Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。该燃料电池放电时,正极的电极反应式是
(5)如右图是一个电解过程示意图。

假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)
您最近一年使用:0次
3 . I.A〜G七种元素中,除F外其他均为短周期主族元素,它们的原子结构或性质如下表所示:
请回答下列问题:
(1)A在元素周期表中的位置是_______ ;F的原子结构示意图是_____________ 。
(2)下列事实能证明C和E的非金属性强弱的是_____ 。(填序号)
①常温下,C的单质呈气态,E的单质呈固态②C的气态氢化物的温定性强于E的气态氢化物的温定性③C与E形成的化合物中,E呈正价④E的氢化物的沸点高于于C的氢化物的沸点
(3)由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是______ (填化学式),它与足量NaOH溶液在加热时反应的离子方程式为:_______ 。
(4)A的氢化物有多种,1 molA的某种氢化物分子中含有14mol电子,请写出该氢化物的电子式:______ 。已知在25℃、101kPa下,1g该氢化物在足量氧气中完全燃烧生成液态水时放出的热量为40kJ,写出该氢化物燃烧热:_________ 。
Ⅱ.甲、乙、丙,丁均为上述元素所形成的物质,甲是单质。它们之间有如下的反应关系:
(5)若乙为淡黄色固体,②③反应均用到同一种液态氢化物,丁物质常用于食品工业。乙所含化学键的类型是________ 。写出乙→丙的化学方程式:__________ 。
(6)若丁物成质具有两性,②③反应均要用强碱溶液,④反应是通入过量的—种引起温室效应的主要气体。写出丙→丁的离子方程式:__________ 。室温下,若由丁物质形成的水溶液中甲离子浓度为1.3×10-6mol·L-1,则该溶液的pH为______ 。
(丁的Ksp为1.3×10-33)
| 元素 | 原子结构或性质 |
| A | 其形成的一种同位素原子在考古中可推测化石的年代 |
| B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
| C | 地壳中含量最多的元素 |
| D | D原子的最外层电子数与其电子层数相同,是地壳中含量多的金属元素 |
| E | 其单质主要存在于火山口附近 |
| F | 生活中常见的金属,它的某种氧化物具有磁性 |
| G | G原子与D原子同周期,且原子半径是同周期元素中最大的 |
(1)A在元素周期表中的位置是
(2)下列事实能证明C和E的非金属性强弱的是
①常温下,C的单质呈气态,E的单质呈固态②C的气态氢化物的温定性强于E的气态氢化物的温定性③C与E形成的化合物中,E呈正价④E的氢化物的沸点高于于C的氢化物的沸点
(3)由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是
(4)A的氢化物有多种,1 molA的某种氢化物分子中含有14mol电子,请写出该氢化物的电子式:
Ⅱ.甲、乙、丙,丁均为上述元素所形成的物质,甲是单质。它们之间有如下的反应关系:
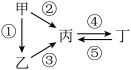
(5)若乙为淡黄色固体,②③反应均用到同一种液态氢化物,丁物质常用于食品工业。乙所含化学键的类型是
(6)若丁物成质具有两性,②③反应均要用强碱溶液,④反应是通入过量的—种引起温室效应的主要气体。写出丙→丁的离子方程式:
(丁的Ksp为1.3×10-33)
您最近一年使用:0次
2012·河北石家庄·一模
名校
解题方法
4 . 由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种或两种以上元素,它们分子中质子总数均与氩原子的质子数相同,已知甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第2周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲含有某相同元素,且该元素在二者中的百分含量相同,则丁中一定含有-l价元素 |
您最近一年使用:0次
2016-12-09更新
|
370次组卷
|
5卷引用:2012届河北省石家庄市高三补充题、压轴题化学试卷
(已下线)2012届河北省石家庄市高三补充题、压轴题化学试卷2013届河北省衡水中学高三第二次模拟考试化学试卷12013届河北省衡水中学高三第二次模拟考试化学试卷 22017届湖南省衡阳市第八中学高三实验班第三次质检化学试卷安徽省滁州市定远县育才学校2021届高三上学期第三次月考化学试题
真题
名校
5 . 短周期元素甲、乙、丙、丁的原子序数依次增大,甲和丁的原子核外均有两个未成对电子,乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应。下列说法错误的是
| A.元素丙的单质可用于冶炼金属 |
| B.甲与丁形成的分子中有非极性分子 |
| C.简单离子半径:丁 > 乙 > 丙 |
| D.甲与乙形成的化合物均有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
1411次组卷
|
8卷引用:江苏省南通市2023-2024学年高三下学期化学调研测试卷
江苏省南通市2023-2024学年高三下学期化学调研测试卷 2015年全国普通高等学校招生统一考试化学(上海卷)2016届黑龙江省哈尔滨第六中学高三上期中测试化学试卷2016届山西省山西大学附属中学高三上12月月考化学试卷(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训吉林省长春市东北师大附中2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分四川省武胜烈面中学校2019-2020学年高二下学期期中考试化学试题
名校
6 . 五种短周期元素A、B、C、D、E、F的原子序数依次增大.A和C同族,B和E同族,C离子和B离子具有相同的电子层结构,D的最外层电子数与电子层数相同.A和B、E、F均能形成共价化合物(由分子构成的化合物).A和B形成的化合物在水中呈碱性,C和F形成的化合物在水中呈中性.
回答下列问题:
(1)五种元素中,原子半径最大的是______ (填元素名称).最高价氧化物对应水化物酸性最强的元素为____ (填元素符号),其最高价氧化物对应水化物与NaOH反应的离子方程式为___________________________ .
(2)由A和B、E、F所形成的化合物中,热稳定性最差的是_________________ (用化学式表示).
(3)A和F形成的化合物与A和B形成的化合物反应,产物的化学式为________ .
(4)D元素最高价氧化物的化学式为_______ ,最高价氧化物对应水化物与氢氧化钠反应的离子方程式为___________________________ .
(5)单质F与水反应的离子方程式为___________________ ..
回答下列问题:
(1)五种元素中,原子半径最大的是
(2)由A和B、E、F所形成的化合物中,热稳定性最差的是
(3)A和F形成的化合物与A和B形成的化合物反应,产物的化学式为
(4)D元素最高价氧化物的化学式为
(5)单质F与水反应的离子方程式为
您最近一年使用:0次
2017-02-28更新
|
558次组卷
|
3卷引用:【校级联考】天津市静海区2019届高三上学期12月四校联考化学试题
名校
解题方法
7 . W、X、Y、Z、M为原子序数依次增大的短周期主族元素,其中仅有X、Y、Z相邻,且为同周期元素,五种元素可组成抗生素氧哌嗪青霉素中间体,其结构如图所示,下列说法正确的是

A.W与X、Y、Z、M形成的简单化合物的熔点: |
B.X、Y、M元素形成的氧化物对应的水化物的酸性: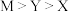 |
C.Y、Z、M元素对应的简单阴离子的半径: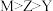 |
| D.W与X、Y、Z、M元素均能形成18电子的化合物 |
您最近一年使用:0次
2024-05-16更新
|
33次组卷
|
2卷引用:重庆市荣昌永荣中学校2024届高三下学期模拟预测化学试题2
名校
8 . 原子序数依次增大的X、Y、Z、M、W为五种短周期元素。已知Y与Z、M与W分别同周期,X与M同主族;X、Z、M的质子数之和等于Y、W的质子数之和;X与Z、M与Z都可以分别形成A2B、A2B2型的化合物;X与Y形成的气态化合物在标准状况下的密度为0.76g·L-1;Y、M、W的最高价氧化物的水化物。两两间都能发生反应。下列说法不正确的是
| A.由X、M与Z形成的化合物X2Z2和M2Z2中所含的化学键类型相同 |
| B.含有W阳离子的某种盐,可用作净水剂 |
| C.M的单质可保存于煤油中 |
| D.由X、Y、Z 种元素形成的某种化合物的水溶液,可能呈碱性或酸性 |
您最近一年使用:0次
2016-09-01更新
|
272次组卷
|
3卷引用:2015届山东省济宁市高三第一次模拟考试理综化学试卷
9-10高三·湖北黄冈·阶段练习
解题方法
9 . A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如右图转化关系:
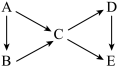
(1)若右图中B、C均为氧化物、D、E均为盐,则A可能是(填编号)__________ 。
①Na ②N2 ③C ④S
(2)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C>D>E,B可做生氧剂,则B中含有的化学键类型为__________________ ;A转化成C的离子方程式为:________________________________ ,D转化成E的离子方程式为_______________________________________ 。
(3)若常温下B、C、D均为气体,且B气体能使湿润的红色石蕊试纸变蓝。
①在工业上生产B气体时为了加快反应速率应选择的条件是______________ ,其中能提高反应物的转化率的条件是___________ 。
②C、D是汽车尾气中的有害成分,用NaOH溶液吸收可消除污染,反应的化学方程式为__________________________________ 。

(1)若右图中B、C均为氧化物、D、E均为盐,则A可能是(填编号)
①Na ②N2 ③C ④S
(2)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C>D>E,B可做生氧剂,则B中含有的化学键类型为
(3)若常温下B、C、D均为气体,且B气体能使湿润的红色石蕊试纸变蓝。
①在工业上生产B气体时为了加快反应速率应选择的条件是
②C、D是汽车尾气中的有害成分,用NaOH溶液吸收可消除污染,反应的化学方程式为
您最近一年使用:0次
名校
10 . 短周期元素X、Y、Z、W原子序数依次增大。X的质子数与电子层数相同,Y、Z同周期且相邻,Z的最外层电子数是其内层电子数的3倍,元素W在地壳中的含量仅次于氧。下列说法正确的是
| A.原子半径:r(W)>r(Y)>r(Z)>r(X) |
| B.X、Y、Z三种元素形成的化合物中只有共价键 |
| C.最高价氧化物对应水化物的酸性:W>Y |
| D.气态简单氢化物的热稳定性:Y>Z |
您最近一年使用:0次
2016-12-09更新
|
239次组卷
|
2卷引用:2015届山东省淄博市高三二模理综化学试卷



