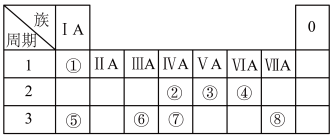
(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)用电子式表示②的最高价氧化物的形成过程为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为
②铯单质与H2O反应的化学反应方程式为
③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
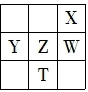
| A.X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 |
| B.Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 |
| C.YX2的熔点低于WX3 |
| D.根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
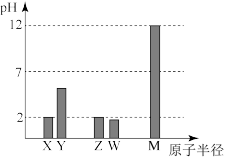
| A.M元素一定位于第三周期第IA族 |
| B.X与Z的简单气态氢化物反应生成的化合物中含有离子键和极性键 |
| C.Z、W的气态氢化物的热稳定性:Z<W |
| D.W的氧化物可能具有还原性、氧化性 |
| 元素 | 特征 | 元素 | 特征 |
| A | 常见金属,其最高价氧化物对应的水化物可以溶于强碱 | D | 在地壳中含量最多 |
| B | 常见化肥的主要元素,单质常温下呈气态 | E | 单质为黄绿色有毒气体 |
| C | 在短周期主族元素中,原子半径最大 | F | 原子的核外电子只有1个 |
(2)A、C、D对应的简单离子的半径由大到小的排序是
(3)B的最简单氢化物的稳定性
 的稳定性。
的稳定性。(4)
 溶液中存在的化学键类型有
溶液中存在的化学键类型有 溶液反应的离子方程式为
溶液反应的离子方程式为(5)用电子式表示化合物
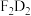 的形成过程
的形成过程(6)已知
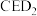 是一种强氧化性漂白剂,它在碱性环境中稳定存在。在碱性条件下,
是一种强氧化性漂白剂,它在碱性环境中稳定存在。在碱性条件下,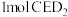 和
和 恰好完全反应,该反应的离子方程式为
恰好完全反应,该反应的离子方程式为 的外围电子排布式为
的外围电子排布式为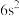 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是( )
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是( )A. 具有还原性 具有还原性 |
| B.X的最高价氧化物具有强氧化性 |
| C.该元素是第ⅥA族元素 |
| D.X的常见化合价有+2、+4 |
(1)E的离子结构示意图:
(2)D单质与C单质反应产物可能是
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为
(4)DA化合物与A2C化合物反应可以得到A的单质,则化学方程式
(5)E的最高价氧化物对应水合物的浓溶液加入G单质,下列说法不正确的是
A.常温下两者不发生反应
B.常温下无现象,G单质不溶解
C.受热能发生反应,开始放出氢气
D.受热能发生反应,开始放出是SO2
| A.A与B形成的化合物中只含离子键 |
| B.A的气态氢化物的沸点一定高于D的气态氢化物的沸点 |
| C.若A与C的原子序数相差5,则二者形成化合物的化学式一定为C2A3 |
| D.相同条件下,B的最高价氧化物的水化物的碱性比C的最高价氧化物的水化物的碱性强 |
8 . A、B、C、D、E、F、G为原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性;G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:
(2)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(3)E的最高价氧化物对应水合物的浓溶液加入G单质,下列说法正确的是
A.常温下两者不发生反应
B.常温下无现象,G单质不溶解
C.受热能发生反应,开始放出氢气
D.受热能发生反应,开始放出是SO2
(4)用电子式写出A2C的形成过程
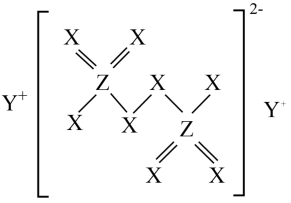
| A.元素的非金属性:W>X>Z | B.X、Z的简单氢化物的沸点:Z>X |
| C.X、Y形成的两种化合物只含离子键 | D.Y、Z形成的化合物的水溶液显碱性 |
| A.X与Y只能形成一种化合物 |
| B.最高价氧化物对应水化物的碱性:Y>Z |
| C.元素X、Y、Z的简单离子具有相同电子层结构,且离子半径依次增大 |
| D.单质的氧化性:X<M |



