1 . ①、②、③、④是原子序数依次增大的四种短周期元素,①周期表中原子半径最小的元素,②的最外层电子数比次外层多1,③的第一电离能比左右相邻两元素的都要大,④是周期表中电负性最大的元素。元素①和③可形成一种三角锥形的分子A,元素②和④可形成一种平面三角形的分子B。
(1)元素②的基态原子的电子排布式为___________ 。
(2)元素③的价电子的轨道表示式为___________ 。
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:___________ (用元素符号表示)。
(4)分子A的电子式为___________ ,分子B的中心原子杂化方式为___________ ;A与B之间能否形成配位键?若能,用化学用语表示出两者之间的配位键;若不能,说明理由:___________ 。
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:___________ 。
(1)元素②的基态原子的电子排布式为
(2)元素③的价电子的轨道表示式为
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:
(4)分子A的电子式为
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:
您最近一年使用:0次
名校
解题方法
2 . 安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为___________ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为___________ ,能量最高的电子为___________ 层上的电子。反应中涉及的主族元素的简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有___________ 个氮原子(保留三个有效数字);已知获得上述N2需要NaN3130g,反应生成N2的产率是___________ %(产率= ×100%)
×100%)
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有
 ×100%)
×100%)
您最近一年使用:0次
3 . 写出下列概念的含义:
(1)反应的热效应:_______________________________ 。
(2)泡利不相容原理:______________________________ 。
(1)反应的热效应:
(2)泡利不相容原理:
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)原子核外电子是分层排布的,当N层为最外层时,最多可容纳电子数是______ ;
(2)某元素原子,L层上的电子数是M层电子数的两倍,中子数为15,可表示相关信息的原子符号为______ ;
(3)原子核外电子排布可以用原子结构示意图简明的表示,如:
a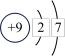 b
b c
c d
d
微粒d在化学反应中容易______ (选填“得到”或“失去”)电子,达到______ 结构;这些微粒中的稀有气体元素原子的电子式是______ ; 和
和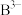 两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则
两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则 的结构示意图为
的结构示意图为______ ,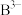 的电子式为
的电子式为______ 。
(1)原子核外电子是分层排布的,当N层为最外层时,最多可容纳电子数是
(2)某元素原子,L层上的电子数是M层电子数的两倍,中子数为15,可表示相关信息的原子符号为
(3)原子核外电子排布可以用原子结构示意图简明的表示,如:
a
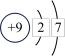 b
b c
c d
d
微粒d在化学反应中容易
 和
和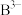 两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则
两种离子的核外电子排布与这种稀有气体原子的核外电子排布相同,则 的结构示意图为
的结构示意图为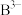 的电子式为
的电子式为
您最近一年使用:0次
名校
5 . A、B、C为电子层数小于或等于3的元素,A元素原子M层电子数为K层电子数的 ,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的
,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的 。由此推断三种元素名称分别是A
。由此推断三种元素名称分别是A________ 、B_______ 、C________ 。写出A的阳离子的结构示意图________ 。写出由A和B两种元素所形成的化合物的电离方程式________ 。
 ,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的
,B元素原子M层电子数为次外层与最内层电子数之差,C元素原子L层达稳定结构所需电子数为该层电子数的 。由此推断三种元素名称分别是A
。由此推断三种元素名称分别是A
您最近一年使用:0次
名校
解题方法
6 . 基态24Cr的核外电子排布式为___________ ;基态35Br-的核外电子排布式为___________ ,原子结构示意图为___________ ;基态Fe原子结构示意图为___________ 。
您最近一年使用:0次
7 . 为什么第一个电子层最多容纳2个电子?第二层最多只能容纳8个电子?第三、四、五电子层最多能容纳的电子数分别是多少?_________
您最近一年使用:0次
8 . 最外层电子数目的变化
除第1周期外,每隔一定数目的元素,元素原子的最外层电子数重复出现从_____ 逐渐增加到_____ 的周期性变化。
除第1周期外,每隔一定数目的元素,元素原子的最外层电子数重复出现从
您最近一年使用:0次
9 . 电子在原子核外的区域内作高速运动,根据电子的能量高低划分为电子层,在各电子层上电子的排布也遵循着一定的规律。一些粒子的结构都可用下面的示意图来表示,且0<y≤8。
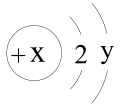
(1)若x=12时对应的元素为A,则y =_______ ;
(2)若某粒子带一个单位正电荷,则该粒子的化学符号为_______ ;
(3)若x=10,与其电子数相同的的微粒有(各举1个例子,可以是多核微粒):正离子_______ ,负离子_______ ,分子_______ 。
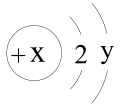
(1)若x=12时对应的元素为A,则y =
(2)若某粒子带一个单位正电荷,则该粒子的化学符号为
(3)若x=10,与其电子数相同的的微粒有(各举1个例子,可以是多核微粒):正离子
您最近一年使用:0次



