1 . 甘蔗含糖量十分丰富,其中蔗糖(结构如图所示)、葡萄糖及果糖的含量可达12%,它们极易被人体吸收利用。下列说法正确的是
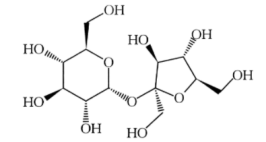
| A.蔗糖不能使酸性高锰酸钾溶液褪色 |
| B.葡萄糖和果糖互为同分异构体 |
| C.蔗糖分子中碳元素含量最高 |
| D.基态氢原子中电子云轮廓图形状为哑铃形 |
您最近半年使用:0次
名校
解题方法
2 . 研究发现,在饮用水、食物或牙膏中添加氟化物,能起到预防龋齿的作用。这是因为氟离子能与羟基磷灰石发生反应,生成氟磷灰石[ ],下列说法错误的是
],下列说法错误的是
 ],下列说法错误的是
],下列说法错误的是A. 的空间结构:正四面体形 的空间结构:正四面体形 |
| B.基态O原子核外电子的运动状态有8种 |
C. 比 比 稳定,是因为 稳定,是因为 分子间存在氢键 分子间存在氢键 |
D.基态 原子中,电子占据最高能级的电子云轮廓图为球形 原子中,电子占据最高能级的电子云轮廓图为球形 |
您最近半年使用:0次
2024-04-26更新
|
88次组卷
|
3卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高二下学期入学考试化学试题
3 . 以下关于铁元素的相关说法正确的是
A. 的电子有23种空间运动状态 的电子有23种空间运动状态 |
B.Fe的价电子轨道表示式为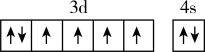 |
| C.Fe的26个电子在原子轨道中做圆周运动 |
| D.铁与盐酸反应时失去的都是3d电子 |
您最近半年使用:0次
名校
解题方法
4 . 下列化学用语表达正确的是
A.NH3的VSEPR模型: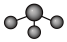 |
| B.As原子的简化电子排布式:[Ar]4s24p3 |
C.p-p σ键电子云轮廓图: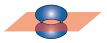 |
D.基态Mn原子价电子轨道表示式: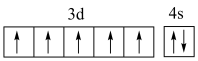 |
您最近半年使用:0次
2024-02-01更新
|
515次组卷
|
3卷引用:湖南省长沙麓山国际实验学校2023-2024学年高二下学期4月份学情检测化学试卷
5 . 根据有关知识,回答下列问题。
(1)符号 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。
(2)铝原子核外电子云有__________ 种不同的伸展方向,有__________ 种不同运动状态的电子。
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是__________ (填元素符号,下同),电负性最大的元素是__________ 。
(4)Be的第一电离能大于B的第一电离能,这是因为__________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:__________ 。
(6)锰元素位于第四周期第ⅦB族,请写出基础 的价层电子排布式
的价层电子排布式__________ 。
(1)符号
 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第3个电子层 轨道有三个伸展方向 轨道有三个伸展方向 |
C. 电子云有3个伸展方向 电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是
(4)Be的第一电离能大于B的第一电离能,这是因为
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:(6)锰元素位于第四周期第ⅦB族,请写出基础
 的价层电子排布式
的价层电子排布式
您最近半年使用:0次
6 . 下列有关化学用语表示错误的是
A.氯气的共价键电子云轮廓图: |
| B.二氧化硅的分子式为SiO2 |
C.N2H4的电子式: |
D.基态氧原子电子轨道表示式为: |
您最近半年使用:0次
2024-01-11更新
|
942次组卷
|
3卷引用:湖南省常德市第一中学2023-2024学年高二上学期期末考试化学试题
7 . 硒化锌是一种重要的半导体材料,图甲为其晶胞结构,图乙为晶胞的俯视图。已知a点的坐标(0,0,0),b点的坐标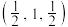 。下列说法正确的是
。下列说法正确的是

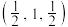 。下列说法正确的是
。下列说法正确的是
A. 的配位数为8 的配位数为8 | B.基态Se核外有34种不同空间运动状态的电子 |
C.晶胞中d点原子分数坐标为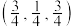 | D.若 换为 换为 ,则晶胞棱长保持不变 ,则晶胞棱长保持不变 |
您最近半年使用:0次
2023-12-26更新
|
587次组卷
|
3卷引用:湖南省衡阳市第八中学2023-2024学年高三上学期1月月考化学
湖南省衡阳市第八中学2023-2024学年高三上学期1月月考化学湖北省武汉市华中师范大学第一附属中学2023-2024学年高三上学期11月期中考试化学试题(已下线)微题型02 晶体结构及相关计算-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
8 . 按要求回答下列问题。
(1)基态硅原子核外电子的运动状态有___________ 种,价层电子轨道表示式为___________ 。
(2)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
(3)①钴位于元素周期表中___________ (填“s”、“p”、“d”或“ds”)区,与钴位于同一周期且含有相同未成对电子数的元素有___________ 种。
②钴元素可形成配合物[Co(NH3)6]Cl3,1mol该配合物含有σ键的数目为___________ 。该配合物中存在的化学键有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.氢键 E.配位键
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的 、
、 可知,气态Mn2+再失去1个电子比气态
可知,气态Mn2+再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(5)第四周期主族元素中,第一电离能介于Ga、As之间的元素有___________ 种。
(6)氯化铝熔点为194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成为Al2Cl6,其结构式为___________ (已知Al2Cl6中原子均满足8e-稳定结构)。
(1)基态硅原子核外电子的运动状态有
(2)下列氟元素的不同微粒,用光谱仪可捕捉到发射光谱的是___________。
| A.1s22s22p43s1 | B.1s22s22p43d2 | C.1s22s22p5 | D.1s22s22p6 |
②钴元素可形成配合物[Co(NH3)6]Cl3,1mol该配合物含有σ键的数目为
A.离子键 B.极性键 C.非极性键 D.氢键 E.配位键
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/ | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 、
、 可知,气态Mn2+再失去1个电子比气态
可知,气态Mn2+再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是(5)第四周期主族元素中,第一电离能介于Ga、As之间的元素有
(6)氯化铝熔点为194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成为Al2Cl6,其结构式为
您最近半年使用:0次
名校
解题方法
9 . 下列说法正确的是
A.基态Be原子最外层电子的电子云轮廓图为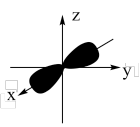 |
| B.基态Br原子的简化电子排布式为[Ar]4s24p5 |
| C.基态铝原子核外有5种能量不同的电子 |
| D.白磷分子空间构型为正四面体形,键角为109°28′ |
您最近半年使用:0次
10 . (CH3NH3)PbI3的晶胞结构如图所示,其中B代表Pb2+下列说法不正确的是
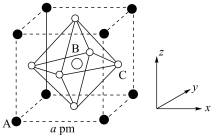

| A.A代表I— |
| B.(CH3NH3)PbI3中涉及的短周期元素的电负性由大到小的顺序为N>C>H |
| C.基态Ⅰ原子核外电子占据最高能级的电子云轮廓图为哑铃状 |
D.已知(CH3NH3)PbI3的摩尔质量为 ,NA为阿伏加德罗常数,则该晶体密度为 ,NA为阿伏加德罗常数,则该晶体密度为 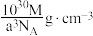 |
您最近半年使用:0次



