1 . 1869年,俄国化学家门捷列夫提出了元素周期律,并在此基础上发表了第一张元素周期表。为了纪念元素周期表诞生150年,联合国将2019年定为“国际化学元素周期表年”,并认为元素周期表是“科学共同的语言”。 、Ⅱ
、Ⅱ 元素属于
元素属于___________ 区。
②2017年5月9日我国发布了113号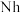 、115号
、115号 、117号
、117号 、118号
、118号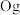 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是___________ (填字母序号)。
a.113号元素在周期表中的位置是第七周期Ⅴ 族
族
b.117号元素 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体
c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:
(2)认识原子结构与元素周期表的关系:见表中元素 的信息,其中“
的信息,其中“ ”称为该元素原子的
”称为该元素原子的___________ ,该元素 能层上具有
能层上具有___________ 种不同运动状态的电子。
(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
②前四周期同族元素的某种性质 随核电荷数的变化趋势如图所示,则下列说法正确的是
随核电荷数的变化趋势如图所示,则下列说法正确的是___________ (填字母)。 、
、 、
、 表示氧族元素,则
表示氧族元素,则 表示对应氢化物的稳定性
表示对应氢化物的稳定性
B.若 、
、 、
、 表示卤族元素,则
表示卤族元素,则 表示对应简单离子的还原性
表示对应简单离子的还原性
C.若 、
、 、
、 表示第Ⅰ
表示第Ⅰ 族元素,则
族元素,则 表示对应离子的氧化性
表示对应离子的氧化性
D.若 、
、 、
、 表示第Ⅱ
表示第Ⅱ 族元素,则
族元素,则 表示最高价氧化物对应水化物的碱性
表示最高价氧化物对应水化物的碱性

 、Ⅱ
、Ⅱ 元素属于
元素属于②2017年5月9日我国发布了113号
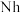 、115号
、115号 、117号
、117号 、118号
、118号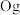 四种元素,则下列说法正确的是
四种元素,则下列说法正确的是a.113号元素在周期表中的位置是第七周期Ⅴ
 族
族b.117号元素
 位于金属与非金属分界线上,属于准金属,可能是半导体
位于金属与非金属分界线上,属于准金属,可能是半导体c.这四种元素都是主族元素
d.最高价氧化物的水化物的碱性:

(2)认识原子结构与元素周期表的关系:见表中元素
 的信息,其中“
的信息,其中“ ”称为该元素原子的
”称为该元素原子的 能层上具有
能层上具有(3)认识元素周期律及其应用:
①第三周期元素的第一电离能:

 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是②前四周期同族元素的某种性质
 随核电荷数的变化趋势如图所示,则下列说法正确的是
随核电荷数的变化趋势如图所示,则下列说法正确的是
 、
、 、
、 表示氧族元素,则
表示氧族元素,则 表示对应氢化物的稳定性
表示对应氢化物的稳定性B.若
 、
、 、
、 表示卤族元素,则
表示卤族元素,则 表示对应简单离子的还原性
表示对应简单离子的还原性C.若
 、
、 、
、 表示第Ⅰ
表示第Ⅰ 族元素,则
族元素,则 表示对应离子的氧化性
表示对应离子的氧化性D.若
 、
、 、
、 表示第Ⅱ
表示第Ⅱ 族元素,则
族元素,则 表示最高价氧化物对应水化物的碱性
表示最高价氧化物对应水化物的碱性
您最近半年使用:0次
名校
解题方法
2 . 铊的相关信息卡片如图所示:
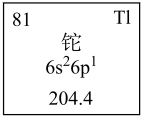
(1)铊的原子序数为81,铊在元素周期表中位置_______ 。
(2)根据所学知识,下列推断正确的是_______ 。
(3)铊(Tl)是某超导材料的组成元素之一。Tl3+与Ag在酸性介质中发生反应:Tl3++2Ag=Tl++2Ag+。下列推断正确的是_______ 。
(4)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。表中列出了第三周期的几种元素的部分性质:请按要求回答下列问题:
①写出基态a原子的价层电子轨道表示式:_______ 。
②预测X值的范围:_______ <X<_______ 。
③表中五种元素的第一电离能由大到小排第二的是_______ (写元素符号)。
(5)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
①基态Ti原子的核外电子排布式为:_______ 。
②基态Fe3+、Fe2+离子中未成对的电子数之比为_______ 。
③元素Li为_______ 区元素。

(1)铊的原子序数为81,铊在元素周期表中位置
(2)根据所学知识,下列推断正确的是
| A.单质的还原性:Tl>Al | B.原子半径:Al>Tl |
| C.碱性:Al(OH)3>Tl(OH)3 | D.氧化性:Tl3+>Al3+ |
| A.Tl+最外层有1个电子 | B.Tl能形成+3价和+1价的化合物 |
C.Tl3+的氧化性比 弱 弱 | D.Tl+的还原性比Ag强 |
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
①写出基态a原子的价层电子轨道表示式:
②预测X值的范围:
③表中五种元素的第一电离能由大到小排第二的是
(5)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
①基态Ti原子的核外电子排布式为:
②基态Fe3+、Fe2+离子中未成对的电子数之比为
③元素Li为
您最近半年使用:0次
3 . I.表中列出了第三周期的几种元素的部分性质:
请按要求回答下列问题:
(1)写出基态a原子的价层电子排布式:____ 。
(2)表中元素原子半径最大的是(写元素符号)_____ 。
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)_____ 。
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为_____ 。
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)____ 。
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为____ 。
(7)下列说法合理的是____ 。
a.SeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)写出基态a原子的价层电子排布式:
(2)表中元素原子半径最大的是(写元素符号)
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为
(7)下列说法合理的是
a.SeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
您最近半年使用:0次
名校
解题方法
4 . X、Y为第三周期元素,Y最高正价与最低负价的代数和为6,二者形成的一种化合物能以 的形式存在。下列说法错误的是
的形式存在。下列说法错误的是
 的形式存在。下列说法错误的是
的形式存在。下列说法错误的是A.最高价氧化物水化物的酸性: |
B.简单氢化物的还原性: |
| C.同周期元素形成的单质中Y氧化性最强 |
| D.同周期中第一电离能小于X的元素有4种 |
您最近半年使用:0次
2022-05-18更新
|
158次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
5 . 含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有 NO 等氮氧化物的尾气,反应方程式如下:NaClO + NO + H2O — NaCl + HNO3 (未配平)。
(1)氯在元素周期表中的位置是_______ ,其所在主族的元素中,最高价氧化物对应的水化物酸性最强的是_______ (填化学式)。其所在周期的元素中,第一电离能最大的是______ (填化学式)。
(2)配平上述反应方程式_______ 。每有 0.3mol 电子发生转移,可消耗标准状况下 NO 气体的体积约为______ L。
(3)NaClO 溶液中存在如下关系:c(OH-)_____ c(HClO)(填“>”、“=”、或“<”)。
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。
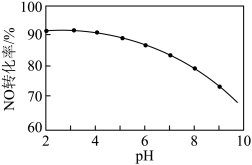
(4)NaClO 溶液的初始pH 越大,NO 的转化率越________ (填“高”或“低”),其原因是_________ 。
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
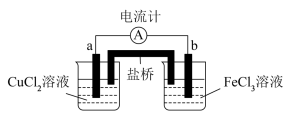
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式________ ;盐桥在原电池中所起的作用(任意写出一条)__________ 。
(1)氯在元素周期表中的位置是
(2)配平上述反应方程式
(3)NaClO 溶液中存在如下关系:c(OH-)
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。

(4)NaClO 溶液的初始pH 越大,NO 的转化率越
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
| 滴加 KI 溶液 | 再滴加 CCl4,振荡、静置 | 结论 | |
| A 试管 | 溶液变为棕黄色 | 溶液分层,下层显 | 氧化性强弱:(填“>”或“<”) KClO3 |
| B 试管 | 无现象 | 溶液分层,均无色 |
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式

您最近半年使用:0次
解题方法
6 . 硒(34Se)是人和动物体中一种必需的微量元素,存在于地球所有环境介质中,其同位素可有效示踪硒生物地球化学循环过程及其来源,下列说法不正确 的是
| A.Se位于周期表中第四周期第VIA族 |
| B.可用质谱法区分Se的两种同位素78Se和80Se |
| C.第一电离能:34Se>33As |
| D.SeO2既具有氧化性又具有还原性 |
您最近半年使用:0次
解题方法
7 . 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是
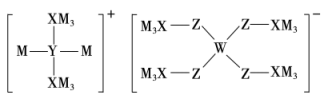
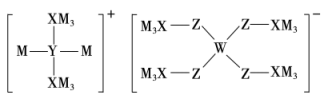
| A.第一电离能:W<X<Z<Y | B.简单氢化物的还原性:Z>Y>X |
| C.阴、阳离子中均有配位键 | D.同周期元素形成的单质中Z氧化性最强 |
您最近半年使用:0次
名校
解题方法
8 . 碳、氧、氮、镁、铬、铁、铜是几种重要的元素,请回答下列问题:
(1) 在第二周期的元素中,第一电离能介于B 与N之间的元素有_________ 种。
(2)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是____________________ 。
(3)Fe 与CO能形成一种重要的催化剂Fe(CO)5,该分子中σ键与π键个数比为______________ 。请写出一个与CO互为等电子体的离子:____________________ 。
(4)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+。
①K2Cr2O7具有很强的氧化性,能直接将CH3CH2OH 氧化成CH3COOH,试写出基态铬原子的价层电子排布式:_______________ ;CH3COOH 分子中碳原子的杂化类型为_________________ ;乙醇和丙烷相对分子质量相近,但乙醇的熔、沸点比丙烷高很多,试解释其主要原因:____________________________________ 。
②该配离子[Cr(H2O)3(NH3)3]3+中,中心离子的配位数为_______ ,NH3的VSEPR模型为_______ 。
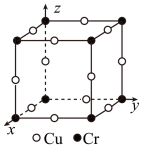
③图为Cu-Cr形成的一种合金的晶胞(假设晶体中原子之间彼此相切),单独属于该晶胞的Cu原子共有三个,其原子坐标可分别表示为:( ,0,0)、 (0,
,0,0)、 (0, ,0)、
,0)、_______ ;已知晶胞中Cr 和Cu原子间的最近距离为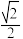 a pm,则该晶体的密度为
a pm,则该晶体的密度为_______ g·cm-3 (用含a的代数式表示,设N A为阿伏伽德罗常数的值)。
(1) 在第二周期的元素中,第一电离能介于B 与N之间的元素有
(2)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是
(3)Fe 与CO能形成一种重要的催化剂Fe(CO)5,该分子中σ键与π键个数比为
(4)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+。
①K2Cr2O7具有很强的氧化性,能直接将CH3CH2OH 氧化成CH3COOH,试写出基态铬原子的价层电子排布式:
②该配离子[Cr(H2O)3(NH3)3]3+中,中心离子的配位数为
③图为Cu-Cr形成的一种合金的晶胞(假设晶体中原子之间彼此相切),单独属于该晶胞的Cu原子共有三个,其原子坐标可分别表示为:(
 ,0,0)、 (0,
,0,0)、 (0, ,0)、
,0)、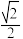 a pm,则该晶体的密度为
a pm,则该晶体的密度为
您最近半年使用:0次
9 . 我国研究人员开发出的铝/镁/铝层压板,质量轻、耐腐蚀。下说法不正确 的是
| A.原子半径:Mg > Al | B.第一电离能:Mg < Al |
| C.碱性:Mg(OH)2 > Al(OH)3 | D.氧化性:Mg2+ < Al3+ |
您最近半年使用:0次
解题方法
10 . 下列有关微粒性质的排列顺序,错误的是
| A.原子半径:Ba>Ca>Ge>N | B.第一电离能:Br>As>Se>Ga |
| C.还原性:As3->S2->Cl->F- | D.氧化性:Li+<Na+<K+<Ca2+ |
您最近半年使用:0次



