名校
1 . Fe、HCN与K2CO3在一定条件下发生如下反应:Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,下列说法正确的是
| A.此化学方程式中涉及的第二周期元素的电负性大小的顺序为O<N<C |
B.配合物K4Fe(CN)6的中心离子的价电子排布图为 ,该中心离子的配位数是10 ,该中心离子的配位数是10 |
| C.1mol[Fe(CN)6]4-分子中含有σ键的数目为12×6.02×1023 |
| D.K2CO3中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 |
您最近一年使用:0次
2 . 短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是
| A.X能与多种元素形成共价键 | B.简单氢化物沸点: |
C.第一电离能: | D.电负性: |
您最近一年使用:0次
2022-07-06更新
|
9295次组卷
|
28卷引用: 天津市静海区第一中学2023-2024学年高三上学期12月月考化学试题
天津市静海区第一中学2023-2024学年高三上学期12月月考化学试题(已下线)专题06 物质结构元素周期律-2022年高考真题模拟题分项汇编(已下线)2022年辽宁省高考真题化学试题(部分试题)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)吉林省长春外国语学校2021-2022学年高二下学期期末考试化学试题2022年辽宁高考真题化学试题(已下线)2022年辽宁省高考真题变式题(1-10)(已下线)第29讲 原子结构与性质(讲)-2023年高考化学一轮复习讲练测(新教材新高考)北京清华附中2022-2023学年高三上学期10月统练(三)化学试题(已下线)易错点13 原子结构与核外电子排布-备战2023年高考化学考试易错题(已下线)第36讲 原子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破吉林省长春市第五中学2022-2023学年高二上学期期末考试化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)河南省鹤壁市高中2022-2023学年高二下学期第一次段考化学试题(已下线)回归教材重难点12 原子、分子和晶体结构再归纳-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2022年辽宁高考真题化学试题变式题(选择题1-5)(已下线)题型9 元素“位—构-性”关系的综合应用-高考必备50个题型天津市和平区2022-2023学年高二下学期期末质量调查化学试题(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)天津市第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)江西省宜春市宜丰中学2023-2024学年高三上学期11月期中考试化学试题河北省遵化市第一中学2023-2024学年高二上学期月考2化学试题吉林省长春市第二实验中学2023-2024学年高二下学期开学考试化学试题天津市和平区2023-2024学年高三下学期第一次质量调查化学试卷内蒙古呼和浩特市剑桥中学2023-2024学年高二下学期3月月考化学试题
解题方法
3 . 短周期元素 、
、 、
、 、
、 、
、 在元素周期表中相对位置如图所示。请用
在元素周期表中相对位置如图所示。请用化学用语 回答下列问题:
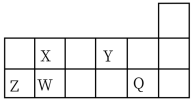
(1) 、
、 的离子半径由大到小的顺序为
的离子半径由大到小的顺序为_______ ; 、
、 、
、 元素的电负性最大的是
元素的电负性最大的是_______ 。
(2)下列说法正确的是_______
a. 和
和 都能溶于水生成对应的酸
都能溶于水生成对应的酸
b. 的含氧酸的酸性比
的含氧酸的酸性比 的含氧酸的酸性强
的含氧酸的酸性强
c. 的最简单气态氢化物的稳定性大于
的最简单气态氢化物的稳定性大于 的最简单气态氢化物的稳定性
的最简单气态氢化物的稳定性
d. 由 溶液分别滴入
溶液分别滴入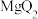 、
、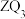 溶液中的反应现象可比较
溶液中的反应现象可比较 和
和 金属性的强弱
金属性的强弱
(3) 与
与 两元素的单质反应生成
两元素的单质反应生成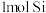 的最高价化合物,恢复至室温,放热
的最高价化合物,恢复至室温,放热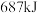 ,已知该化合物的熔、沸点分别为
,已知该化合物的熔、沸点分别为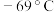 和
和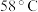 。写出该反应的热化学方程式
。写出该反应的热化学方程式_______ 。
(4)自来水厂用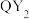 对饮用水进行消毒,处理后的水中要求
对饮用水进行消毒,处理后的水中要求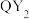 浓度在
浓度在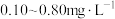 之间。碘量法可以检测水
之间。碘量法可以检测水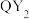 的浓度,步骤如下:
的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,再用 溶液调至中性,并加入淀粉溶液,溶液变蓝。
溶液调至中性,并加入淀粉溶液,溶液变蓝。
操作Ⅱ:再加入一定量的 溶液。(已知:
溶液。(已知: )
)
操作Ⅲ:然后再加硫酸调节水样 至1~3。
至1~3。
操作时,不同 环境中
环境中 元素粒子种类及化合价如图所示:
元素粒子种类及化合价如图所示:

①操作I中反应的离子方程式是_______ 。
②确定操作II完全反应的现象是_______ 。
③在操作III过程中,溶液又呈蓝色,反应的离子方程式是_______ 。
 、
、 、
、 、
、 、
、 在元素周期表中相对位置如图所示。请用
在元素周期表中相对位置如图所示。请用
(1)
 、
、 的离子半径由大到小的顺序为
的离子半径由大到小的顺序为 、
、 、
、 元素的电负性最大的是
元素的电负性最大的是(2)下列说法正确的是
a.
 和
和 都能溶于水生成对应的酸
都能溶于水生成对应的酸b.
 的含氧酸的酸性比
的含氧酸的酸性比 的含氧酸的酸性强
的含氧酸的酸性强c.
 的最简单气态氢化物的稳定性大于
的最简单气态氢化物的稳定性大于 的最简单气态氢化物的稳定性
的最简单气态氢化物的稳定性d. 由
 溶液分别滴入
溶液分别滴入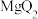 、
、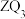 溶液中的反应现象可比较
溶液中的反应现象可比较 和
和 金属性的强弱
金属性的强弱(3)
 与
与 两元素的单质反应生成
两元素的单质反应生成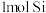 的最高价化合物,恢复至室温,放热
的最高价化合物,恢复至室温,放热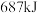 ,已知该化合物的熔、沸点分别为
,已知该化合物的熔、沸点分别为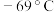 和
和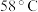 。写出该反应的热化学方程式
。写出该反应的热化学方程式(4)自来水厂用
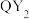 对饮用水进行消毒,处理后的水中要求
对饮用水进行消毒,处理后的水中要求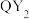 浓度在
浓度在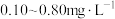 之间。碘量法可以检测水
之间。碘量法可以检测水 的浓度,步骤如下:
的浓度,步骤如下:操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,再用
 溶液调至中性,并加入淀粉溶液,溶液变蓝。
溶液调至中性,并加入淀粉溶液,溶液变蓝。操作Ⅱ:再加入一定量的
 溶液。(已知:
溶液。(已知: )
)操作Ⅲ:然后再加硫酸调节水样
 至1~3。
至1~3。操作时,不同
 环境中
环境中 元素粒子种类及化合价如图所示:
元素粒子种类及化合价如图所示:
①操作I中反应的离子方程式是
②确定操作II完全反应的现象是
③在操作III过程中,溶液又呈蓝色,反应的离子方程式是
您最近一年使用:0次
名校
解题方法
4 . 电负性越大,元素的非金属性越强,第一电离能也越大。(____)
您最近一年使用:0次
2021-12-03更新
|
649次组卷
|
7卷引用:天津市静海区第一中学2021-2022学年高三上学期12月调研考试化学试题
天津市静海区第一中学2021-2022学年高三上学期12月调研考试化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)人教2019选择性必修2第一章第二节 原子结构与元素的性质课后习题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第五章 物质结构与性质 元素周期律 第27讲 元素周期表和元素周期律1.3.2元素的电离能、电负性及其变化规律(课中)-鲁科版选择性必修2(已下线)考点41 原子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)



