解题方法
1 . 中国科学家团队成功合成了五氮阴离子盐 。五氮阴离子(
。五氮阴离子(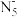 )为环状平面结构,是制备全氮类物质
)为环状平面结构,是制备全氮类物质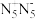 的中间体。
的中间体。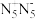 是新一代超高能含能材料下列说法正确的是
是新一代超高能含能材料下列说法正确的是
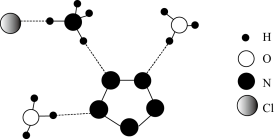
 。五氮阴离子(
。五氮阴离子(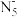 )为环状平面结构,是制备全氮类物质
)为环状平面结构,是制备全氮类物质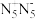 的中间体。
的中间体。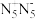 是新一代超高能含能材料下列说法正确的是
是新一代超高能含能材料下列说法正确的是
| A.阴阳离子之间作用力只存在离子键 | B.五氮阴离子盐中N、O两种元素均为sp3杂化 |
| C.电负性:N>O>H | D.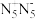 可以作炸药、推进剂 可以作炸药、推进剂 |
您最近一年使用:0次
名校
解题方法
2 . 运用物质结构与性质的相关知识,回答下列问题:
(1) 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是_______ 。基态 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有_____ 个伸展方向,原子轨道呈______ 形。
(2) 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为________ , 价电子轨道表示式为
价电子轨道表示式为________ 。
(3) 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
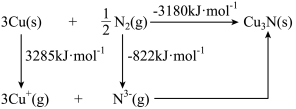
通过图中数据________ (填“能”或“不能”)计算出 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为________  。
。
(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。
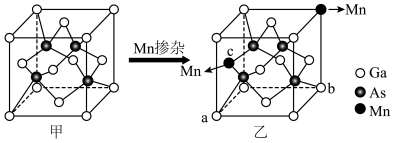
①GaAs晶胞中距离Ga原子最近As原子的个数为________ 。
②掺杂 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为________ (化为最简整数比)。
(1)
 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性
呈正电性 ,与
,与 原子相连的
原子相连的 呈负电性
呈负电性 电负性大小顺序是
电负性大小顺序是 原子中能量最高的电子所在的原子轨道的电子云在空间上有
原子中能量最高的电子所在的原子轨道的电子云在空间上有(2)
 的价层电子排布式为
的价层电子排布式为 在周期表中的位置为
在周期表中的位置为 价电子轨道表示式为
价电子轨道表示式为(3)
 是离子晶体,其晶格能可通过Born-Haber循环计算得到。
是离子晶体,其晶格能可通过Born-Haber循环计算得到。
通过图中数据
 原子的第一电离能,
原子的第一电离能, 的晶格能为
的晶格能为 。
。(4)GaAs的晶胞结构如图甲。将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料(图乙)。

①GaAs晶胞中距离Ga原子最近As原子的个数为
②掺杂
 之后,晶体中
之后,晶体中 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
解题方法
3 . 酞菁和酞菁钴可制得光动力学中的光敏剂,分子结构如图,其中酞菁分子中所有原子共平面,下列说法正确的是
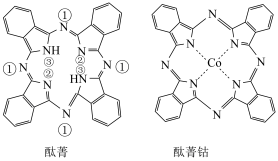
| A.酞菁钴中钴的化合价为+4 |
| B.直径为1.5×10–9 m的酞菁钴分子能透过半透膜 |
| C.酞菁钴中元素的电负性由大到小的顺序为N>C>H>Co |
| D.标注①②的N原子的杂化方式是sp2,③的N原子的杂化方式是sp3 |
您最近一年使用:0次
2024-03-13更新
|
483次组卷
|
2卷引用:福建省厦门第一中学2023-2024学年高三下学期2月第一次月考化学试卷
4 . 氮氧化物会导致光化学烟雾和酸雨,在 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
 的催化作用下,
的催化作用下, 可将NO还原为无污染的气体,反应历程如图,下列说法正确的是
可将NO还原为无污染的气体,反应历程如图,下列说法正确的是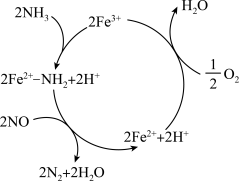
A.基态 的价层电子排布式为 的价层电子排布式为 |
| B.电负性:N>O>H>Fe |
| C.该过程中存在极性键和非极性键的断裂和形成 |
D.图中的总反应可表示为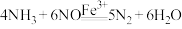 |
您最近一年使用:0次
2024-02-25更新
|
267次组卷
|
5卷引用:福建省福州第三中学2023-2024学年高三上学期第五次质量检测化学试题
名校
5 . 电负性用来描述不同元素的原子对键合电子吸引力的大小,是元素的一种基本性质。下表为一些元素的电负性(已知两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键):
下列说法不正确的是
| 元素 | Li | Be | B | C | N | F | Na | Mg | Al | Si | Cl | Ca |
| 电负性 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 4.0 | 0.9 | a | 1.5 | 1.8 | 3.0 | 1.0 |
| A.根据电负性变化规律,确定a的最小范围为1.0<a<1.5 |
| B.NF3中N-F键的极性比NCl3中N-Cl键的极性强 |
| C.AlCl3是一种可溶性盐,属于离子化合物 |
| D.可以通过测定化合物在熔融状态下是否导电鉴别Li3N与SiC |
您最近一年使用:0次
2024-02-22更新
|
192次组卷
|
4卷引用:福建省漳州市华安县第一中学2023-2024学年高二下学期3月月考化学试题
名校
6 . 叠氮化钠( )可用于汽车安全气囊的制造,
)可用于汽车安全气囊的制造, 与
与 发生反应可以生成
发生反应可以生成 ,反应方程式为
,反应方程式为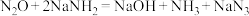 。下列有关说法错误的是
。下列有关说法错误的是
 )可用于汽车安全气囊的制造,
)可用于汽车安全气囊的制造, 与
与 发生反应可以生成
发生反应可以生成 ,反应方程式为
,反应方程式为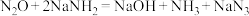 。下列有关说法错误的是
。下列有关说法错误的是A.键角: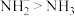 | B.电负性: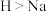 |
C. 溶液显碱性 溶液显碱性 | D.1 mol  中含2 mol σ键 中含2 mol σ键 |
您最近一年使用:0次
2024-02-01更新
|
447次组卷
|
3卷引用:福建省厦门第一中学2023-2024学年高二下学期第一次月考化学试题
解题方法
7 . 一种用作锂离子电池电解液的锂盐结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族元素,W原子的最外层电子数等于其电子总数的 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是
| A.原子半径:W>Z>Y>X |
| B.简单氢化物稳定性:Y>Z>X |
| C.电负性:Z>Y>X |
D.阴离子中所有原子最外层均达到 稳定结构 稳定结构 |
您最近一年使用:0次
名校
8 . 三氯甲硅烷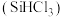 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为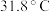 ,熔点为
,熔点为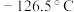 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
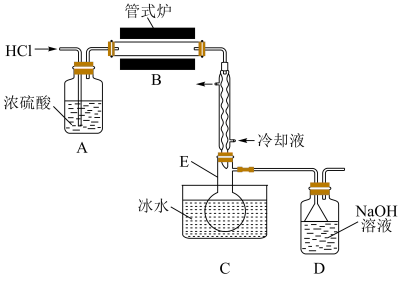
(1)制备 时进行操作:(i)……;(ii)将盛有硅粉的瓷舟置于管式炉中;(iii)通入
时进行操作:(i)……;(ii)将盛有硅粉的瓷舟置于管式炉中;(iii)通入 、一段时间后接通冷凝装置,加热开始反应。操作(i)为
、一段时间后接通冷凝装置,加热开始反应。操作(i)为___________ ;判断制备反应结束的实验现象是___________ 。图示装置存在的两处缺陷是___________ ,装置 的名称为
的名称为___________ 。
(2)已知电负性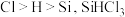 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为___________ 。
(3)采用如下方法测定溶有少量 的
的 纯度。
纯度。
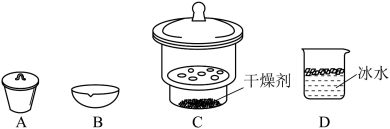
 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①___________ ,②___________ (填操作名称),③称量等操作,测得所得固体氧化物质量为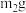 ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为___________ (填标号)。测得样品纯度为___________ (用含 的代数式表示)。
的代数式表示)。
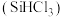 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为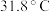 ,熔点为
,熔点为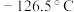 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
(1)制备
 时进行操作:(i)……;(ii)将盛有硅粉的瓷舟置于管式炉中;(iii)通入
时进行操作:(i)……;(ii)将盛有硅粉的瓷舟置于管式炉中;(iii)通入 、一段时间后接通冷凝装置,加热开始反应。操作(i)为
、一段时间后接通冷凝装置,加热开始反应。操作(i)为 的名称为
的名称为(2)已知电负性
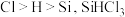 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为(3)采用如下方法测定溶有少量
 的
的 纯度。
纯度。 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①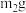 ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
9 . 2023年诺贝尔化学奖颁给合成量子点的三位科学家。量子点是一种重要的低维半导体材料,常由硅(Si)、磷(P)、硫(S)、硒(Se)等元素组成。下列说法正确的是
| A.原子半径:r(Si)>r(S)>r(Se) |
| B.电负性:χ(Se)>χ(S)>χ(Si) |
| C.第一电离能:I1(P)>I1(S)>I1(Si) |
| D.氢化物的稳定性:H2Se>H2S>PH3 |
您最近一年使用:0次
2024-01-20更新
|
222次组卷
|
4卷引用:福建省永春第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
10 . 2022年12月,首架国产大飞机C919正式交付,国之重器,世界瞩目。铼( )是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
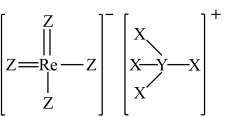
 )是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是
)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法正确的是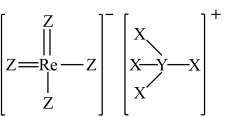
| A.电负性:Z>Y>Q>W |
| B.图中的阳离子存在三个共价键和一个配位键,四个键的性质不同 |
| C.熔点:W晶体小于W、Y形成的晶体 |
| D.Q的氧化物可以和氨水反应 |
您最近一年使用:0次



