1 . 回答下列问题:
(1) 中含有的
中含有的 键数目为
键数目为___________ , 键数目为
键数目为___________ 。
(2)已知CO和 与
与 结构相似,CO分子内
结构相似,CO分子内 键与
键与 键个数之比为
键个数之比为___________ 。 分子中
分子中 键与
键与 键数目之比为
键数目之比为___________ 。
(3)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
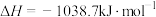 ,若该反应中有
,若该反应中有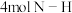 键断裂,则形成的
键断裂,则形成的 键有
键有___________ mol。
(4)Co基态原子核外电子排布式为___________ ; 的价电子轨道表示式为
的价电子轨道表示式为___________ ; 核外电子未成对电子数为
核外电子未成对电子数为___________ 。
(5) 、
、 、
、 、
、 分子中共价键的极性由强到弱的顺序是
分子中共价键的极性由强到弱的顺序是___________ 。
(1)
 中含有的
中含有的 键数目为
键数目为 键数目为
键数目为(2)已知CO和
 与
与 结构相似,CO分子内
结构相似,CO分子内 键与
键与 键个数之比为
键个数之比为 分子中
分子中 键与
键与 键数目之比为
键数目之比为(3)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
(氨基)取代形成的另一种氮的氢化物。肼可用作火箭燃料,燃烧时发生的反应:
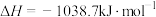 ,若该反应中有
,若该反应中有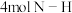 键断裂,则形成的
键断裂,则形成的 键有
键有(4)Co基态原子核外电子排布式为
 的价电子轨道表示式为
的价电子轨道表示式为 核外电子未成对电子数为
核外电子未成对电子数为(5)
 、
、 、
、 、
、 分子中共价键的极性由强到弱的顺序是
分子中共价键的极性由强到弱的顺序是
您最近一年使用:0次
2024-04-27更新
|
60次组卷
|
2卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
2 . 3-氨基-1-金刚烷醇可用于合成药物维格列汀(治疗2型糖尿病),其分子结构如下图所示。下列说法不正确的是

A.分子中O原子和N原子均为 杂化 杂化 | B.分子中的键角: |
C.电负性: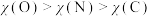 | D.第一电离能: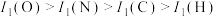 |
您最近一年使用:0次
2024-04-15更新
|
174次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高二下学期4月月考化学试题
解题方法
3 . 原子序数依次增大的五种元素的性质或结构信息如下表。
回答下列问题:
(1)T元素的原子结构示意图是___________ ,其三价阳离子的价电子轨道表示式为___________ 。
(2)五种元素中电负性最大与电负性最小的元素形成化合物的化学式为___________ ,基态W原子运动状态不同的电子数为___________ 。
(3)写出W元素与同周期相邻元素的第一电离能从大到小顺序:___________ ,Y元素与比其原子序数大8的元素,二者最高价氧化物对应的水化物酸性较强的是___________ (填化学式)。
(4)W的氢化物是有机化学反应的重要还原剂、火箭推进剂及氢燃料汽车中氢气的储存材料,遇水剧烈燃烧或爆炸,写出W的氢化物遇水释放出 的化学方程式:
的化学方程式:___________ 。
| 元素 | 原子结构和性质 |
| X | 基态原子s能级的电子总数是p能级电子总数的2倍 |
| Y | 其单质含有3对共用电子对 |
| Z | 大气中大量存在着两种单质,对人类生存都有重要意义 |
| W | 单质、最高价氧化物和最高价氧化物的水化物与盐酸或NaOH溶液都能反应 |
| T | 二价阳离子的电子排布式为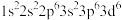 |
(1)T元素的原子结构示意图是
(2)五种元素中电负性最大与电负性最小的元素形成化合物的化学式为
(3)写出W元素与同周期相邻元素的第一电离能从大到小顺序:
(4)W的氢化物是有机化学反应的重要还原剂、火箭推进剂及氢燃料汽车中氢气的储存材料,遇水剧烈燃烧或爆炸,写出W的氢化物遇水释放出
 的化学方程式:
的化学方程式:
您最近一年使用:0次
解题方法
4 . 尿素[ ]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为
]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为 。回答下列问题:
。回答下列问题:
(1)上述反应所涉及的各元素中,原子半径最大的是___________ (填元素符号),其原子核外电子共占据___________ 个原子轨道。
(2)上述元素中有三种元素处于同周期,则:
①最高价氧化物对应水化物的酸性最强的是___________ (填化学式)。
②元素的第一电离能由大到小的顺序是___________ (填元素符号,下同)。
③元素的电负性由大到小的顺序是___________ 。
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:___________ 、___________ 。
 ]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为
]是一种重要的工业原料,在160℃下分解生成异氰酸和氨气,化学方程式为 。回答下列问题:
。回答下列问题:(1)上述反应所涉及的各元素中,原子半径最大的是
(2)上述元素中有三种元素处于同周期,则:
①最高价氧化物对应水化物的酸性最强的是
②元素的第一电离能由大到小的顺序是
③元素的电负性由大到小的顺序是
(3)氰酸有两种结构,一种分子内含有三键,称为氰酸,另一种分子内不含三键,称为异氰酸,且两种结构中所有原子最外层均已达到稳定结构,分子中也不含环状结构。写出氰酸和异氰酸的结构式:
您最近一年使用:0次
5 . 次氟酸(又名氟氧酸)是一种强氧化剂,可用被氮气稀释的氟气在细冰上缓慢通过制得,发生反应: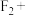
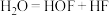 。下列关于次氟酸的说法正确的是
。下列关于次氟酸的说法正确的是
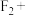
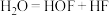 。下列关于次氟酸的说法正确的是
。下列关于次氟酸的说法正确的是| A.氟原子半径大于氧原子 | B.HOF分子中F为+1价 |
| C.第一电离能和电负性,F都大于O | D.次氟酸的强氧化性是F元素表现出来的 |
您最近一年使用:0次
名校
6 . 下列关于元素周期表、原子结构或元素性质的说法中错误的是
| A.共价化合物中,电负性大的成键元素表现为负价 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.目前的元素周期表共有7个周期,7个主族,8个副族,1个0族 |
| D.主族元素的价电子即最外层电子,过渡元素的价电子还包括次外层甚至倒数第三层电子 |
您最近一年使用:0次
名校
7 . 如表为元素周期表的一部分,其中的编号代表对应的不同元素。
请回答下列问题:
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为___________ 。
(2)基态③原子中电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形。
(3)写出②的氧化物与NaOH溶液反应的化学方程式:___________ 。
(4)元素④⑤⑥的电负性:___________>___________>___________。(填元素符号)___________
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式___________ 。
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素的名称是___________ 。
(7)⑨基态原子的简化电子排布式为___________ ,在周期表中的位置___________ 。
(8)⑩基态原子的价层电子轨道表示式为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为
(2)基态③原子中电子占据最高能级的符号是
(3)写出②的氧化物与NaOH溶液反应的化学方程式:
(4)元素④⑤⑥的电负性:___________>___________>___________。(填元素符号)
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素的名称是
| 元素 | 电离能(kJ•mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
(8)⑩基态原子的价层电子轨道表示式为
您最近一年使用:0次
名校
8 . 高压发电系统常用SF6作为绝缘气体,该气体分子呈正八面体结构(如图所示)。下列有关SF6的说法错误的是
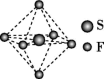

| A.是非极性分子 |
| B.键角∠FSF都等于90° |
| C.S与F之间共用电子对偏向F |
| D.基态硫原子的电子排布式为1s22s22p63s23p4 |
您最近一年使用:0次
名校
9 . 分子结构修饰是指不改变分子的主体骨架,保持分子的基本结构不变,仅改变分子结构中的某些基团而得到新分子的过程,此法在药物设计与合成中有广泛的应用。如图为蔗糖分子修饰得到的三氯蔗糖。下列说法不正确的是
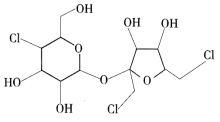

| A.电负性最大的元素为氧元素 |
| B.氯原子核外有17种空间运动状态不同的电子 |
| C.三氯蔗糖分子中含有9个手性碳原子 |
| D.三氯蔗糖易溶于水,与三氯蔗糖分子和水分子之间形成氢键有关 |
您最近一年使用:0次
10 . 下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
| A.氟化氢分子的极性强于氯化氢分子的极性 |
B. 键的键能小于 键的键能小于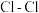 键的键能 键的键能 |
C.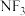 的键角比 的键角比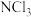 的小 的小 |
D.气态氟化氢中存在 ,而气态氯化氢中是 ,而气态氯化氢中是 分子 分子 |
您最近一年使用:0次
2024-02-19更新
|
176次组卷
|
3卷引用:黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期4月月考化学试题



