1 . 依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是_______ ;基态硫原子的价电子排布式是________ 。
(2)基态铁原子有____ 个未成对电子,基态 的价电子排布图为
的价电子排布图为______ 。
(3) 、K、O、F四种元素中第一电离能最小的是
、K、O、F四种元素中第一电离能最小的是______ ,电负性最大的是______ 。
(4)下列说法错误的是_______。
(5)过氧化氢( )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。 的电子式为
的电子式为______ ,结构式为_______ 。
② 中存在
中存在_____ 键和______ 键,为_____ (填“极性”或“非极性”)分子。
(1)基态硅原子的电子排布式是
(2)基态铁原子有
 的价电子排布图为
的价电子排布图为(3)
 、K、O、F四种元素中第一电离能最小的是
、K、O、F四种元素中第一电离能最小的是(4)下列说法错误的是_______。
A.元素的电负性: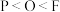 | B.元素的第一电离能: |
C.离子半径: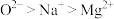 | D.原子的未成对电子数: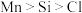 |
(5)过氧化氢(
 )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。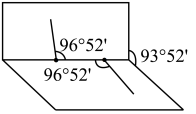
 的电子式为
的电子式为②
 中存在
中存在
您最近一年使用:0次
名校
2 . 科学家利用四种原子序数依次增大的短周期主族元素X、Y、Z、W“组合”成一种超分子,具有高效的催化性能,其分子结构示意图如图(注:实线代表共价键,其他重复单元的W、X未标注)。X、Z分别位于不同周期,Z的第一电离能在同周期元素中最小。下列说法中不正确的是


| A.电负性:W>Y>X | B.简单离子半径:Z<Y |
| C.Z与Y组成的化合物可能含有共价键 | D.该化合物中X、Y、W均满足8电子稳定结构 |
您最近一年使用:0次
3 . W、X、Y、Z、M、Q是原子序数依次递增的前四周期元素,W元素基态原子的三个能级上电子相同,Y元素基态原子核外有8种不同运动状态的电子,Y与Z位于同主族,M是前四周期基态原子核外未成对电子数最多的元素,Q元素位于ds区,常见的化合价有两种。回答下列问题:
(1)X、Z元素符号分别是___________ ,Q元素在周期表的位置是___________ ,M的基态原子的价电子排布式是___________ 。
(2)原子核外电子的运动有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为
号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为___________ ,基态的X原子最高能级的电子所在原子轨道的轮廓图形为___________ 。
(3)W、X、Y元素第一电离能最大的是___________ (用元素符号表示,下同),电负性最大的是___________ 。
(4)W与Z的化合物共用电子对偏向于Z,举出一个事实,说明Z的非金属性比W强(用化学方程式表示):___________ 。
(5)在较高温度下QY转化成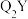 ,从原子结构角度分析
,从原子结构角度分析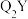 比QY更稳定的原因:
比QY更稳定的原因:___________ 。
(1)X、Z元素符号分别是
(2)原子核外电子的运动有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为
号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为(3)W、X、Y元素第一电离能最大的是
(4)W与Z的化合物共用电子对偏向于Z,举出一个事实,说明Z的非金属性比W强(用化学方程式表示):
(5)在较高温度下QY转化成
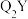 ,从原子结构角度分析
,从原子结构角度分析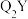 比QY更稳定的原因:
比QY更稳定的原因:
您最近一年使用:0次
名校
解题方法
4 . 下图为元素周期表的一部分,X、Y、Z、W均为短周期主族元素,Z的基态原子有3个未成对电子,下列比较中正确的是
| X | Y | |
| Z | W |
| A.原子半径:Y>X>Z>W | B.最高正化合价:Y>W>X=Z |
| C.第一电离能:Y>X>Z>W | D.电负性:Y>X>Z>W |
您最近一年使用:0次
名校
5 . 分子R称为“点击化学试剂”,如图所示。下列叙述错误的是
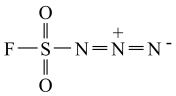
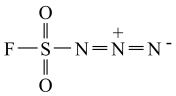
A.电负性: |
B.第一电离能: |
| C.S原子核外有6种运动状态不同的电子 |
| D.基态F原子核外电子占据3个能级 |
您最近一年使用:0次
2024-02-10更新
|
184次组卷
|
2卷引用:辽宁省沈阳市辽中区第一私立高级中学2023-2024学年高二上学期12月月考化学试题
6 . 酯在 溶液中发生水解反应,历程如下:
溶液中发生水解反应,历程如下: 水解相对速率与取代基R的关系如下表:
水解相对速率与取代基R的关系如下表:
下列说法不正确 的是
 溶液中发生水解反应,历程如下:
溶液中发生水解反应,历程如下: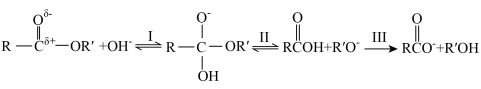
①
 水解相对速率与取代基R的关系如下表:
水解相对速率与取代基R的关系如下表:| 取代基R | 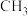 |  |  |
| 水解相对速率 | 1 | 290 | 7200 |
A.步骤I是 与酯中 与酯中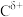 作用 作用 |
B.步骤III使I和Ⅱ平衡正向移动,使酯在 溶液中发生的水解反应不可逆 溶液中发生的水解反应不可逆 |
C.酯的水解速率: |
D. 与 与 反应、 反应、 与 与 反应,两者所得醇和羧酸盐均不同 反应,两者所得醇和羧酸盐均不同 |
您最近一年使用:0次
2024-02-02更新
|
2102次组卷
|
3卷引用:辽宁省沈阳市东北育才学校高中部2023-2024学年高三下学期第六次模拟考试化学试题
名校
解题方法
7 . 下列关于物质结构或性质及解释都正确的是
| 物质结构或性质 | 解释 | |
| A | 键角: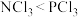 | N的电负性比P大,孤电子对对成键电子对的斥力比较大 |
| B | 稳定性:HF>HCl | HF分子间可以形成氢键,HCl没有氢键 |
| C | 配位键的稳定性: |  中O电负性更大,因而形成的配位键更稳定 中O电负性更大,因而形成的配位键更稳定 |
| D | 电子云半径:2s<4s | 4s电子能量高,在离核更远的区域出现的概率大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是原子半径最小的元素;B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是| A.A、B、C三种元素的电负性:C<B<A |
| B.B、C、D、E四种元素的第一电离能:B>C>E>D |
| C.B元素单质分子中π键和σ键的个数比为1:2 |
| D.F元素位于元素周期表d区 |
您最近一年使用:0次
2024-01-22更新
|
158次组卷
|
3卷引用:辽宁省葫芦岛市普通高中2023-2024学年高二上学期学业质量监测考试化学试题
解题方法
9 . 某食品添加剂的结构如图所示,其中W、X、Y、Z、Q为原子序数依次增大的短周期主族元素,Z核外最外层电子数与X核外电子总数相等,下列说法错误的是
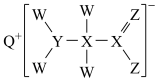
| A.电负性:Q>Z>Y>X |
| B.简单离子半径:Y>Z>Q |
| C.第一电离能:Y>Z>X>Q |
D.W能分别与X、Y和Z形成 分子 分子 |
您最近一年使用:0次
2024-01-19更新
|
206次组卷
|
2卷引用:辽宁省丹东市2023-2024学年高二上学期期末考试化学试题
10 . 填空。
(1)写出基态As原子的核外电子排布式:___________ ,根据元素周期律,原子半径Ga___________ (填“大于”或“小于”,下同)As,第一电离能Ga___________ As。
(2)C、N、O的第一电离能由大到小的顺序为___________ ;H、O、S电负性由大到小的顺序是___________ 。B和N相比,电负性较大的是___________ ;BN中B元素的化合价为___________ ;从电负性角度分析,C、Si、O的非金属活泼性由强至弱的顺序为___________ 。
(3)铬基态原子的电子排布式为___________ ,氯元素的基态原子的价层电子排布式是___________ ,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号)。
(4)基态Fe3+的M层电子排布式为___________ ,基态铝原子核外自旋平行的电子最多有___________ 个,与铝同族的第四周期元素原子的价层电子排布式为___________ ,基态磷原子的核外电子运动状态共有___________ 种,其价层电子排布式为___________ 。在硼、氧、氟、氮中第一电离能由大到小的顺序是___________ (用元素符号表示)。
(1)写出基态As原子的核外电子排布式:
(2)C、N、O的第一电离能由大到小的顺序为
(3)铬基态原子的电子排布式为
(4)基态Fe3+的M层电子排布式为
您最近一年使用:0次



