名校
1 . 短周期主族元素X、Y、Z、W的原子序数依次增大。基态Y原子最外层电子排布式为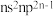 ,Y和W位于同主族,Z是短周期元素中金属性最强的元素。这四种元素的原子最外层电子数之和等于15。下列叙述正确的是
,Y和W位于同主族,Z是短周期元素中金属性最强的元素。这四种元素的原子最外层电子数之和等于15。下列叙述正确的是
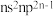 ,Y和W位于同主族,Z是短周期元素中金属性最强的元素。这四种元素的原子最外层电子数之和等于15。下列叙述正确的是
,Y和W位于同主族,Z是短周期元素中金属性最强的元素。这四种元素的原子最外层电子数之和等于15。下列叙述正确的是A.简单离子半径: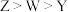 | B.电负性: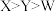 |
| C.ZXY含离子键和共价键 | D.工业上电解熔融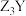 制备Z的单质 制备Z的单质 |
您最近一年使用:0次
2024-01-11更新
|
248次组卷
|
2卷引用:河北省石家庄市第九中学2023-2024学年高三上学期12月联考化学试题
名校
2 . 2022年诺贝尔化学奖授予了点击化学领域的三位科学家。一价铜催化的叠氮化物-炔烃环加成反应可谓点击化学中的第一个经典之作,催化剂CuCl的晶体结构如图所示,下列说法错误的是
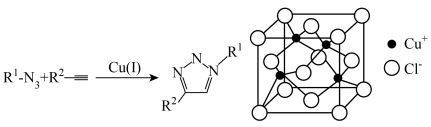

| A.N、O、Cu的电负性从大到小的顺序是N>O>Cu |
B.基态 的简化电子排布式为 的简化电子排布式为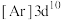 |
C.晶胞结构中, 的配位数为4 的配位数为4 |
D.若晶体的密度为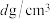 ,则晶胞参数 ,则晶胞参数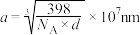 |
您最近一年使用:0次
名校
解题方法
3 . 由原子序数依次增大的短周期元素X、Y、Z、W、R组成的一种离子液体(其阳离子中五元环上5个原子共面),其结构如图。Z的最简单氢化物易液化,可用作制冷剂。W的氢化物的水溶液能腐蚀玻璃,Z、R为同一主族元素。下列说法错误的是
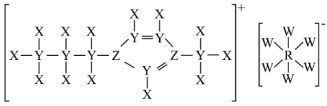
| A.电负性:W>Z>Y |
| B.该离子液体中的Z原子的杂化方式均为sp2 |
C.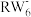 空间结构为正八面体形 空间结构为正八面体形 |
| D.最简单氢化物的沸点:Z<R |
您最近一年使用:0次
4 . 光电材料[氟代硼铍酸钾晶体(KBe2BO3F2)、CaTiO3等]是目前科学家特别关注的材料。KBe2BO3F2(晶胞结构如图a,其中氧原子已省略,图a中的原子分别位于晶胞的顶点、棱及面上)是一种可制造出深紫外固体激光器的光电材料,可由BeO、KBF4和B2O3在一定条件下制得,同时放出BF3气体;CaTiO3(晶胞结构如图b)在光、电、热等领域有着独特的性质特征。
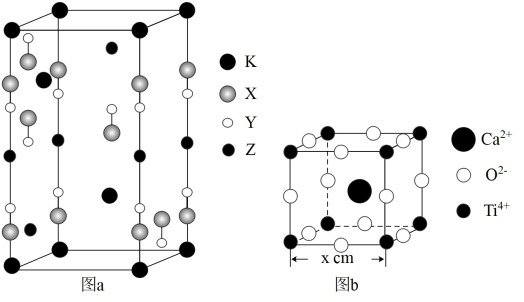
(1)基态Ti原子的核外电子排布式为____ 。
(2)KBF4是离子化合物,BF3、BF 中B原子的杂化方式依次为
中B原子的杂化方式依次为____ 、____ 。
(3)KBe2BO3F2的组成元素中,非金属元素的电负性由强到弱的顺序为____ (填元素符号),基态原子的第一电离能:Be____ (填“>”或“<”)B。
(4)图a中,已知原子半径X>Y,X、Z分别表示____ 、____ 。(填元素符号)
(5)图b中,与Ti4+最近且距离相等的氧离子构成的几何图形为____ ,若设晶胞边长为xcm,则Ti4+与最近的 间的距离为
间的距离为____ (填含x的表达式)cm;表示该晶体的晶胞还可以有另一种画法,将Ca2+置于立方体的顶点,则Ti4+的位置是____ 。

(1)基态Ti原子的核外电子排布式为
(2)KBF4是离子化合物,BF3、BF
 中B原子的杂化方式依次为
中B原子的杂化方式依次为(3)KBe2BO3F2的组成元素中,非金属元素的电负性由强到弱的顺序为
(4)图a中,已知原子半径X>Y,X、Z分别表示
(5)图b中,与Ti4+最近且距离相等的氧离子构成的几何图形为
 间的距离为
间的距离为
您最近一年使用:0次
解题方法
5 . 化合物A (结构如下图)由原子序数依次增大的X、Y、Z、W短周期元素组成,常用来做金属矿物的浮选剂。已知Z与W位于不同周期。下列说法正确的是


| A.四种元素中X的电负性最小 |
| B.最简单气态氢化物的稳定性:Z<Y |
| C.W位于周期表的第二周期VIA族 |
| D.四种元素可组成既含离子键又含共价键的化合物 |
您最近一年使用:0次
2023-02-14更新
|
313次组卷
|
2卷引用:河北省唐山市2022-2023学年高二上学期期末考试化学试题
名校
解题方法
6 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 三氟乙酸酸性强于三氯乙酸 | F原子电负性大于Cl原子,吸电子能力强 |
| B | 常温下,铜与稀硫酸不反应,与稀硝酸反应 | 硝酸酸性强于硫酸 |
| C | 常温下溶解度: 大于 大于 |  水解程度大于 水解程度大于 |
| D |  、 、 混合气体通入 混合气体通入 溶液中产生的白色沉淀是 溶液中产生的白色沉淀是 | 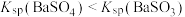 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 物质结构决定物质性质,下列性质不能通过元素的电负性进行解释的是
A. 的沸点高于 的沸点高于 的沸点 的沸点 |
| B.乙烯能发生加成反应,而乙烷不能 |
C. 酸性大于 酸性大于 的酸性 的酸性 |
D.气态氟化氢中存在 分子,而气态氯化氢中只存在 分子,而气态氯化氢中只存在 分子 分子 |
您最近一年使用:0次
2024-04-10更新
|
263次组卷
|
2卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高三下学期模拟演练化学试题
8 . 氮化锗(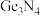 )具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
)具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
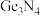 )具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是
)具有耐腐蚀、硬度高等优点,应用广泛。下列说法正确的是| A.锗是金属,不能做半导体材料 |
| B.第4周期基态原子与锗未成对电子数相等的元素共有2种 |
C.基态锗原子的电子排布式可表示为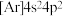 |
| D.氮化锗中氮显-3价,说明氮的电负性比锗大 |
您最近一年使用:0次
2022-10-08更新
|
281次组卷
|
2卷引用:河北省石家庄市第十七中学2022-2023高二下学期第一次月考化学试题
解题方法
9 . X、Y、Z、M是电负性逐渐减小的短周期非金属元素。X、Z、M位于三个不同周期,Y与Z的价电子数之和为M价电子数的两倍;化合物 的电子总数为18个。下列说法错误的是
的电子总数为18个。下列说法错误的是
 的电子总数为18个。下列说法错误的是
的电子总数为18个。下列说法错误的是| A.Y的含氧酸为弱酸 |
| B.Z与M形成的化合物具有较强的还原性 |
| C.简单氢化物的稳定性:X>Y>M |
| D.原子半径:Z<X<Y<M |
您最近一年使用:0次
名校
解题方法
10 . 现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B元素基态原子中能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(2)E位于第_______ 族_______ 区,该元素原子的核外电子排布式为_______ 。
(3)已知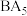 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:_______ 。
(4)检验D元素的方法是_______ ,请用原子结构的知识解释产生此现象的原因:_______ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
C元素的第一至第四电离能如下: 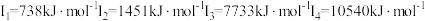 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第七列 |
(2)E位于第
(3)已知
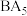 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:(4)检验D元素的方法是
您最近一年使用:0次



